Clear Sky Science · pl
Pozycje R5 i R7 w szkielecie fluorochinolonów napędzają rozpad filamentów F-aktyny
Przekształcanie antybiotyków w pomocników mózgu
Wiele powszechnych zaburzeń mózgu, od choroby Alzheimera po chorobę Parkinsona, ma wspólnego ukrytego sprawcę: drobne strukturalne pręty wewnątrz komórek nerwowych, które z czasem zablokowują się i sztywnieją. Te pręty zbudowane są z białka zwanego aktyną, która w normalnych warunkach stanowi elastyczną część wewnętrznego rusztowania komórki. W badaniu tym badacze rozważają zaskakującą możliwość — że dobrze znana klasa antybiotyków, fluorochinolony, mogłaby zostać przeprojektowana tak, by łagodnie rozluźniać te szkodliwe agregaty aktyny i potencjalnie pomagać chronić mózg.
Gdy rusztowanie komórkowe zawodzi
Zdrowe komórki mózgowe nieustannie przekształcają swoje wewnętrzne szkieletowe struktury, by tworzyć i przebudowywać połączenia. Filamenty aktynowe są kluczowe w tym procesie — formują się i rozpuszczają w zależności od potrzeb. Pod wpływem stresu aktyna może jednak zablokować się w uporczywych, prętowych agregatach, które zatykają komórkę, zaburzają transport niezbędnego ładunku i sprzyjają gromadzeniu białek powiązanych z chorobami, takich jak amyloid i tau. Z upływem lat te pręty mogą dojrzewać do gęstych struktur znanych jako ciała Hirano, często obserwowanych w mózgach osób z różnymi schorzeniami neurodegeneracyjnymi. Ponieważ dostępne leki celujące w aktynę bywają bardzo toksyczne, badacze dążą do znalezienia bezpieczniejszych małych cząsteczek, które potrafiłyby poluzować te agregaty bez uszkadzania komórek.
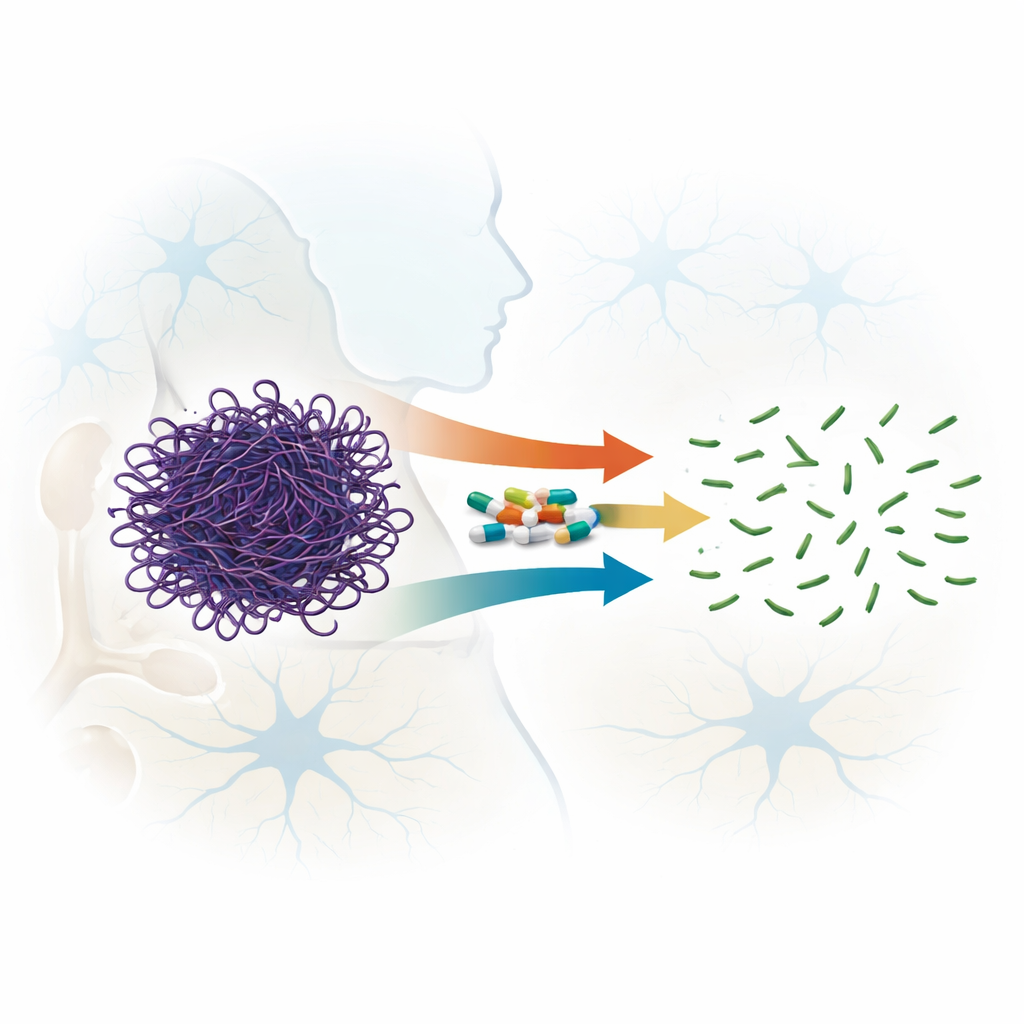
Nieoczekiwany talent znanych leków
Fluorochinolony to antybiotyki o szerokim spektrum działania stosowane na całym świecie w leczeniu zakażeń; niektóre nowsze związki z tej rodziny potrafią przenikać barierę krew–mózg. Wcześniejsze wskazówki sugerowały, że niektóre fluorochinolony mogą destabilizować filamenty aktynowe. W tej pracy autorzy systematycznie porównali siedem spokrewnionych związków, obejmujących cztery generacje tej rodziny leków, aby sprawdzić, jak skutecznie rozbijają już uformowane filamenty aktyny, a nie tylko zapobiegają ich powstawaniu. Przy użyciu pomiarów rozpraszania światła, mikroskopii elektronowej i filtracji na żelu wykazali, że wszystkie testowane leki potrafią zakłócać filamenty aktynowe, ale o bardzo różnej sile działania. Dwa związki — sparfloksacyna (z trzeciej generacji) i moksyfloksacyna (czwartej generacji) — wyróżniały się szybkim i nieodwracalnym rozdrabnianiem długich filamentów na znacznie krótsze fragmenty, nawet przy stosunkowo niskich stosunkach leku do białka.
Obserwowanie, jak filamenty się rozpadają
Obrazowanie o wysokiej rozdzielczości i testy biofizyczne ujawniły, jak filamenty zmieniają się pod wpływem leczenia. Mikroskopia elektronowa pokazała, że nieleczona aktyna tworzy długie, ciągłe pasma, podczas gdy skuteczne fluorochinolony przekształcają je w krótkie, rozrzucone fragmenty. Mniej aktywne związki powodowały pojawienie się zgiętych i wykrzywionych filamentów, ale nie prowadziły do ich całkowitego rozbicia. Pomiary termiczne stabilności białka potwierdziły tę fizyczną dezintegrację: po leczeniu aktyna zachowywała się bardziej jak forma wolna, niezespolona, o niższej temperaturze topnienia, przy czym jej podstawowa struktura budulcowa pozostawała niemal niezmieniona. Wskazuje to, że leki nie denaturują ani nie uszkadzają samej aktyny — głównie rozrywają sposób, w jaki jednostki łączą się we filamenty.
Powiększając molecularny uchwyt
Aby zrozumieć, dlaczego niektóre fluorochinolony działają lepiej od innych, zespół połączył zaawansowane eksperymenty magnetycznego rezonansu jądrowego z symulacjami komputerowymi interakcji lek–białko. Odkryli, że wszystkie związki opierają się na wspólnym pierścieniowym „rdzeniu”, który nawiązuje kontakt z aktyną, zwłaszcza w dwóch pozycjach na tym rdzeniu, które wielokrotnie dotykają filamentu. Jednak dodatkowe grupy chemiczne przyłączone w określonych miejscach — oznaczonych jako R5 i R7 — silnie wpływają na to, jak mocno i gdzie każda cząsteczka wiąże się z aktyną. W najbardziej efektywnych czynnikach te pozycje noszą grupę aminową i rozbudowane systemy pierścieniowe, które sięgają do małej kieszonki na styku sąsiadujących nici aktyny. Tam zakłócają kluczowe stabilizujące kontakty, w tym ważny most soli, który zwykle pomaga utrzymać filamenty razem.
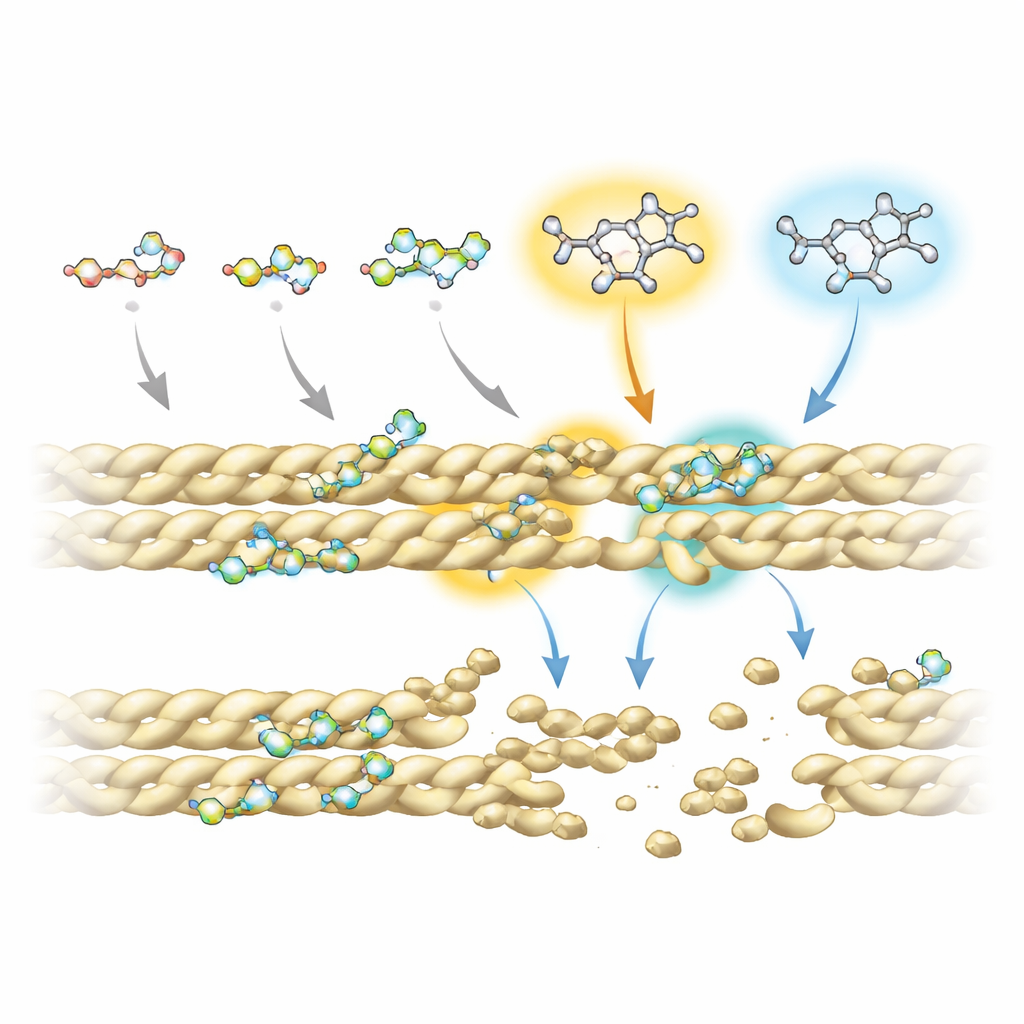
Od drożdży do przyszłych terapii
Badacze przetestowali również leki na szczepie drożdży, który naturalnie gromadzi pęczki aktyny, naśladując aspekty komórek chorych. W mikroskopie nieleczone drożdże wykazywały duże, jasne grudki aktyny, podczas gdy komórki eksponowane na fluorochinolony — szczególnie sparfloksacynę, moksyfloksacynę i przy wyższych dawkach kwas nalidyksowy — ujawniały znacznie bardziej rozproszone, punktowe wzory, co wskazuje, że pęczki zostały rozbite. Co ważne, działanie leków wydawało się relatywnie łagodne: osłabiały upakowanie filamentów bez poważnego zniekształcania podstawowego kształtu aktyny, a ich wiązanie było słabsze niż w przypadku klasycznych toksyn aktyny, co potencjalnie zmniejsza ryzyko poważnych działań niepożądanych.
Projektowanie mądrzejszych leków celujących w aktynę
Podsumowując, badanie pokazuje, że drobne modyfikacje dobrze znanych antybiotyków mogą dramatycznie zmieniać ich interakcję z wewnętrznym rusztowaniem komórki. Wskazując pozycje R5 i R7 jako kluczowe „pokrętła sterujące” zarówno dla rozkładu aktyny, jak i penetracji do mózgu, autorzy szkicują plan tworzenia nowych cząsteczek inspirowanych fluorochinolonami, które selektywnie rozmontowują szkodliwe agregaty aktyny. Choć te odkrycia stanowią wczesne, laboratoryjne dowody na zasadę działania, otwierają możliwość, że przyszłe leki pochodne znanych antybiotyków mogą pomóc oczyścić toksyczne rusztowania w komórkach nerwowych i spowolnić lub zapobiec niektórym postaciom neurodegeneracji.
Cytowanie: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Słowa kluczowe: agregaty aktyny, antybiotyki fluorochinolonowe, choroby neurodegeneracyjne, ponowne zastosowanie leków, cytoszkielet