Clear Sky Science · pl
Ekspresja ACE2 w komórkach nabłonka okrężnicy wiąże się z infekcją wirusową, odpornością i metabolizmem energetycznym
Dlaczego jelito ma znaczenie w przypadku wirusa oddechowego
Kiedy myślimy o COVID-19, wyobrażamy sobie płuca wypełniające się płynem i pacjentów z trudnościami w oddychaniu. Jednak wiele osób zakażonych SARS-CoV-2 ma też bóle brzucha, biegunkę i długotrwałe problemy jelitowe. Badanie to analizuje, dlaczego jelita — a w szczególności okrężnica — mogą być ważnym celem dla wirusa. Dzięki przyjrzeniu się pojedynczym komórkom pochodzącym z okrężnicy dzieci naukowcy pokazują, że kluczowy „wejściowy” białkowy receptor wirusa, ACE2, jest wysoce aktywny w określonych komórkach jelita i wiąże się nie tylko z infekcją wirusową, ale też z mechanizmami odpornościowymi i sposobem gospodarowania energią przez komórki.
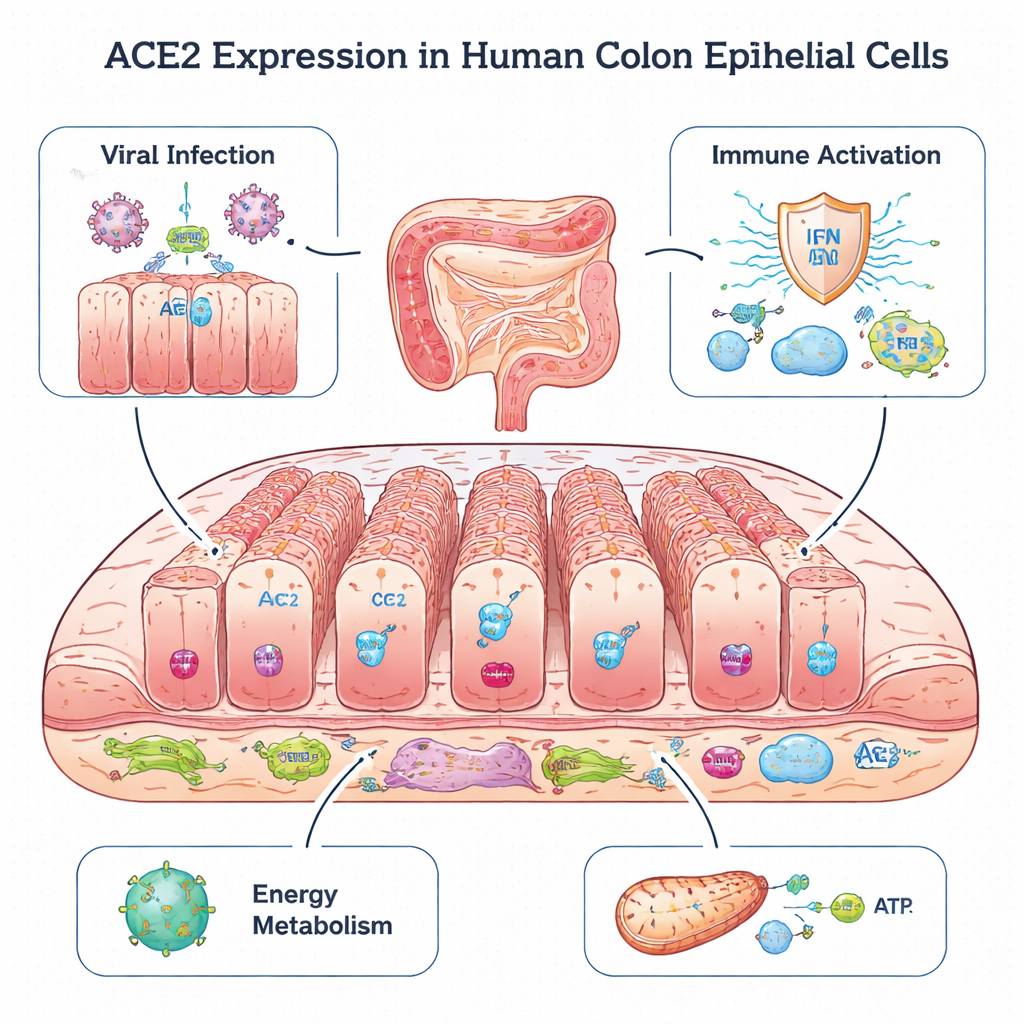
Komórkowe „wejście” w okrężnicy
ACE2 jest najlepiej znane jako główny punkt wejścia, którego używa zarówno pierwotny wirus SARS, jak i SARS-CoV-2 do zakażania komórek płuc. Paradoksalnie badania na zwierzętach sugerują, że ACE2 może także chronić tkanki przed uszkodzeniem, pomagając utrzymać równowagę układu hormonalnego kontrolującego ciśnienie krwi. W jelicie ACE2 jest już powiązane ze wspieraniem zdrowej mikroflory i zapobieganiem stanom zapalnym. W tej pracy naukowcy ponownie przeanalizowali dane z sekwencjonowania RNA pojedynczych komórek (single-cell RNA-seq) pochodzące z biopsji okrężnicy 17 dzieci: część miała zdrowe jelita, inni mieli zapalenie okrężnicy lub zapalne choroby jelit, w tym wrzodziejące zapalenie jelita grubego i chorobę Leśniowskiego-Crohna. Ta technika pozwoliła zobaczyć, które geny są aktywne w tysiącach pojedynczych komórek i dokładnie określić, gdzie ACE2 jest włączone.
Kolonocyty: główne cele i pierwsi sygnalizatorzy
Analiza wykazała, że ACE2 jest skoncentrowane niemal wyłącznie w kolonocytach — głównym typie komórek nabłonkowych wyściełających wnętrze okrężnicy i zwróconych ku zawartości jelita. W porównaniu z innymi komórkami nabłonkowymi kolonocyty wykazywały wyższą aktywność genów ułatwiających wirusom wnikanie do komórki, pączkowanie i opuszczanie komórek. Jednocześnie komórki te wyrażały wiele genów zaangażowanych w wykrywanie materiału genetycznego wirusów i uruchamianie odpowiedzi interferonów typu I i III — kluczowych wczesnych alarmów układu odpornościowego. Produkowały też sygnały zapalne i cząsteczki prezentujące fragmenty wirusa limfocytom T, co sugeruje, że kolonocyty są zarówno potencjalnymi celami wirusa, jak i ważnymi wczesnymi strażnikami alarmującymi układ odpornościowy.
Powiązane sieci odporności i wykorzystania energii
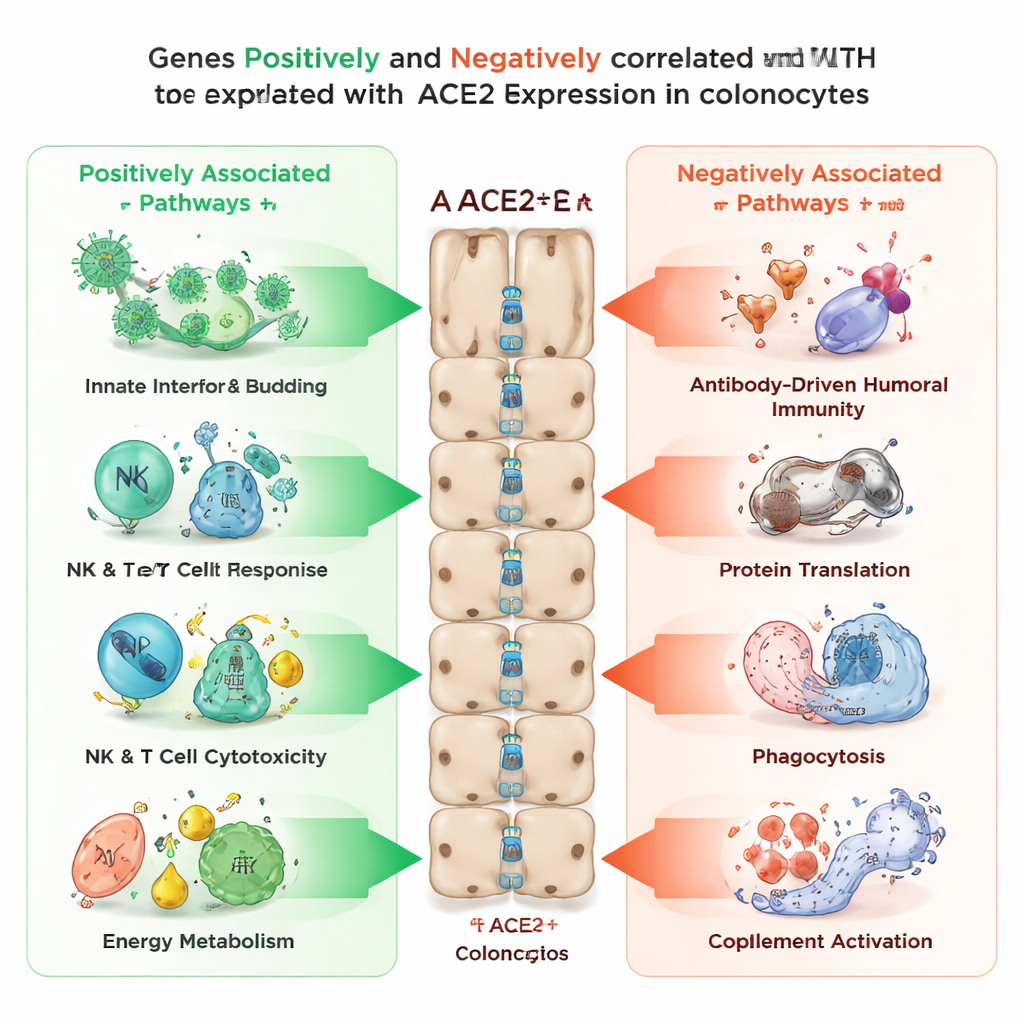
Następnie badacze sprawdzili, które inne geny mają tendencję do włączania się lub wyłączania razem z ACE2 w kolonocytach. Znaleźli ponad 3 400 genów, których ekspresja rosła wraz z poziomem ACE2, oraz ponad 2 100 genów, których ekspresja malała wraz ze wzrostem ACE2. Geny skorelowane dodatnio z ACE2 były wzbogacone w procesy związane z wnikaniem i uwalnianiem wirusów, sygnalizacją odporności wrodzonej, cytotoksyczną aktywnością komórek NK i limfocytów T oraz kilkoma ścieżkami produkcji energii wewnątrzkomórkowej, w tym funkcjonowaniem mitochondriów oraz przetwarzaniem tłuszczów i cukrów. Natomiast geny poruszające się w przeciwnym kierunku — wysokie, gdy ACE2 było niskie — wiązały się z odpornością humoralną opartą na przeciwciałach, aparatem syntezy białek komórki, procesami „zjadania” komórek takimi jak fagocytoza oraz układem dopełniacza, innym ramieniem obrony immunologicznej. Ten wzorzec sugeruje, że ACE2 oznacza stan, w którym kolonocyty są nastawione na szybkie wykrywanie wirusów i produkcję energii, podczas gdy inne, wolniejsze programy odpornościowe są przyciszone.
Dane z zapalnych jelit
Aby sprawdzić, czy te wzorce występują w rzeczywistych tkankach, zespół zastosował multiplexową immunofluorescencję — technikę, która uwidacznia konkretne białka różnymi kolorami — na próbkach okrężnicy dzieci z wrzodziejącym zapaleniem jelita grubego, chorobą Crohna i od osób kontrolnych. Potwierdzili, że białko ACE2 znajduje się głównie na komórkach nabłonkowych oznaczonych EPCAM. U pacjentów z zapalnymi chorobami jelit komórki pozytywne dla ACE2 wykazywały wyższe poziomy IFNA4 i RSAD2, dwóch białek silnie związanych z sygnalizacją interferonów i aktywnością przeciwwirusową. Wskazuje to, że w zapalnym jelicie komórki kolonów z ACE2 nie są tylko potencjalnymi bramami dla wirusów; są także ogniskami odpowiedzi przeciwwirusowej.
Co to oznacza dla pacjentów i przyszłych terapii
Dla osób niebędących specjalistami komunikat jest taki: okrężnica nie jest biernym obserwatorem w przebiegu COVID-19. To samo białko, które pozwala wirusowi wejść do komórek, pomaga też koordynować odporność jelitową i wykorzystanie energii, szczególnie u dzieci z istniejącym wcześniej zapaleniem jelit. Ta podwójna rola może pomóc wyjaśnić, dlaczego niektórzy pacjenci rozwijają objawy żołądkowo-jelitowe oraz dlaczego osoby z zapalnymi chorobami jelit mają złożone, lecz niekoniecznie gorsze, wyniki przebiegu COVID-19. Praca ta wpisuje się także w szersze dyskusje o lekach wpływających na krzepnięcie krwi i szlaki regulujące ciśnienie, z których niektóre mogą łagodzić uszkodzenia płuc i naczyń w ciężkich infekcjach. Choć badanie opiera się na korelacjach i nie dowodzi związku przyczynowo-skutkowego, podkreśla kolonocyty bogate w ACE2 jako ważnych graczy na skrzyżowaniu wejścia wirusa, obrony immunologicznej i metabolizmu — wskazując jelito jako kluczowe, a potencjalnie możliwe do leczenia, pole w chorobie koronawirusowej.
Cytowanie: Qi, Y., Huang, Y., Chen, H. et al. ACE2 expression by colonic epithelial cells is associated with viral infection, immunity, and energy metabolism. Sci Rep 16, 5738 (2026). https://doi.org/10.1038/s41598-026-36052-w
Słowa kluczowe: ACE2, kolonocyty, COVID-19 jelita, zapalne choroby jelit, odporność przeciwwirusowa