Clear Sky Science · pl
Analiza proteomiczna sekretomu komórek progenitorowych śródbłonka identyfikuje Serpine 1 jako silny regulator osteogenezy
Gojenie złamanej kości bez przeszczepów dawcy
Gdy kość jest poważnie złamana lub brakuje jej fragmentu, chirurdzy często mają problem z przywróceniem jednocześnie wytrzymałości i kształtu. Obecne opcje — pobranie kości z innej części ciała lub użycie syntetycznych przeszczepów — mogą być bolesne, obarczone ryzykiem i nie zawsze skuteczne. W tym badaniu rozważa się inną koncepcję: zamiast przeszczepiać komórki, czy można dostarczyć odpowiednie naturalne białka, które uruchomią własne mechanizmy budujące kość organizmu?
Dlaczego niektóre urazy kości nie chcą się zarośnieć
Większość złamań goi się samoistnie, ale duże ubytki kości — na przykład w wyniku urazu, nowotworów lub znacznej zanikowej utraty kości żuchwy — często tego nie robią. W takich przypadkach organizm po prostu nie ma wystarczającej liczby lokalnych komórek naczyń krwionośnych i komórek macierzystych tworzących kość, by odbudować brakujący fragment. Naukowcy zajmujący się inżynierią tkankową próbują rozwiązać ten problem, łącząc trzy składniki: żywe komórki zdolne do tworzenia nowej kości, rusztowanie dające im podłoże do wzrostu oraz sygnały mówiące, co robić. Przeszczepy komórek mogą działać, ale są kosztowne, silnie regulowane i nie zawsze praktyczne w codziennej praktyce klinicznej. To skłoniło badaczy do poszukiwania „bezkomórkowych” rozwiązań opartych na inteligentnych biomateriałach i precyzyjnie dobranych białkach.
Ukryte sygnały od komórek budujących naczynia
Komórki progenitorowe śródbłonka to rzadkie komórki krwi, które pomagają formować nowe naczynia krwionośne. Wcześniejsze badania wykazały, że gdy te komórki są wszczepiane w pobliże kości, wspierają gojenie — w dużej mierze przez wydzielanie rozpuszczalnych sygnałów, a nie przez przekształcanie się w kość. W nowym badaniu autorzy zebrali płyn hodowlany, w którym te komórki rosły, i zastosowali zaawansowaną analizę białek, aby skatalogować setki wydzielanych molekuł. Skoncentrowali się na ośmiu białkach silnie powiązanych z angiogenezą i osteogenezą. Przy użyciu ludzkich komórek macierzystych szpiku kostnego i ludzkich mikrośródbłonkowych komórek śródbłonka in vitro systematycznie testowali, które z tych białek najlepiej zwiększają proliferację, kierują migracją i wywołują odkładanie minerału podobnego do kości.
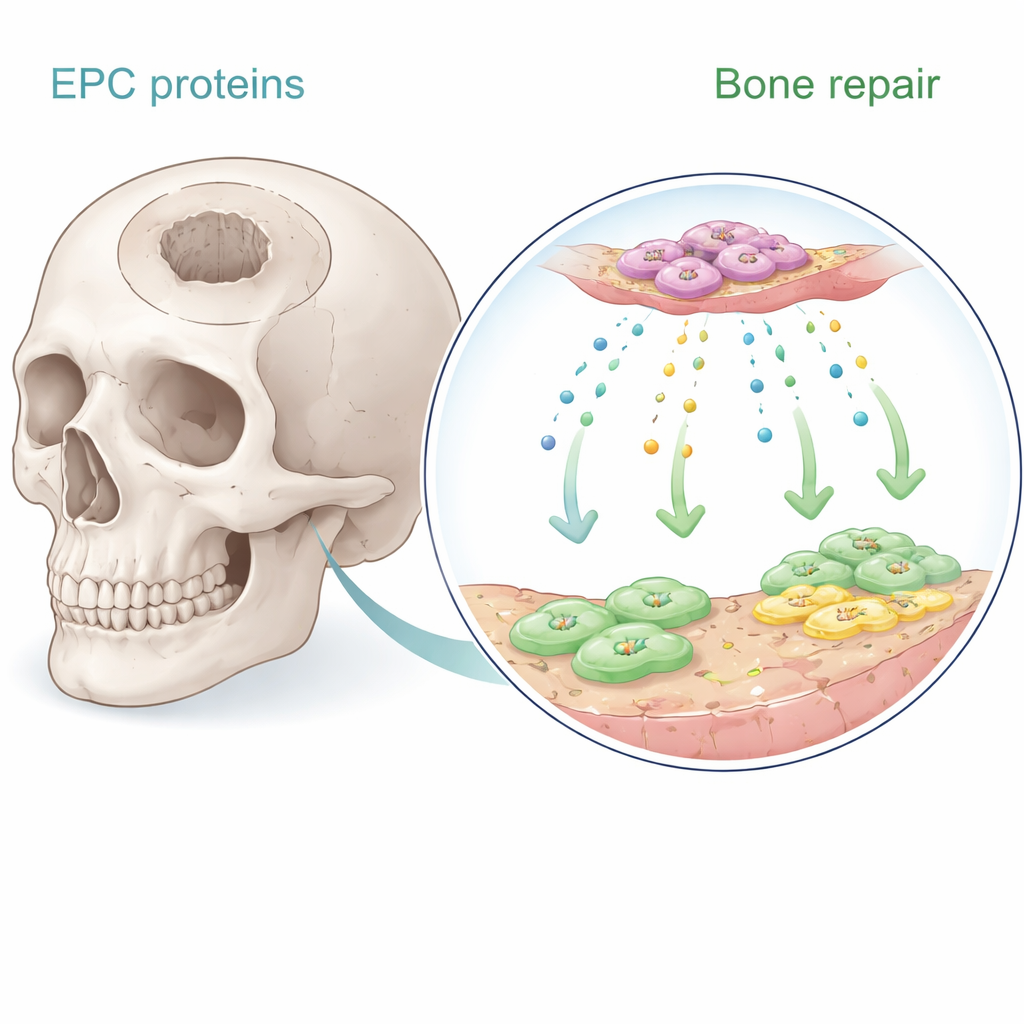
Zaskakujące białko wychodzi na prowadzenie
Wśród kandydatów wyróżniło się jedno białko: Serpine-1, lepiej znane z roli w regulacji krzepnięcia i gojenia ran. W hodowlach Serpine-1 istotnie zwiększał proliferację zarówno komórek macierzystych szpiku, jak i komórek śródbłonka w sposób zależny od dawki, przewyższając pod tym względem znane czynniki wzrostu, takie jak BMP-2 i SDF-1. Promował też dojrzewanie komórek macierzystych w kierunku komórek tworzących kość, co wykazano klasycznymi metodami barwienia uwidaczniającymi aktywność fosfatazy alkalicznej i osady bogate w wapń. Inne białka, jak czynnik wzrostu pochodzący od płytek (PDGF) i BMP-2, były skuteczniejsze w zachęcaniu komórek do przemieszczania się w testach migracji, ale Serpine-1 oferował rzadkie połączenie stymulowania zarówno liczby komórek, jak i zachowań sprzyjających tworzeniu kości.
Przekształcenie białka w praktyczny implant
Odnalezienie obiecującego białka to tylko połowa wyzwania; trzeba je jeszcze dostarczyć do miejsca urazu w sposób kontrolowany. Zespół enkapsulował Serpine-1 w małych biodegradowalnych kulkach z medycznego polimeru PLGA, a następnie wymieszał te mikrokulki z miękkim żelem kolagenowym. Powstało rusztowanie uwalniające białko stopniowo w czasie. Przetestowali je na myszach, wykonując okrągły otwór o średnicy 4 milimetrów w czaszce — wielkość defektu, która sama się nie goi. Niektóre defekty wypełniono samym kolagenem, niektóre kolagenem z pustymi mikrokulkami, a niektóre rusztowaniem z załadowanym Serpine-1. Po ośmiu tygodniach wysokorozdzielcze skany mikro-CT wykazały, że grupa z Serpine-1 miała istotnie większą objętość kości, gęstość i grubość wewnątrz defektu. Co godne uwagi, tylko te zwierzęta rozwinęły nową tkankę kostną w centrum ubytku, a nie tylko wzdłuż jego krawędzi.
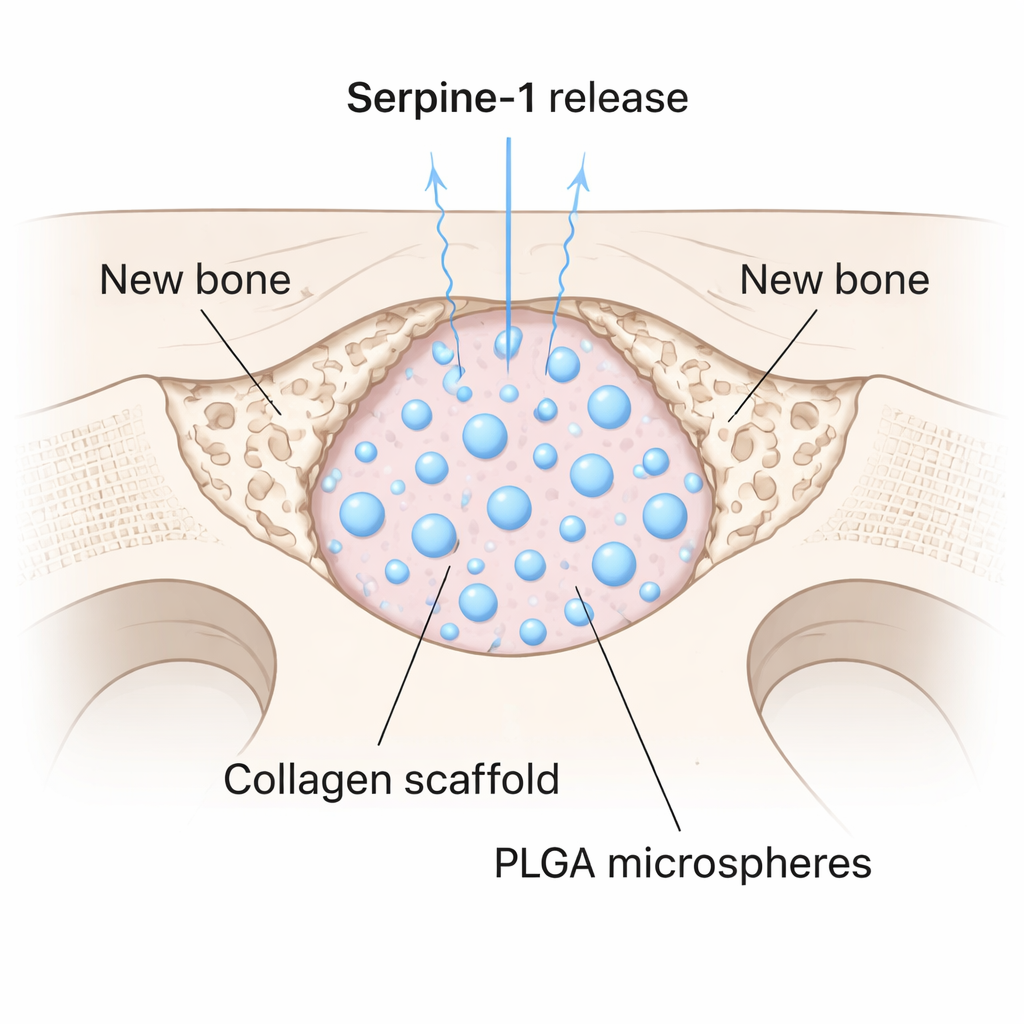
Co to może znaczyć dla przyszłej opieki nad kośćmi
Badanie przedstawia Serpine-1 jako silny i wcześniej niedoceniany sygnał sprzyjający tworzeniu kości. Łącząc to białko z rusztowaniem o powolnym uwalnianiu, badacze uzyskali istotny odrost kości w defekcie, który normalnie pozostałby pusty. Choć Serpine-1 nie przyciągał komórek do defektu tak skutecznie jak niektóre inne czynniki, jego zdolność do wspierania namnażania i dojrzewania istniejących komórek sugeruje, że można go połączyć z białkami promującymi migrację dla jeszcze lepszych efektów. Dla pacjentów takie bezkomórkowe, oparte na białkach materiały mogłyby kiedyś zmniejszyć potrzebę pobierania kości z własnego organizmu lub polegania na złożonych terapiach komórkowych, oferując prostszy sposób nakłonienia opornych urazów kości do ostatecznego wygojenia.
Cytowanie: Asbi, T., Tamari, T., Doppelt-Flikshtain, O. et al. Proteomic analysis of endothelial progenitor cells secretome identifies Serpine 1 as a potent regulator of osteogenesis. Sci Rep 16, 5165 (2026). https://doi.org/10.1038/s41598-026-36048-6
Słowa kluczowe: regeneracja kości, Serpine-1, inżynieria tkankowa, komórki progenitorowe śródbłonka, rusztowanie kolagenowe