Clear Sky Science · pl
Klasyfikacja stopnia demencji związanej z chorobą Alzheimera na podstawie rezonansu magnetycznego z użyciem optymalizacji bezpochodnej sieci konwolucyjnej
Pomoc lekarzom w wcześniejszym wykrywaniu demencji
W miarę starzenia się społeczeństw wiele rodzin obawia się utraty pamięci i demencji. Badania mózgu mogą ujawnić wczesne zmiany powiązane z chorobą Alzheimera, ale przeglądanie tysięcy obrazów wzrokowo jest powolne i trudne, nawet dla ekspertów. W tym badaniu przedstawiono inteligentne narzędzie komputerowe, które analizuje skany MRI mózgu i klasyfikuje osoby na cztery poziomy nasilenia demencji, od braku demencji po umiarkowane upośledzenie. System zaprojektowano tak, by był zarówno wyjątkowo dokładny, jak i na tyle lekki, by działać na zwykłych komputerach szpitalnych, co zwiększa dostępność zaawansowanej analizy obrazów.
Nowy inteligentny asystent do analizy skanów mózgu
Naukowcy skupili się na typie sztucznej inteligencji zwanej siecią konwolucyjną (CNN), która świetnie radzi sobie z wykrywaniem wzorców na obrazach. Zamiast jedynie stwierdzać, czy ktoś ma chorobę Alzheimera, ich narzędzie rozróżnia cztery stadia: brak demencji, bardzo łagodne, łagodne i umiarkowane. W tym celu zespół trenował model na dużych publicznych zbiorach skanów MRI, które zostały wcześniej oznaczone przez ekspertów. Cel był dwojaki: osiągnąć niemal perfekcyjną dokładność oraz zachować kompaktowość i szybkość modelu, aby był praktyczny w codziennej pracy klinicznej, a nie tylko w dobrze finansowanych laboratoriach badawczych.
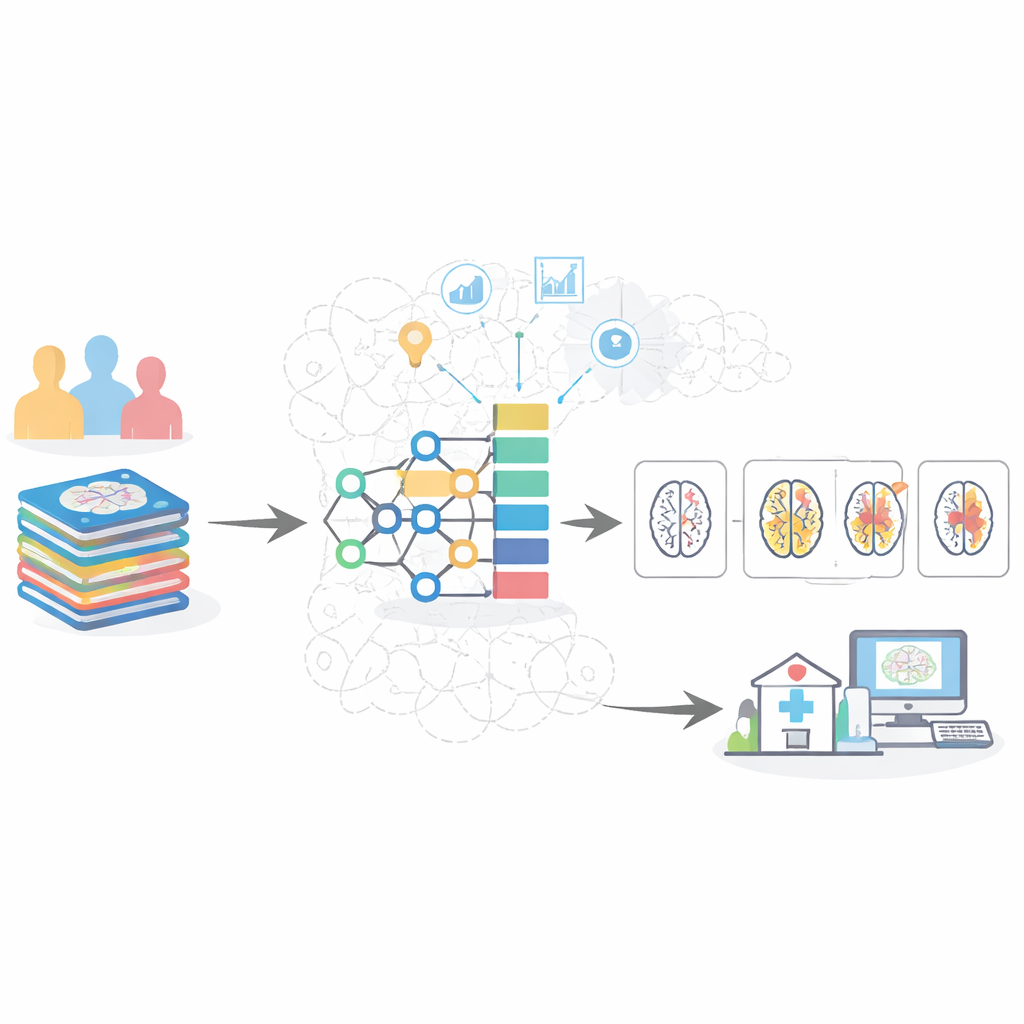
Wyważanie danych i oczyszczanie obrazów
Kluczowym wyzwaniem w danych medycznych jest nierównomierna reprezentacja poszczególnych stadiów choroby. W tych zbiorach skanów najczęstsze są przypadki osób zdrowych i z bardzo łagodnymi objawami, podczas gdy skany osób z umiarkowaną demencją są znacznie rzadsze. Standardowe systemy AI mają wtedy tendencję do „bezpiecznego” faworyzowania często występujących klas i pomijania przypadków wczesnych lub umiarkowanych. Aby temu przeciwdziałać, autorzy zastosowali dwuetapową strategię: najpierw usunęli mylące obrazy graniczne, a potem stworzyli realistyczne syntetyczne przykłady dla niedostatecznie reprezentowanych stadiów. Równocześnie starannie przygotowali każdy przekrój MRI poprzez filtrowanie, izolowanie mózgu od tkanek otaczających oraz normalizację jasności i kontrastu, tak by model mógł skupić się na medycznie istotnych cechach, takich jak kurczenie się głębokich struktur pamięciowych i poszerzanie przestrzeni wypełnionych płynem.
Projektowanie mniejszej, sprytniejszej sieci
Zamiast polegać na tradycyjnych metodach trenowania opartych na śledzeniu gradientów, zespół użył rodziny technik tzw. optymalizacji bezpochodnej. Rozpoczęli od większej, konwencjonalnej sieci CNN, a następnie użyli przeszukiwania ewolucyjnego i neural architecture search, aby ewoluować prostszy projekt zaledwie z trzema warstwami konwolucyjnymi i znacznie mniejszą liczbą filtrów. Optymalizacja bayesowska dostroiła sposób trenowania sieci, a symulowane wyżarzanie i przycinanie usunęły zbędne połączenia po treningu. Końcowy efekt, nazwany DAPA-CNN, ma około 85% mniej regulowanych parametrów niż model wyjściowy, zużywa około jednej czwartej pamięci i trenuje w mniej niż dwóch trzecich czasu, a mimo to wychwytuje kluczowe wzorce na skanach.
Bliska perfekcji sprawność i czytelne wizualne wyjaśnienia
Mimo mniejszego rozmiaru DAPA-CNN okazał się niezwykle dokładny. Na dużym zbiorze danych dotyczących choroby Alzheimera przypisywał stadium demencji prawidłowo w niemal każdym przypadku, a miary jakościowe, w tym dokładność, oscylowały wokół 99%. Model dobrze uogólnił także na odrębnym, wieloośrodkowym zbiorze zebranym na różnych skanerach, co sugeruje odporność na rzeczywiste wariacje w obrazowaniu. Aby uczynić system bardziej przejrzystym dla klinicystów, autorzy wygenerowali mapy aktywacji klas — nakładki przypominające mapy cieplne, które pokazują, które rejony mózgu wpłynęły na daną decyzję. W wczesnych stadiach te mapy podkreślają obszary związane z pamięcią, które wiadomo, że ulegają pierwszemu pogorszeniu w chorobie Alzheimera; w późniejszych stadiach rozszerzają się na szerzej położone rejony korowe, co zgadza się z klinicznym rozumieniem postępu choroby.
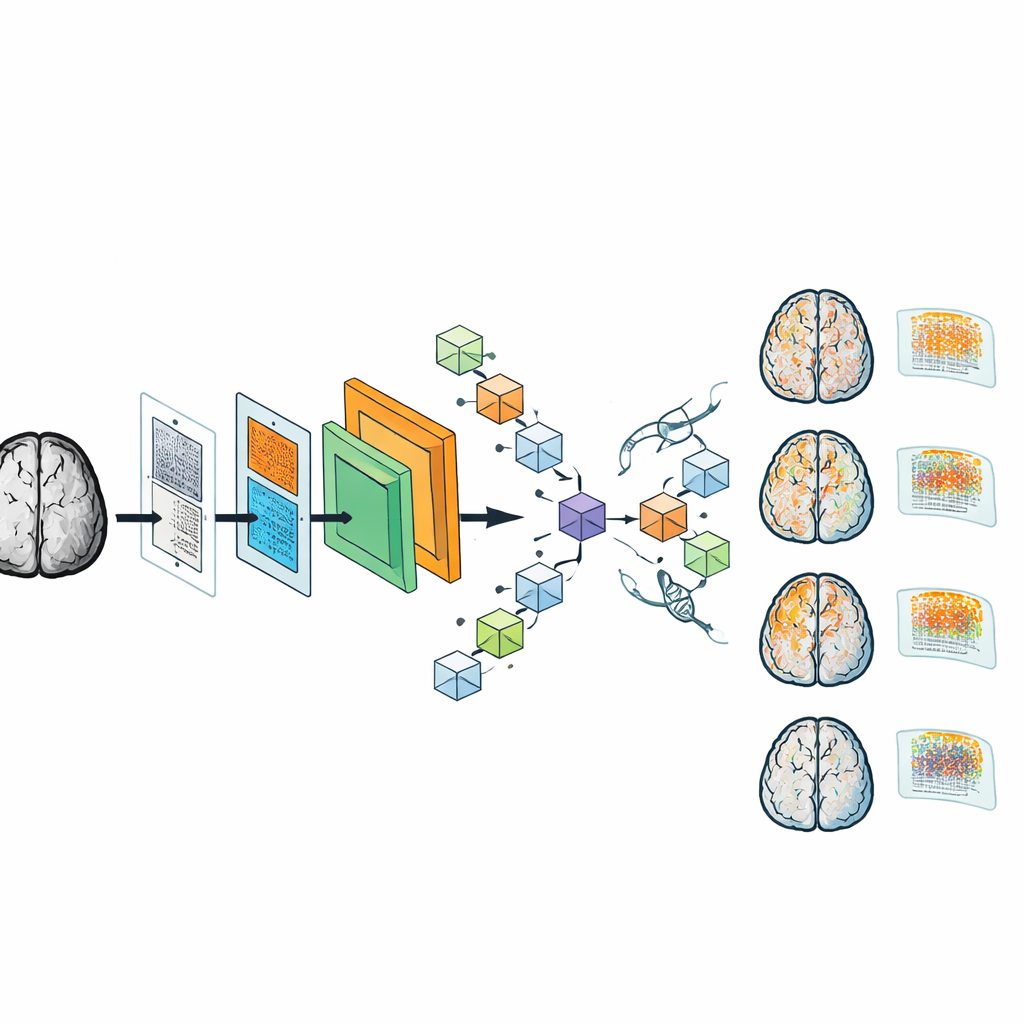
Co to oznacza dla pacjentów i placówek
Dla osób niebędących specjalistami główne przesłanie jest takie, że badanie oferuje szybkie, kompaktowe i interpretable narzędzie do oceny nasilenia demencji na podstawie rutynowych skanów MRI. Poprzez zbalansowanie danych treningowych i staranne kształtowanie sieci za pomocą optymalizacji bezpochodnej, autorzy stworzyli model, który może działać na skromnym sprzęcie, jednocześnie dostarczając niemal doskonałej dokładności i wskazując rejony mózgu będące podstawą swoich decyzji. Jeśli potwierdzą to przyszłe prospektywne badania kliniczne, taka technologia mogłaby wspierać wcześniejszą diagnozę, bardziej spójną klasyfikację stadiów między szpitalami oraz lepsze śledzenie, jak choroba Alzheimera zmienia mózg w czasie.
Cytowanie: Ganesan, S.K., Velusamy, P., Parthsarathy, P. et al. Alzheimer’s related dementia severity classification from magnetic resonance imaging using derivative-free optimization of convolutional neural network. Sci Rep 16, 10077 (2026). https://doi.org/10.1038/s41598-026-36037-9
Słowa kluczowe: choroba Alzheimera, MR mózgu, stadia demencji, uczenie głębokie, Sztuczna inteligencja w obrazowaniu medycznym