Clear Sky Science · pl
SULT1E1 odgrywa rolę ochronną w POChP poprzez hamowanie szlaku AKT: badanie in vivo i in vitro
Dlaczego enzym płucny ma znaczenie dla codziennego oddychania
Przewlekła obturacyjna choroba płuc (POChP) jest jedną z głównych przyczyn zgonów na świecie, a lekarze wciąż nie dysponują narzędziami do wczesnego zatrzymania choroby ani odwrócenia jej szkód. To badanie rzuca światło na nieoczekiwanego uczestnika POChP: niewielki enzym o nazwie SULT1E1, który pomaga przetwarzać hormony i związki chemiczne w organizmie. Śledząc ten enzym od analiz dużych zbiorów danych, przez próbki krwi pacjentów, płuca zwierząt, aż po hodowane komórki, badacze odkrywają dowody, że SULT1E1 działa jak wbudowana tarcza dla dróg oddechowych — a jego utrata może sprzyjać postępowi POChP.
Nowe spojrzenie na znaną chorobę płuc
POChP to nie pojedyncza jednostka chorobowa, lecz zespół przewlekłych problemów płucnych, w tym przewlekłego zapalenia oskrzeli i rozedmy, zazwyczaj wywołanych długotrwałym narażeniem na dym lub zanieczyszczone powietrze. Z czasem drogi oddechowe ulegają zapaleniu, bliznowaceniu i zatykaniu śluzem, powodując duszność nawet przy niewielkim wysiłku. Obecne terapie głównie łagodzą objawy; niewiele robią, aby zatrzymać powolne, nieodwracalne uszkodzenia tkanki płucnej. Dlatego naukowcy poszukują nowych molekularnych wskazówek — białek lub szlaków, które nie tylko odzwierciedlają nasilenie choroby, lecz mogłyby też być celem działań chroniących lub naprawczych dla płuc.
Śledzenie enzymu w zbiorach danych i u pacjentów
Zespół badawczy rozpoczął od przeszukania czterech dużych publicznych zestawów danych dotyczących ekspresji genów w ludzkiej tkance płucnej, porównując próbki osób z POChP z próbami od osób zdrowych. Spośród setek genów, które się różniły, SULT1E1 wyróżniał się wyraźnym obniżeniem w płucach chorych na POChP. Enzym ten zwykle pomaga dezaktywować estrogen i inne hormony oraz bierze udział w bezpiecznym przetwarzaniu leków i związków obcych. Analizy sieciowe i ścieżek wykazały, że SULT1E1 jest powiązany z wieloma białkami związanymi z metabolizmem i hormonami, sugerując, że zmiany jego poziomu mogą wywoływać efekty kaskadowe w wielu systemach istotnych dla zdrowia płuc.
Aby sprawdzić, czy ten wzorzec występuje także poza ekranami komputerów, zespół zmierzył poziom SULT1E1 u rzeczywistych pacjentów. W próbkach krwi od 92 osób z POChP i 40 zdrowych ochotników zarówno poziom białka w surowicy, jak i aktywność genu w komórkach układu odpornościowego były istotnie niższe w grupie POChP. Co istotne, osoby z najniższym SULT1E1 miały skłonność do najgorszej czynności płuc, mierzonej standardowymi testami oddechowymi (FEV1% i stosunek FEV1/FVC). To silne powiązanie sugeruje, że SULT1E1 mógłby służyć jako prosty marker krwiowy wskazujący stopień zaawansowania POChP.
Dowody z płuc zwierząt i komórek hodowanych w laboratorium
Historia nie zatrzymała się na badaniach krwi. W modelu szczurzym narażonym na czynniki drażniące naśladujące POChP u ludzi, zwierzęta rozwinęły klasyczne uszkodzenia płuc widoczne w mikroskopie, a ich tkanka płucna również wykazała wyraźny spadek białka SULT1E1. Aby zrozumieć, co ten enzym robi w komórkach dróg oddechowych, naukowcy wykorzystali ludzką linię komórek oskrzelowych hodowaną w naczyniach. Gdy obniżyli poziom SULT1E1, komórki mnożyły się szybciej, wykazywały oporność na zaprogramowaną śmierć komórkową i zaczęły przyjmować cechy związane z bliznowaceniem i usztywnianiem tkanki — procesem zwanym transformacją nabłonkowo-mezenchymalną (EMT). Gdy zwiększono SULT1E1, wszystkie te zmiany uległy odwróceniu: wzrost spowolnił, apoptoza wróciła w kierunku normy, a markery EMT zmalały.
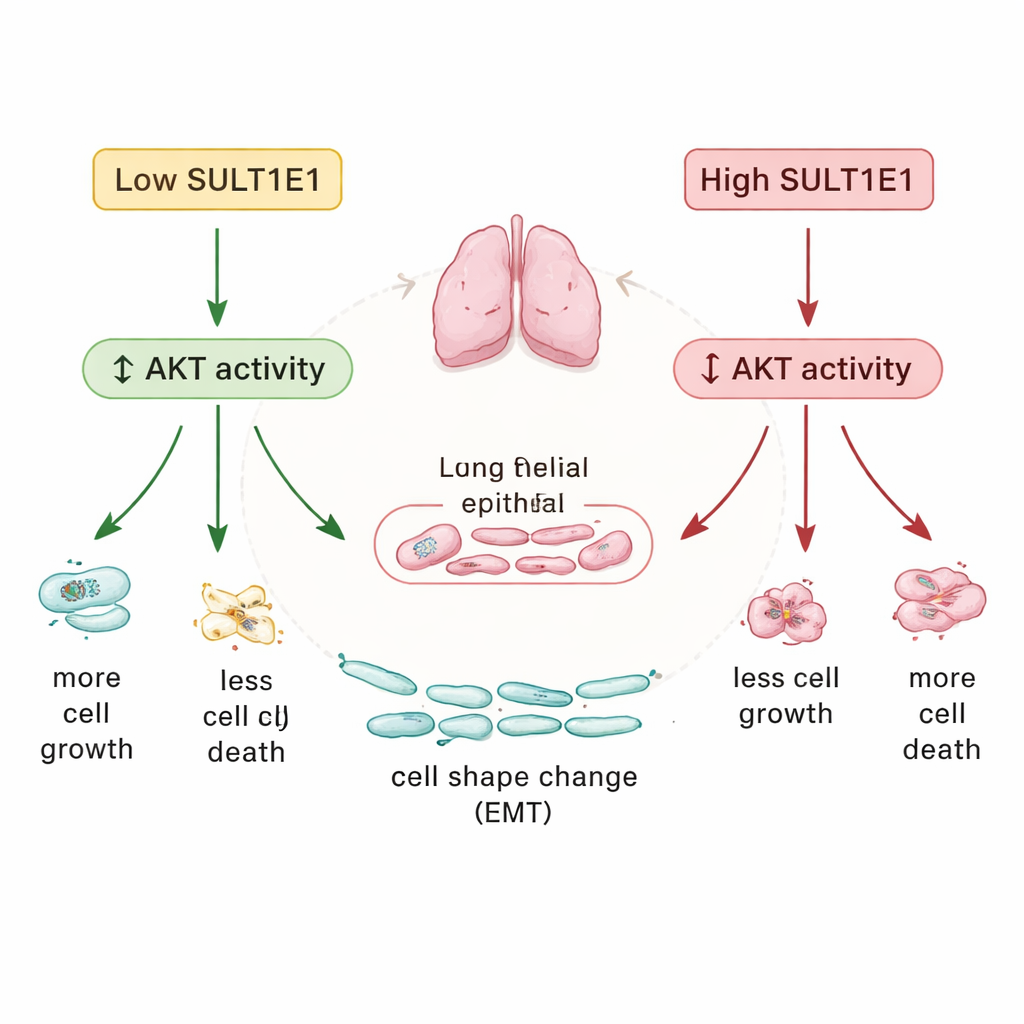
Przełącznik sygnałowy łączący wszystkie elementy
Idąc dalej, zespół powiązał te efekty z centralnym wewnątrzkomórkowym szlakiem sygnałowym znanym jako ścieżka AKT, która kontroluje wzrost, przeżycie i reakcje na stres. W komórkach płucnych pozbawionych SULT1E1 AKT był silniej aktywowany; przy nadmiarze SULT1E1 aktywność AKT malała. Innymi słowy, SULT1E1 wydaje się działać jako naturalny hamulec sygnalizacji AKT. Gdy ten hamulec zawodzi w POChP, skutkiem jest przesunięcie w stronę nadmiernego wzrostu komórek, zmniejszonej odnowy komórkowej i zmian strukturalnych wyściełających drogi oddechowe — wszystkie cechy charakterystyczne choroby. Badacze spekulują, że może to częściowo wynikać ze zmienionego metabolizmu estrogenu, który sam może pobudzać aktywację AKT, choć możliwe są też inne, niehormonalne role SULT1E1.
Co to może oznaczać dla osób z POChP
W sumie wyniki przedstawiają SULT1E1 jako cichego strażnika płuc: gdy występuje na zdrowych poziomach, utrzymuje kluczowe sygnały wzrostu i przeżycia pod kontrolą, pomagając zachować stabilną wyściółkę dróg oddechowych. W POChP ten strażnik jest utracony lub osłabiony, a ścieżka AKT działa zbyt intensywnie, sprzyjając nadmiernemu wzrostowi i bliznowaceniu komórek oskrzeli. Dla pacjentów praca ta otwiera dwie główne perspektywy. Po pierwsze, SULT1E1 w krwi mógłby stać się wygodnym markerem do oceny zaawansowania choroby lub monitorowania odpowiedzi na leczenie. Po drugie, leki zwiększające aktywność SULT1E1 — lub naśladujące jego łagodzący wpływ na AKT — mogłyby pewnego dnia utworzyć nową klasę terapii ukierunkowanych nie tylko na łagodzenie objawów, lecz na spowolnienie podstawowych uszkodzeń utrudniających oddychanie.
Cytowanie: Song, W., Zhang, W., Wang, F. et al. SULT1E1 exerts a protective role in COPD by inhibiting the AKT pathway: an in vivo and in vitro study. Sci Rep 16, 6238 (2026). https://doi.org/10.1038/s41598-026-35997-2
Słowa kluczowe: POChP, SULT1E1, zapalenie płuc, sygnalizacja AKT, biomarker