Clear Sky Science · pl
Wpływ zatłoczenia molekularnego na stabilność białek w proteomie bakteryjnym
Dlaczego zatłoczone życie białek ma znaczenie
W każdej żywej komórce białka wykonują swoje funkcje w przestrzeni tak wypełnionej innymi cząsteczkami, że niemal połowa objętości może być zajęta. Tymczasem większość doświadczeń laboratoryjnych bada białka w rozcieńczonych, prawie pustych roztworach. Artykuł stawia proste, lecz istotne pytanie: jak ta zatłoczona rzeczywistość zmienia stabilność i zachowanie białek oraz co to znaczy dla funkcjonowania życia na poziomie molekularnym?
Zaglądanie do zatłoczonego świata komórkowego
Aby to zbadać, badacze pracowali z bakterią Cupriavidus necator, mikroorganizmem interesującym z punktu widzenia technologii ekologicznych, takich jak wychwytywanie dwutlenku węgla czy produkcja bioplastików. Delikatnie otworzyli komórki, zachowując setki różnych białek w stanie możliwie zbliżonym do naturalnego. Następnie dodali wysokie stężenia dużych, hydrofilowych polimerów — powszechnych „czynników zatłoczenia” takich jak PEG, dekstran i Ficoll — które często stosuje się do naśladowania gęstego wnętrza komórek.
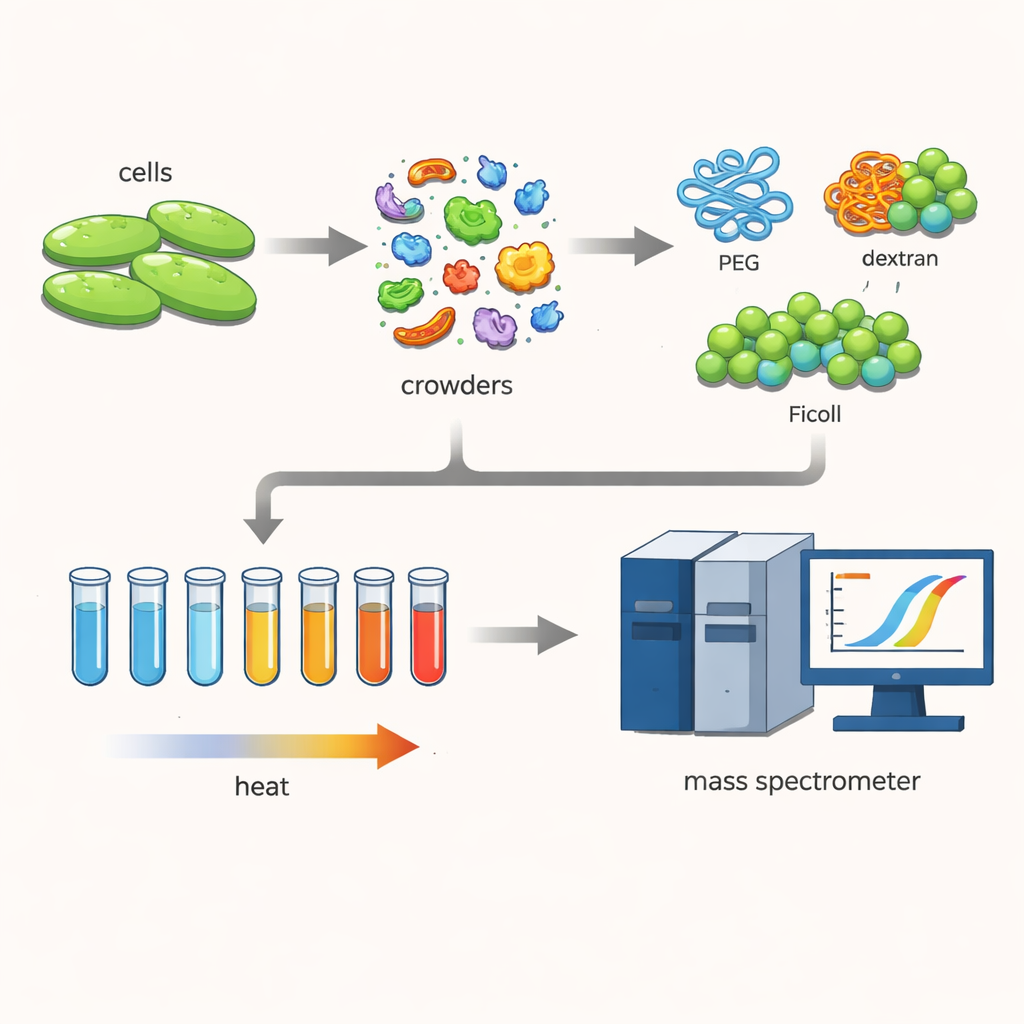
Obserwowanie topnienia białek
Zespół zastosował technikę znaną jako termiczne profilowanie proteomu. Podgrzewali wiele małych próbek mieszaniny białek stopniowo od 30 do 70 stopni Celsjusza. Wraz ze wzrostem temperatury mniej stabilne białka rozwijały się i tworzyły agregaty, wypadając z roztworu. Oznaczając pozostałe rozpuszczalne białka i mierząc je za pomocą czułego spektrometru mas, naukowcy mogli odtworzyć krzywe topnienia dla każdego białka i określić jego temperaturę topnienia — punkt, w którym połowa białka przestaje być w stanie rozpuszczalnym i funkcjonalnym. Porównanie tych temperatur z i bez czynników zatłoczenia ujawniło, jak środowisko zatłoczenia przesuwa stabilność białek.
Mieszany obraz: niektóre białka bardziej stabilne, inne bardziej kruche
Średnio dodanie dowolnego z sześciu polimerów‑czynnika zatłoczenia obniżało temperatury topnienia w całym proteomie bakteryjnym, sugerując niewielki ogólny efekt destabilizujący. Jednak ten globalny trend skrywał znacznie bardziej zniuansowaną historię. Dla dziesiątek pojedynczych białek czynniki zatłoczenia wyraźnie albo podnosiły, albo obniżały stabilność, czasem o kilka stopni. Większość białek reagowała tylko na jeden z sześciu reagentów, ale garstka reagowała na kilka i niemal wszystkie z nich były konsekwentnie albo stabilizowane, albo destabilizowane, co sugeruje wspólne cechy warunkujące ich interakcje z czynnikami zatłoczenia.
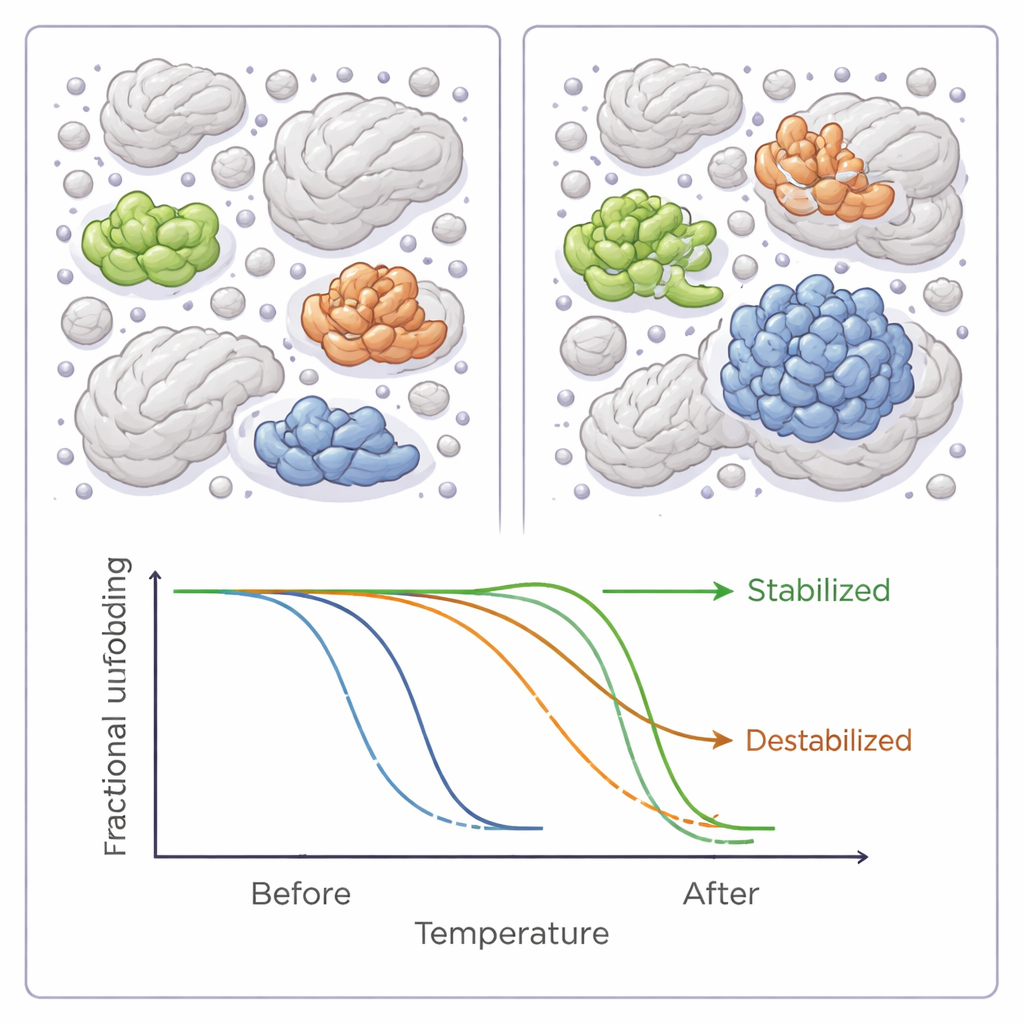
Co sprawia, że białko zyskuje lub traci w tłumie
Gdy autorzy przyjrzeli się bliżej właściwościom tych wrażliwych białek, wyłoniły się wzorce. Białka, które stawały się bardziej stabilne w warunkach zatłoczenia, miały tendencję do bycia bardziej hydrofobowymi — czyli posiadały więcej powierzchni odpychających wodę — i częściej były klasycznymi enzymami z dobrze zdefiniowanymi centrami aktywnymi. Częściej uczestniczyły też w interakcjach białko‑białko lub niosły modyfikacje chemiczne regulujące ich funkcję. Destabilizowane białka z kolei były przeciętnie mniejsze i mniej „ozdobione” takimi modyfikacjami. Te obserwacje pokrywają się z modelami komputerowymi i innymi eksperymentami sugerującymi, że zatłoczenie może sprzyjać niektórym białkom, a czynić inne bardziej podatnymi, w zależności od rozmiaru, kształtu i sposobu, w jaki zwykle wchodzą w interakcje z partnerami.
Ponad proste ściskanie: jak naprawdę działają czynniki zatłoczenia
Tradycyjne wyjaśnienia efektów zatłoczenia molekularnego koncentrują się na „wykluczonej objętości”, czyli idei, że duże cząsteczki po prostu zostawiają mniej miejsca, co skłania białka do utrzymywania struktury złożonej. Gdyby to było całe wyjaśnienie, spodziewalibyśmy się, że czynniki zatłoczenia głównie stabilizują białka i że silne zależności wystąpią w odniesieniu do objętości czy lepkości polimerów. Zamiast tego autorzy zaobserwowali tylko słabe korelacje z rozmiarem i „grubością” polimerów. Dane lepiej pasowały do obrazu „preferencyjnego wykluczenia”: crowdery i białka unikają się chemicznie, co pośrednio faworyzuje niektóre stany złożone, ale może też zaburzać delikatne interakcje utrzymujące stabilność innych białek. Krótko mówiąc, to nie tylko fizyczne ściskanie, lecz subtelne chemiczne popychanie i przyciąganie kształtuje zachowanie białek.
Co to oznacza dla zrozumienia chemii życia
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że białek wewnątrz komórek nie da się w pełni zrozumieć w izolacji, pływających w czystym buforze. Gęsta molekularna dżungla wokół nich może uczynić niektóre białka bardziej odpornymi, a inne bardziej wrażliwymi, zmieniając działanie całych sieci reakcji. Badanie to, mierząc jednocześnie zmiany stabilności setek białek, pokazuje, że efekty zatłoczenia są złożone i specyficzne dla poszczególnych białek, i prawdopodobnie wynikają z bezpośrednich interakcji równie mocno, co z prostego pakowania. Gdy naukowcy projektują leki, enzymy przemysłowe czy zmodyfikowane mikroby, uwzględnienie tej zatłoczonej rzeczywistości będzie kluczowe dla przewidywania, jak białka będą rzeczywiście się zachowywać w żywych układach.
Cytowanie: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Słowa kluczowe: zatłoczenie molekularne, stabilność białek, termiczne profilowanie proteomu, proteom bakteryjny, środowisko komórkowe