Clear Sky Science · pl
Niedobór Negr1 zmienia sygnalizację glutaminergiczną i szlak kinureninowy w modelu myszy zaburzeń psychicznych
Dlaczego to badanie mózgu ma znaczenie
Wiele powszechnych chorób psychicznych, od depresji po schizofrenię, jest powiązanych z subtelnymi zmianami w sposobie, w jaki komórki mózgu komunikują się ze sobą. To badanie analizuje jeden gen ryzyka, nazwany NEGR1, u myszy, aby sprawdzić, jak jego brak zmienia chemię mózgu i zachowanie. Śledząc, jak myszy poruszają się po podaniu leku, który na krótko zaburza kluczowy receptor mózgowy, oraz mierząc powiązane związki chemiczne w mózgu, badacze odkrywają, jak genetyka, płeć i metabolizm mózgu mogą łączyć się, tworząc podatność na zaburzenia psychiczne.
Gen, który utrzymuje równowagę sygnałów mózgowych
Gen NEGR1 koduje białko powierzchni komórkowej, które pomaga neuronom tworzyć i stabilizować połączenia. Wcześniejsze badania wykazały, że usunięcie tego genu u myszy zmienia strukturę mózgu, zmniejsza niektóre hamujące połączenia (GABA) i zmienia odpowiedzi na leki powiązane z dopaminą, takie jak amfetamina. Ponieważ te zmiany wskazują na przesunięcie w kierunku silniejszych sygnałów pobudzających, zespół skupił się na innym głównym układzie pobudzającym: glutaminie i jej receptorach NMDA, które są kluczowe dla uczenia się, pamięci i elastycznego zachowania. Zbadano też „szlak kinureninowy”, metaboliczną drogę rozkładu aminokwasu tryptofanu na związki, które mogą wzmacniać lub blokować receptory NMDA.
Badanie zachowania za pomocą leku zmieniającego świadomość
Aby zbadać funkcję receptorów NMDA, badacze użyli MK-801, znanego leku, który krótko blokuje te receptory i może naśladować aspekty zaburzeń równowagi glutaminergicznej obserwowane w chorobach psychicznych. Samce i samice myszy miały albo normalny gen Negr1, albo brak tego genu. Zwierzęta otrzymywały codzienne zastrzyki MK-801 i były testowane w arenie otwartej, gdzie automatycznie rejestrowano ich całkowitą aktywność, czas spędzony w narożnikach oraz wirowania przypominające obroty. U samców niepodawanych wcześniej leku pojedyncza dawka MK-801 wywołała silniejszy wybuch aktywności u myszy pozbawionych Negr1 niż u myszy normalnych, co sugeruje, że ich mózgi były nadwrażliwe na to zaburzenie sygnalizacji glutaminergicznej.
Zaskakujący wzór szybkiej tolerancji
Przy powtarzanym podawaniu MK-801 wzorzec się zmienił. U samców aktywność skakała w niektóre dni, ale spadała co drugi dzień, tworząc zygzakowaty przebieg sugerujący szybką, częściową tolerancję na efekty leku. W ciągu dziewięciu dni myszy normalne samców wykazywały narastającą odpowiedź zgodną z sensytyzacją, podczas gdy samce pozbawione Negr1 wykazywały stłumione narastanie aktywności i łagodniejsze zmiany dzień po dniu, co wskazuje na zmienioną czułość receptorów NMDA. Samice obu genotypów adaptowały się jeszcze szybciej: około piątego dnia MK-801 przestał wywoływać silne efekty behawioralne, więc przerwano leczenie. We wszystkich miarach płeć miała istotny wpływ, a wyraźne efekty genotypu pojawiły się głównie u samców.
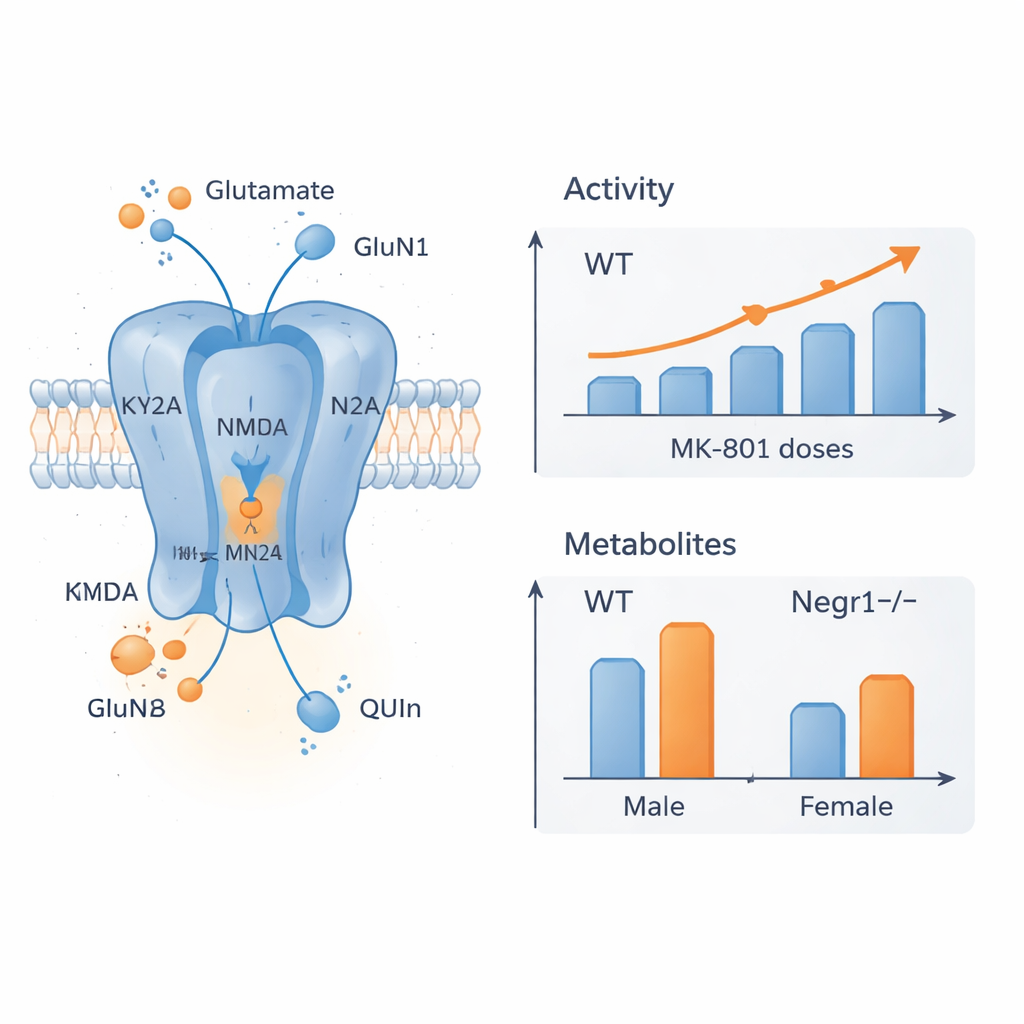
Przemiany receptorów i związków mózgowych
Aby odkryć, co stało za tymi różnicami behawioralnymi, zespół zmierzył aktywność genów dla kluczowych podjednostek receptorów NMDA oraz enzymu produkującego D-serynę, ko-sygnalizator tych receptorów. Skupiono się na obszarach mózgu kluczowych dla nastroju i poznania: korze przedczołowej i hipokampie. W korze przedczołowej samice pozbawione Negr1 leczone MK-801 wykazywały obniżoną ekspresję podstawowych podjednostek receptorowych, co sugeruje, że ich mózgi dostosowują skład receptorów w odpowiedzi zarówno na mutację, jak i lek. W hipokampie samców myszy pozbawione Negr1 miały wyższą podstawową ekspresję niektórych podjednostek NMDA, zgodnie z wcześniejszymi dowodami na większą dostępną liczbę receptorów; leczenie MK-801 obniżało wtedy te poziomy w kierunku normy. Równolegle szczegółowe analizy chemiczne krwi i wielu regionów mózgu wykazały, że kilka metabolitów szlaku kinureninowego oraz sama glutamina były zmienione w sposób zależny od płci i regionu mózgu, z największymi zmianami w korze przedczołowej, a niektóre zjawiska nasilały się z wiekiem.
Co to oznacza dla zrozumienia chorób psychicznych
W sumie wyniki te przedstawiają NEGR1 jako molekularnego organizatora, który pomaga utrzymać równowagę między sygnałami pobudzającymi i hamującymi w mózgu, częściowo poprzez kształtowanie funkcji receptorów NMDA i metabolizmu tryptofanu. Gdy brak Negr1, myszy reagują inaczej na blokadę receptorów NMDA, wykazują zależne od płci przesunięcia w związkach mózgowych oraz stopniowo rozwijają tolerancję w nietypowy sposób. Dla czytelnika nieprofesjonalnego kluczowe przesłanie jest takie, że pojedynczy gen ryzyka nie działa w izolacji: jego efekty zależą od płci, regionu mózgu i stanu metabolicznego. Praca ta wzmacnia pogląd, że ukierunkowanie ścieżek powiązanych z NEGR1 — zamiast jedynie pojedynczych receptorów — może ostatecznie pomóc dostosować leczenie zaburzeń psychicznych związanych z zaburzeniami równowagi glutaminergicznej.
Cytowanie: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
Słowa kluczowe: gen NEGR1, receptor NMDA, sygnalizacja glutaminergiczna, szlak kinureninowy, zaburzenia psychiczne