Clear Sky Science · pl
Hamowanie autofagii wzmacnia właściwości przeciwnowotworowe sulforafanu
Dlaczego związki z brokułów i stara tabletka przeciwmalaryczna mają znaczenie
Rak pęcherza jest powszechny i często śmiertelny po rozsiewie; wielu pacjentów w końcu przestaje odpowiadać na leczenie. Badanie opisuje niespodziewane połączenie: sulforafan, naturalny związek z brokułów, oraz chlorochina, długo stosowany lek przeciwmalaryczny. Wspólnie zakłócają wewnętrzny system recyklingu i zdolność poruszania się komórek nowotworowych w sposób, który mógłby w przyszłości pomóc uczynić terapie raka pęcherza bardziej skutecznymi i trwalszymi.
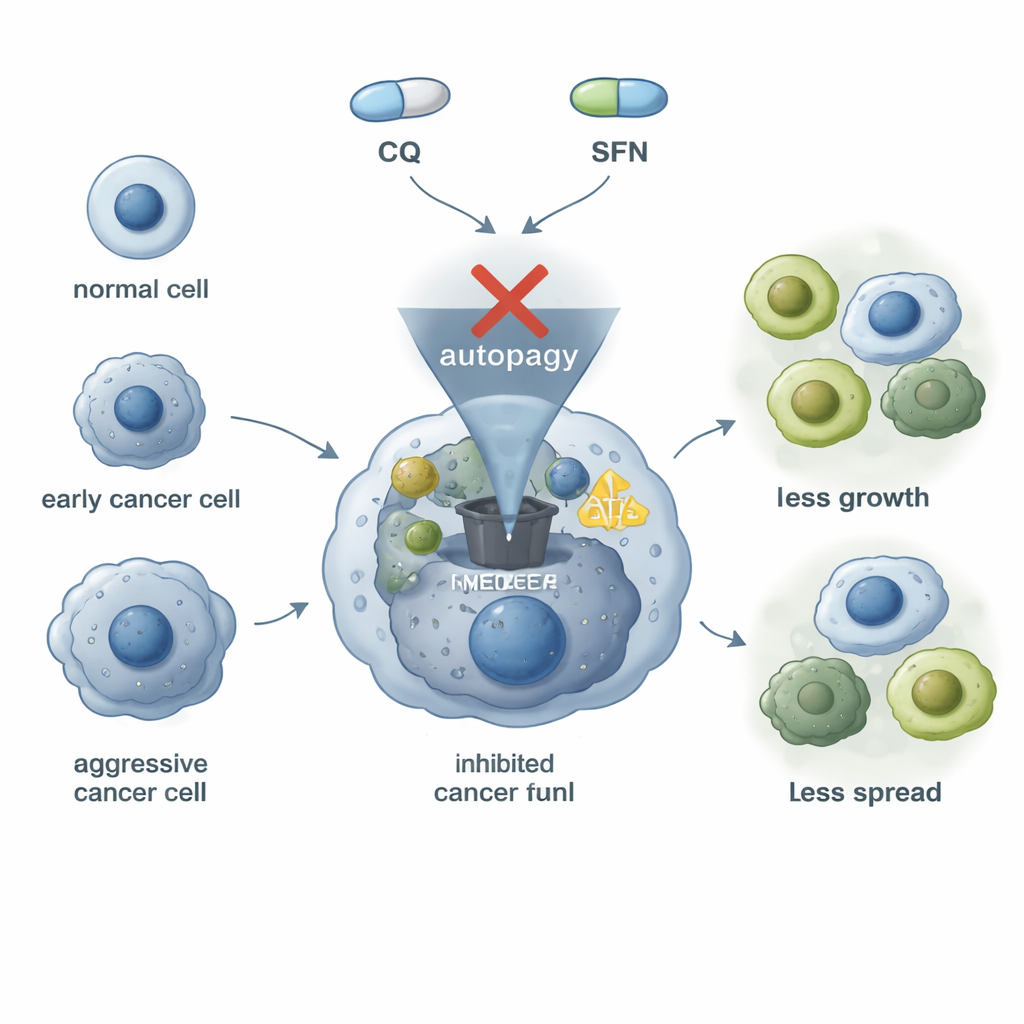
Wyzwanie uporczywych guzów pęcherza
Rak pęcherza nie jest jednorodną chorobą; guzy różnią się pod względem mutacji, złośliwości i odpowiedzi na terapię. Wiele komórek raka pęcherza polega na wysokim poziomie „samoczyszczenia”, czyli procesie zwanym autofagią, aby przetrwać stres, naprawiać uszkodzenia i opierać się lekom. Te same komórki często wykazują wysokie ilości białka powierzchniowego nazwanego ICAM-1 oraz innego białka, N-kadheryny, oba związane ze zwiększoną mobilnością i inwazyjnością, co ułatwia rozsiewanie nowotworu. Ponieważ standardowe terapie nie eliminują w pełni tych mechanizmów przetrwania, badacze poszukują sposobów na jednoczesne zablokowanie zarówno maszynerii recyklingowej, jak i zachowań inwazyjnych.
Przekierowanie chlorochiny i wykorzystanie obrony brokułów
Chlorochina, najbardziej znana jako lek przeciwmalaryczny, może blokować ostatni etap autofagii: moment, gdy wakuole z odpadami łączą się z kwaśnymi przedziałami komórkowymi, które rozkładają materiały na użyteczną energię. Sama w sobie chlorochina spowalniała wzrost i migrację trzech różnych linii komórek raka pęcherza w warunkach laboratoryjnych, wykazując podstawowy efekt przeciwnowotworowy. Jednak nieoczekiwanie podnosiła też poziomy ICAM-1 we wszystkich tych komórkach, co jest niepokojącym sygnałem, ponieważ wyższe ICAM-1 wiąże się z bardziej agresywnym zachowaniem. Sulforafan, związek naturalnie występujący w warzywach krzyżowych, takich jak brokuły, opisano jako spowalniający wzrost wielu rodzajów nowotworów i, co ważne, obniżający poziomy ICAM-1. To uczyniło go atrakcyjnym partnerem dla chlorochiny: jeden lek blokuje system recyklingu, drugi tłumi kluczowy marker złośliwości.
Jak duet leków osłabia komórki nowotworowe
Naukowcy potraktowali trzy linie komórek raka pęcherza chlorochiną, sulforafanem lub oboma środkami i śledzili sieć białek sygnalizacyjnych kontrolujących wzrost, ruch i autofagię. Chlorochina konsekwentnie blokowała autofagię, powodując nagromadzenie standardowych markerów recyklingu wewnątrz komórek. Dodanie sulforafanu wzmocniło kilka pożądanych efektów chlorochiny: obniżyło poziomy ICAM-1 i N-kadheryny w dwóch z trzech linii, skierowało beta-kateninę (białko związane ze wzrostem) ku degradacji oraz zmieniło kluczowe przełączniki (takie jak AKT, GSK-3β, mTOR i ULK) w sposób generalnie zniechęcający do przeżycia i samoczyszczenia. Jednocześnie łączone leczenie uszkadzało mitochondria — elektrownie komórkowe — i, w zależności od linii komórkowej, zmieniało równowagę reaktywnych form tlenu, małych cząsteczek, które mogą przesunąć komórkę w kierunku samozniszczenia.
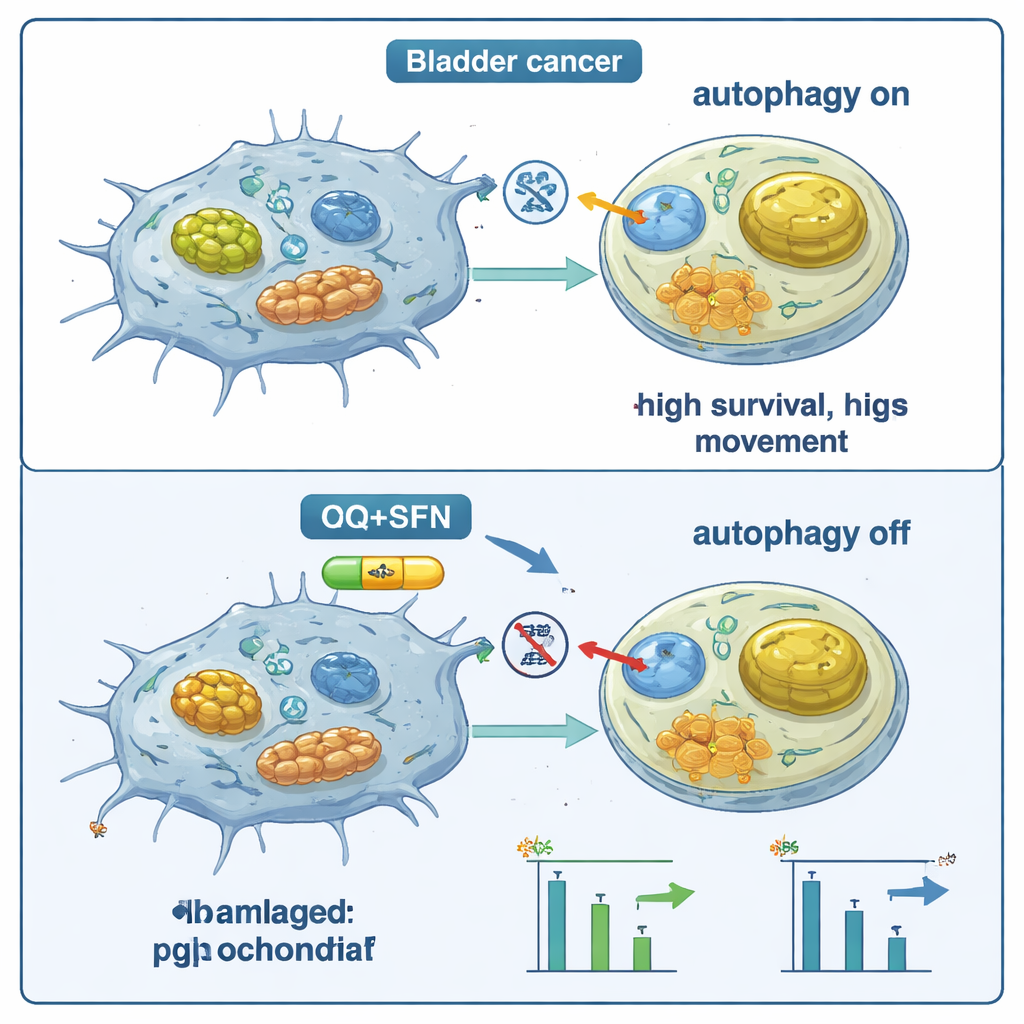
Wolniejszy wzrost i mniejsza ruchliwość zależą od typu komórek
Poza tymi zmianami molekularnymi zespół postawił dwa praktyczne pytania: czy komórki dzielą się mniej i czy poruszają się mniej? We wszystkich trzech badanych liniach komórek raka pęcherza kombinacja sulforafanu i chlorochiny ograniczyła proliferację komórek, ze szczególnie silnym efektem w jednej linii, która już miała wysoki poziom ICAM-1. Test „zarysowania” (scratch assay) pokazał, że leczone komórki wolniej wędrowały i zamykały lukę, co wskazuje na zmniejszony potencjał migracyjny, ponownie z najsilniejszymi efektami przy użyciu obu środków jednocześnie. Jednak nie wszystkie linie komórkowe reagowały tak samo. W jednej linii z relatywnie niskim ICAM-1 blokada autofagii czasami wydawała się chronić agresywny wzorzec nowotworu, podkreślając, że wynik zależy silnie od molekularnego „okablowania” każdego guza.
Co to może znaczyć dla przyszłych terapii
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie, że komórki nowotworowe wykorzystują wewnętrzny program recyklingu i określone białka powierzchniowe, aby przetrwać, dzielić się i rozsiewać się, i że te cechy można zaatakować z więcej niż jednego kierunku. W tym badaniu sulforafan pomógł przeciwdziałać niepożądanemu efektowi chlorochiny — jej skłonności do zwiększania markera sprzyjającego nowotworowi — jednocześnie wzmacniając ogólny wpływ przeciwnowotworowy na komórki pęcherza hodowane w laboratorium. Wyniki nie przekładają się jeszcze bezpośrednio na terapię gotową do stosowania w klinice i podkreślają, że niektóre guzy mogą wręcz skorzystać na blokadzie autofagii, w zależności od ich profilu. Mimo to praca wspiera pomysł, że starannie dobrane kombinacje powszechnego leku i naturalnego związku dietetycznego mogłyby być dopasowane do typu guza, aby spowolnić wzrost raka pęcherza, ograniczyć jego rozsiew i poprawić odpowiedź na istniejące terapie.
Cytowanie: Zarzycka, M., Kotula-Balak, M. & Gil, D. Inhibiting autophagy enhances anti-cancer properties of sulforaphane. Sci Rep 16, 5296 (2026). https://doi.org/10.1038/s41598-026-35891-x
Słowa kluczowe: rak pęcherza, autofagia, sulforafan, chlorochina, ICAM-1