Clear Sky Science · pl
Obniżona ekspresja BIRC2 i BIRC3 związana z dłuższym przeżyciem w pediatrycznych glejakach wysokiego stopnia
Dlaczego nowa wiedza jest potrzebna przy dziecięcych guzach mózgu
Pediatryczne glejaki wysokiego stopnia należą do najbardziej śmiertelnych nowotworów mózgu u dzieci, a obecne metody — operacja, radioterapia i chemioterapia — pomagają tylko niewielkiej części pacjentów. W tym badaniu zadano proste, lecz kluczowe pytanie: czy w tych guzach istnieją molekularne „przełączniki przeżycia”, które umożliwiają komórkom nowotworowym opieranie się śmierci, i czy te przełączniki mogą wyjaśniać, dlaczego niektóre dzieci żyją dłużej niż inne?
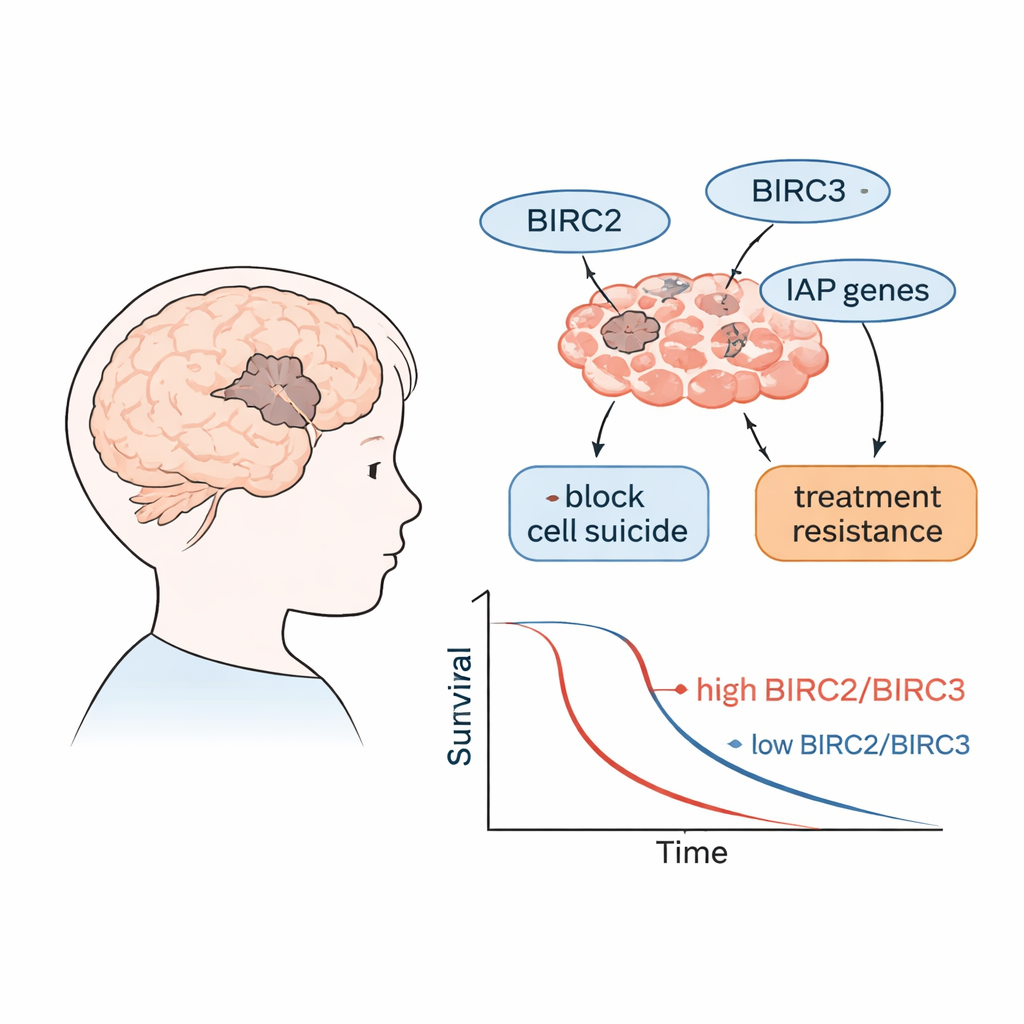
Białka, które nie pozwalają komórkom nowotworowym umrzeć
Komórki mają wbudowany mechanizm samozniszczenia, zwany często programowaną śmiercią komórki lub apoptozą, który usuwa uszkodzone lub niebezpieczne komórki. Rodzina białek określana jako IAP (inhibitory białek apoptozy) może blokować ten mechanizm. Geny kodujące te białka noszą nazwę BIRC. W wielu nowotworach IAP są nadmiernie aktywne, co pozwala komórkom guza ignorować sygnały śmierci i nadal rosnąć. Badacze skupili się na kilku członkach tej rodziny, w tym BIRC2 i BIRC3, a także na pokrewnych genach, które promują lub przeciwdziałają śmierci komórki, aby ocenić ich aktywność w agresywnych nowotworach mózgu u dzieci.
Badanie rzeczywistych guzów od młodych pacjentów
Zespół przeanalizował próbki guzów od 26 młodych osób, wszystkie leczone w ośrodku neuroonkologicznym dla dzieci i wszystkie z rozpoznaniem najbardziej agresywnej postaci glejaka. Na podstawie zachowanych tkanek pobranych podczas operacji zmierzono aktywność wielu genów związanych z przeżyciem i apoptozą komórek, takich jak BIRC2, BIRC3, BIRC5, BIRC6, BIRC7, NAIP, XIAP, DIABLO, XAF1, CASP3 i CASP9. Porównano także te molekularne pomiary z cechami klinicznymi: czasem przeżycia poszczególnych pacjentów, okresem stabilności choroby przed nawrotem oraz obecnością powszechnych markerów nowotworowych, jak Ki‑67 (wskaźnik proliferacji), PD‑1 (punkt kontrolny immunologiczny), Olig2, p53, GFAP i niewielkiego regulatorowego RNA o nazwie miR‑155‑5p.
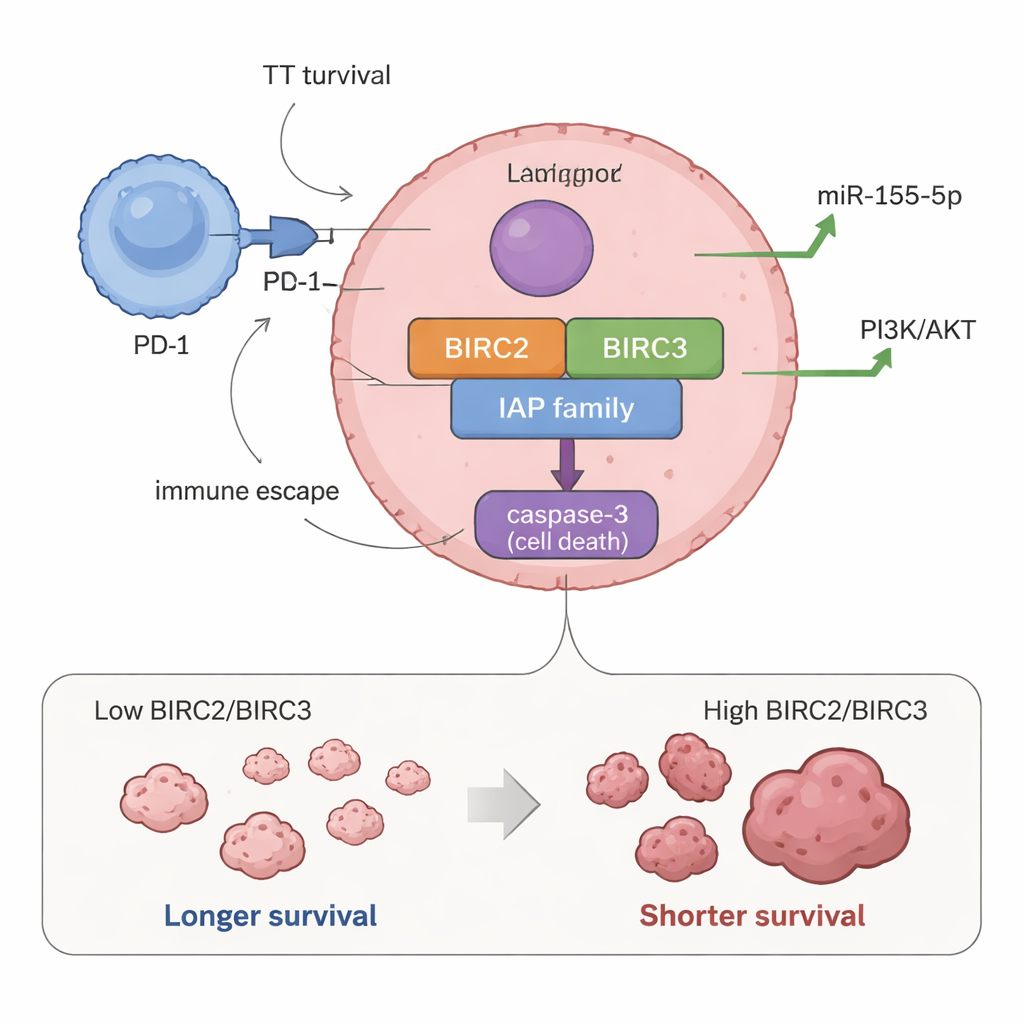
Przełączniki przeżycia powiązane z krótszym czasem życia
Porównując aktywność genów z wynikami pacjentów, wyłoniły się dwa geny. Dzieci, u których guzy wykazywały wyższe poziomy BIRC2 i BIRC3, miały tendencję do krótszego całkowitego przeżycia oraz krótszych okresów bez progresji choroby. Innymi słowy, gdy te „nie‑umieraj” przełączniki były silniej włączone, choroba przebiegała bardziej agresywnie. Guzy o wysokiej ekspresji BIRC2 i BIRC3 wiązały się również z wyższymi poziomami miR‑155‑5p, małego RNA wcześniej wykazanego jako sprzyjającego wzrostowi i hamującego apoptozę, co sugeruje, że te cząsteczki mogą współdziałać, wzmacniając odporność guzów na leczenie.
Powiązania z wzrostem guza i unikaniem układu odpornościowego
Badanie sprawdziło też, jak te przełączniki przeżycia wpisują się w szersze środowisko guza. Co zaskakujące, niektóre geny, które mogą sprzyjać lub regulować śmierć komórek, takie jak NAIP, BIRC3 i XAF1, były bardziej aktywne w guzach pozbawionych markera proliferacji Ki‑67, co sugeruje złożoną równowagę między sygnałami wzrostu a śmierci. Wyższe poziomy BIRC3 i XAF1 częściej występowały w guzach z większą ekspresją PD‑1, kluczowego immunologicznego „hamulca”, który pomaga nowotworowi ukrywać się przed obroną organizmu. Ponadto wyższa aktywność CASP3, centralnego enzymu wykonawczego apoptozy, była silnie związana z ekspresją PD‑1, co sugeruje, że interakcje między komórkami nowotworowymi a komórkami układu odpornościowego mogą zmieniać sposób, w jaki mechanizm śmierci jest używany lub blokowany w obrębie guza.
Co to może oznaczać dla przyszłego leczenia
Dla rodzin i lekarzy mierzących się z pediatrycznymi glejakami wysokiego stopnia te wyniki nie zmieniają jeszcze sposobu leczenia, ale dostarczają ważnych wskazówek. Praca sugeruje, że wysoka aktywność genu BIRC2 w szczególności, a być może także BIRC3, oznacza guzy bardziej oporne i skłonne do szybszych nawrotów, czyniąc te geny potencjalnymi wskaźnikami złego rokowania. Ponieważ białka IAP są już badane jako cele terapeutyczne w nowotworach dorosłych, nowe wyniki wskazują na możliwość, że leki zaprojektowane do wyłączania tych przełączników przeżycia mogłyby w przyszłości być łączone z istniejącymi terapiami mózgu lub z immunoterapiami ukierunkowanymi na PD‑1. Badanie jest niewielkie i eksploracyjne, więc wnioski wymagają potwierdzenia w większych grupach i na poziomie białka, ale wskazuje na przyszłość, w której guz dziecka mógłby zostać zanalizowany pod kątem tych kluczowych przełączników, by lepiej przewidywać wynik i ostatecznie prowadzić do bardziej spersonalizowanych i skutecznych terapii.
Cytowanie: Petniak, A., Gil-Kulik, P., Zarychta, J. et al. Reduced expression of BIRC2 and BIRC3 associated with longer survival in pediatric high-grade gliomas. Sci Rep 16, 6665 (2026). https://doi.org/10.1038/s41598-026-35887-7
Słowa kluczowe: pediatryczny guz mózgu, glejak, apoptoza, BIRC2 BIRC3, immunoterapia