Clear Sky Science · pl
KIN17 ułatwia zapoczątkowanie i postęp nowotworu nerkowego przez szlak PI3K-AKT-mTOR
Dlaczego to badanie nad rakiem nerki ma znaczenie
Raka nerki wykrywa się coraz częściej, ale u wielu pacjentów choroba wciąż jest trudna do opanowania po jej rozsianiu. To badanie zagląda pod mikroskop — aż do poziomu pojedynczych cząsteczek w komórkach nowotworowych — aby zrozumieć, co napędza wzrost i naciekanie guzów nerkowych oraz czy eksperymentalny lek może zahamować ten proces. Wyniki wskazują na mało znane białko KIN17 jako nowego sprawcę w raku nerki i sugerują sposób pośredniego jego zaatakowania tabletką.
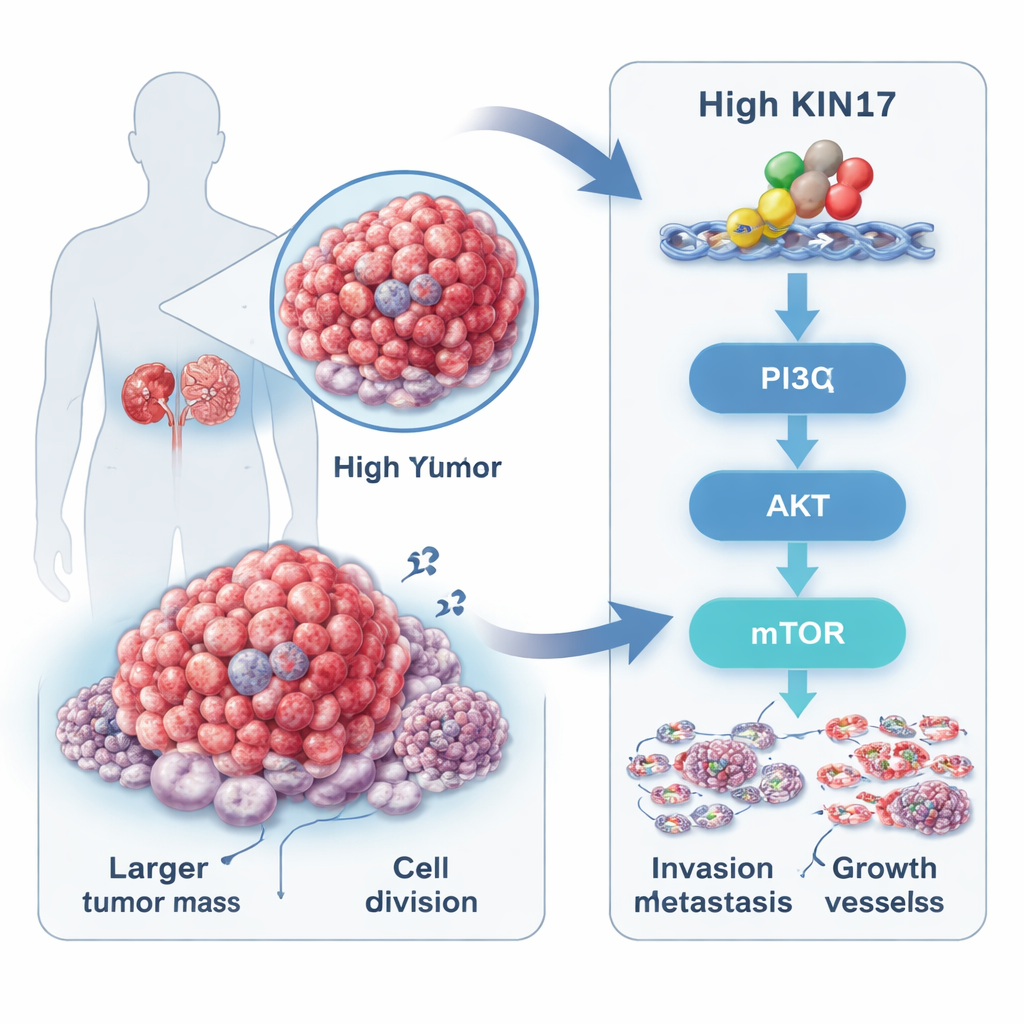
Ukryty sprawca wewnątrz guzów nerkowych
Gruczolakotorbielak nerek (renal cell carcinoma), najczęstsza postać raka nerki, często zaczyna się bez objawów i bywa wykrywana późno. Badacze skupili się na białku o nazwie KIN17, długo znanym z roli w ochronie i replikacji DNA, lecz dopiero ostatnio powiązanym z kilkoma innymi nowotworami. Analizując publiczne bazy danych nowotworowych i próbki guzów od 88 pacjentów, stwierdzili, że poziomy KIN17 były znacznie wyższe w tkance nowotworowej niż w sąsiedniej tkance niezmienionej. Pacjenci, których guzy zawierały więcej KIN17, mieli zwykle większe nowotwory, wyższy stopień złośliwości, bardziej zaawansowane stadium i częstsze przerzuty, a także krótszy czas przeżycia niż osoby z niskim KIN17. Ten wzór sugerował, że KIN17 nie jest jedynie biernym obserwatorem, lecz ściśle związany z agresywnością guza.
Testowanie KIN17 w komórkach nowotworowych
Aby sprawdzić, co KIN17 robi w komórkach raka nerki, zespół zmodyfikował linie komórkowe w laboratorium tak, by albo zmniejszać ekspresję KIN17, albo ją zwiększać. Kiedy obniżono poziom KIN17, komórki rosły wolniej, tworzyły mniej kolonii i miały ograniczoną zdolność poruszania się oraz naciekania przez sztuczne membrany. Więcej z tych komórek zatrzymywało się w fazie spoczynkowej cyklu komórkowego i przechodziło w kierunku obumierania — wykazywały wyższy poziom zaprogramowanej śmierci komórki. Odwrotne efekty obserwowano przy nadprodukcji KIN17: komórki mnożyły się szybciej, chętniej replikowały DNA, szybciej zamykały „zadrapania” w warstwach komórkowych i agresywniej naciekały. Te eksperymenty pokazały, że KIN17 działa jak pedał gazu dla wzrostu i rozprzestrzeniania się komórek raka nerki.
Szlak wzrostu przyłapany na działaniach
Następnie badacze zapytali, w jaki sposób KIN17 wywiera ten wpływ. Ich badania aktywności genów i testy białkowe wskazały na dobrze znaną sieć regulującą wzrost i przeżycie komórkowe — szlak PI3K–AKT–mTOR. Ten szlak często porównuje się do centralnego węzła sterującego, który mówi komórkom, kiedy rosnąć, dzielić się i unikać śmierci. Komórki raka nerek z wysokim poziomem KIN17 wykazywały wyższe sygnały „włączające” — chemiczne znaczniki zwane grupami fosforanowymi — na kluczowych składnikach tego szlaku, mimo że całkowita ilość tych białek nie ulegała zmianie. Gdy KIN17 zostało stłumione, znaczniki aktywujące spadły, a także zmieniły się poziomy cząsteczek związanych z ruchem i inwazją komórek. W eksperymentach na myszach guzy pochodzące z komórek bogatych w KIN17 rosły szybciej i były większe, a barwienia tkanek pokazały, że ten sam szlak wzrostu był w tych guzach silnie aktywowany.
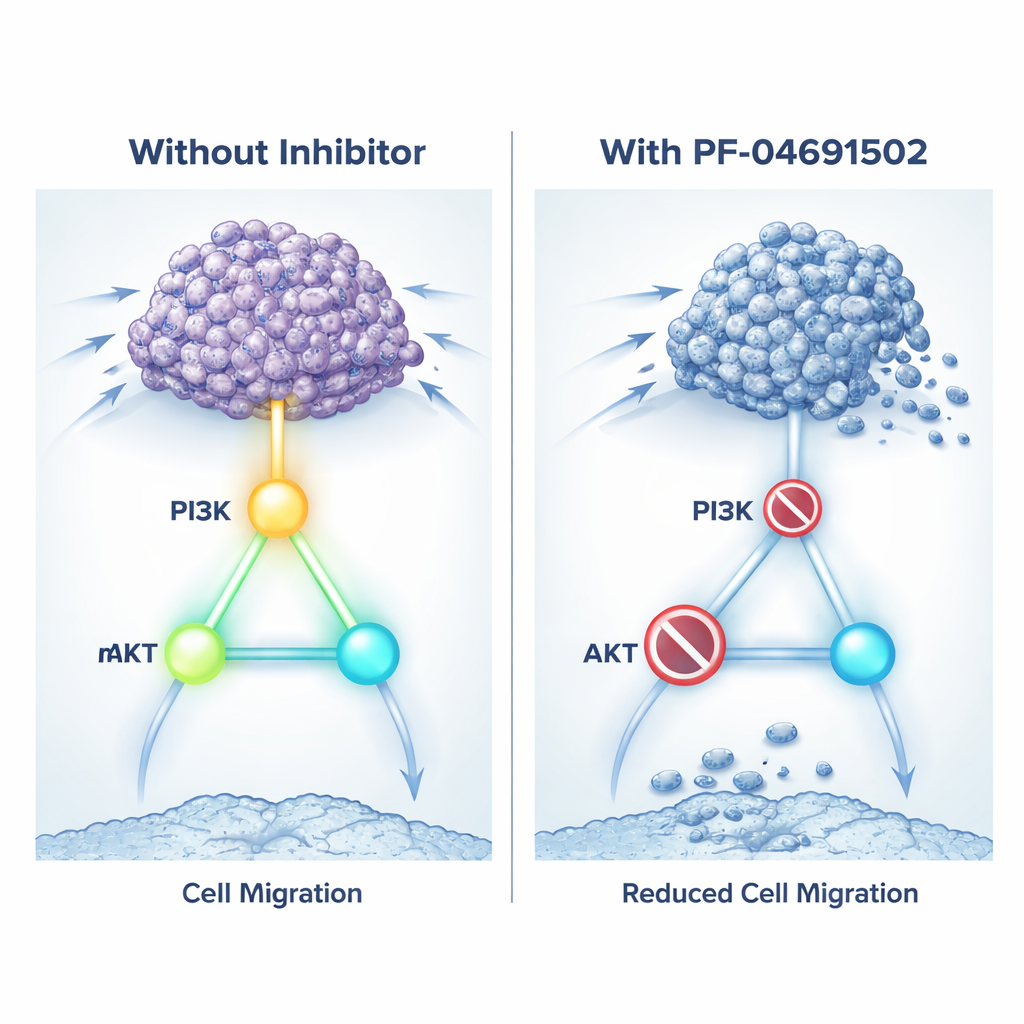
Przyciszanie sygnału lekiem celującym w dwa miejsca
Ponieważ bezpośrednie blokowanie KIN17 nie jest jeszcze możliwe dostępnymi lekami, zespół wypróbował inną taktykę: wyłączenie szlaku wzrostu, który wydaje się kontrolować. Użyto PF-04691502, eksperymentalnego leku blokującego jednocześnie PI3K i mTOR, dwa kluczowe przełączniki w tym szlaku. W hodowlach komórkowych leczenie komórek raka nerki z wysokim KIN17 tym inhibitorem spowalniało ich wzrost, ograniczało zdolność migracji i tworzenia kolonii oraz zwiększało odsetek komórek kierujących się ku śmierci. Lek zmniejszał także znaczniki aktywacyjne na PI3K, AKT i mTOR oraz obniżał poziomy białek związanych z inwazją. U myszy z guzami nerkowymi codzienne dawki PF-04691502 zmniejszały guzy nadprodukujące KIN17 i redukowały markery podziału komórkowego, jednocześnie zwiększając sygnały śmierci komórkowej. W istocie lek potrafił stłumić szkodliwe efekty KIN17 poprzez wyciszenie jego preferowanej drogi wzrostu.
Co to może znaczyć dla pacjentów
Dla osób z rakiem nerki te odkrycia niosą dwie obiecujące idee. Po pierwsze, pomiar KIN17 w próbkach guza mógłby pomóc lekarzom ocenić, jak agresywny jest nowotwór i jak duże jest ryzyko jego rozsiewu. Po drugie, guzy silnie zależne od KIN17 mogą być szczególnie wrażliwe na leki uderzające w szlak PI3K–AKT–mTOR, takie jak PF-04691502 lub podobne inhibitory celujące w dwa miejsca, które już są badane w próbach klinicznych dla innych nowotworów. Choć przed wprowadzeniem nowych terapii do praktyki klinicznej wciąż jeszcze wiele pracy, to badanie wyznacza jasny łańcuch zdarzeń — od KIN17, przez kluczowy szlak wzrostu, po niekontrolowaną ekspansję guza — i pokazuje, że przerwanie tego łańcucha może spowolnić raka nerki w laboratorium i na modelach zwierzęcych.
Cytowanie: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
Słowa kluczowe: rak nerkowokomórkowy, KIN17, PI3K AKT mTOR, terapia celowana, PF-04691502