Clear Sky Science · pl
Nanomateriał ZnO domieszkowany Cu i udekorowany Ag do wzmocnionego zastosowania przeciwbakteryjnego
Dlaczego drobne cząstki mają znaczenie przy poważnych infekcjach
Infekcje oporne na antybiotyki rosną na całym świecie, a opracowanie nowych leków jest powolne i kosztowne. Niniejsze badanie bada inną taktykę: wykorzystanie starannie zaprojektowanych drobnych cząstek z tlenku cynku zmieszanego z miedzią i srebrem, które fizycznie i chemicznie atakują bakterie, w tym trudne do leczenia szczepy, nawet w ciemności. Poprzez zrozumienie, jak te cząstki są zbudowane i jak uszkadzają drobnoustroje, badacze mają nadzieję stworzyć powłoki, opatrunki i powierzchnie, które cicho zabijają zarazki, zanim wywołają poważne choroby.
Budowanie lepszych cząstek zwalczających zarazki
Naukowcy postanowili ulepszyć tlenek cynku, materiał już znany z działania przeciwbakteryjnego, ale przeważnie aktywny jedynie na świetle. Zastosowali metodę „od podstaw przez spalanie”, w której sole metali i powszechny polimer są podgrzewane tak, że pienią się, palą i pozostawiają sztywną, wysoce porowatą sieć drobnych kryształów. W strukturę tlenku cynku wprowadzono miedź i srebro, tworząc materiał mieszany zwany heterostrukturą, w którym kilka metali i tlenków metali styka się ze sobą bardzo blisko. 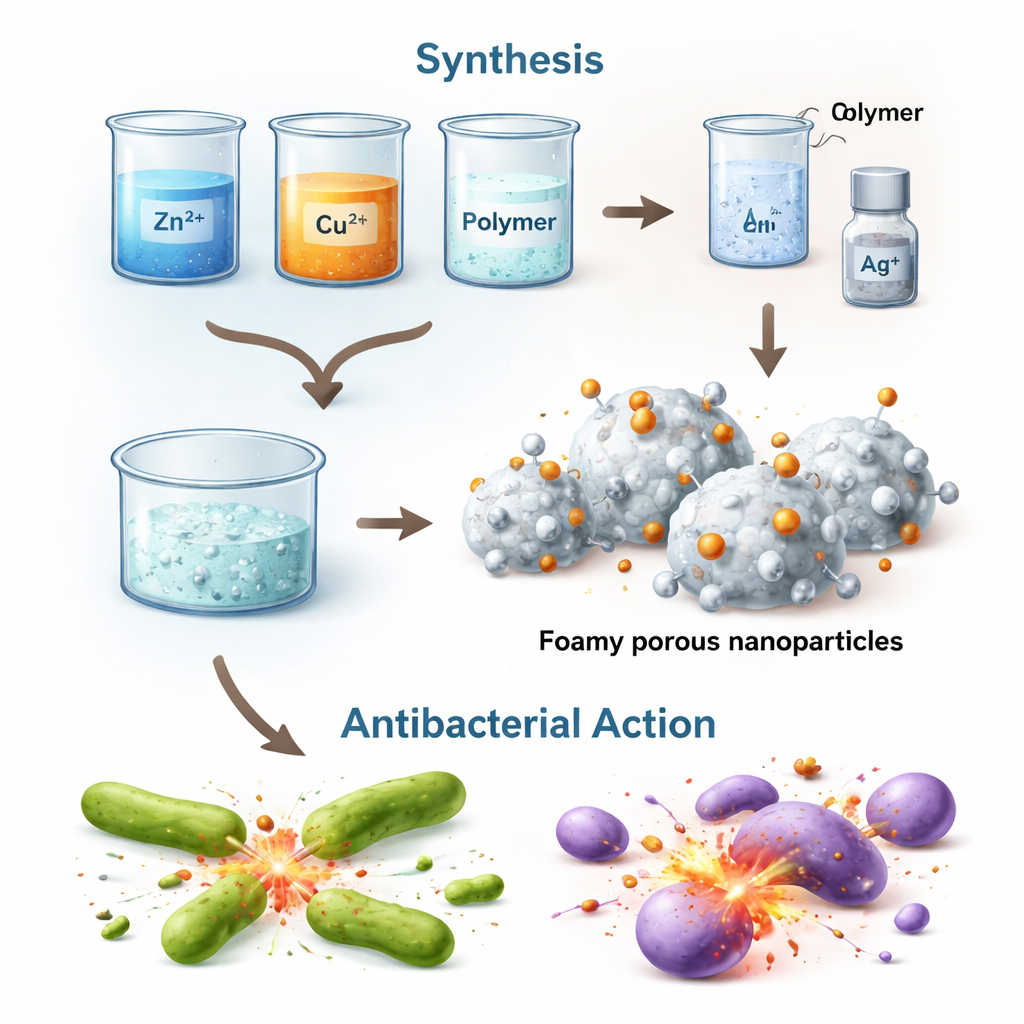
Zajrzeć do wnętrza nowego materiału
Aby zobaczyć, co uzyskano, zespół zastosował zestaw badań strukturalnych i optycznych. Pomiary rentgenowskie wykazały, że atomy miedzi wślizgnęły się w sieć krystaliczną tlenku cynku, nieznacznie ją ściskając, podczas gdy srebro w większości utworzyło własne małe kryształy na powierzchni. Wysokorozdzielcza mikroskopia elektronowa ujawniła te różne składniki upakowane razem w porowatych, piankopodobnych strukturach. Pomiary optyczne potwierdziły, że dodanie miedzi i srebra zmniejszyło przerwę energetyczną tlenku cynku i poprawiło transport ładunków przez materiał. W praktyce oznacza to, że łatwiej może powstawać krótkożyciowe, szkodliwe związki na bazie tlenu oraz że reaktywne ładunki nie ulegają wzajemnemu odwołaniu się, co jest przydatne do zabijania bakterii.
Przekuwanie struktury w moc przeciwbakteryjną
Kluczowym testem było sprawdzenie, czy te zaprojektowane cząstki rzeczywiście mogą powstrzymać wzrost bakterii. Naukowcy porównali zwykły tlenek cynku z próbkami domieszkowanymi miedzią, udekorowanymi srebrem oraz z w pełni połączonymi cząstkami miedź–srebro–tlenek cynku wobec bakterii Gram-dodatnich i Gram-ujemnych, które różnią się budową ściany komórkowej. Badali też wersje przed i po dodatkowym etapie wygrzewania zwanego kalcynacją. Zwykły tlenek cynku działał umiarkowanie, głównie przed końcowym wygrzewaniem, ale w dużej mierze tracił efekt po nim. W przeciwieństwie do tego materiał w pełni złożony — zawierający tlenek cynku, tlenek miedzi i srebro — stał się bardziej efektywny po kalcynacji, osiągając strefę hamowania do 22 milimetrów przeciwko Streptococcus pyogenes, bakteriom Gram-dodatnim, przy najwyższej testowanej dawce. Ogólnie nowe mieszaniny cząstek przewyższały cząstki jedno-metalowe, zwłaszcza wobec szczepów Gram-dodatnich.
Jak cząstki atakują bakterie w ciemności
W odróżnieniu od wielu materiałów aktywowanych światłem, te cząstki zaprojektowano do działania bez oświetlenia. Badanie sugeruje, że mieszane cząstki metaliczne zabijają bakterie poprzez wielotorowy atak. Po pierwsze, jony cynku, miedzi i srebra powoli rozpuszczają się z powierzchni cząstki i wiążą z błonami bakteryjnymi, enzymami i DNA, zaburzając istotne procesy i powodując nieszczelność otoczki komórkowej. Po drugie, bliski kontakt między różnymi metalami sprzyja generowaniu reaktywnych form tlenu — silnie agresywnych postaci tlenu — nawet w ciemności. Te rodzaje uszkadzają białka, lipidy i materiał genetyczny. Po trzecie, porowata, chropowata tekstura cząstek zwiększa kontakt z komórkami bakteryjnymi i może fizycznie uszkadzać ich zewnętrzne warstwy. Razem te efekty przytłaczają mechanizmy obronne bakterii i utrudniają rozwój oporności. 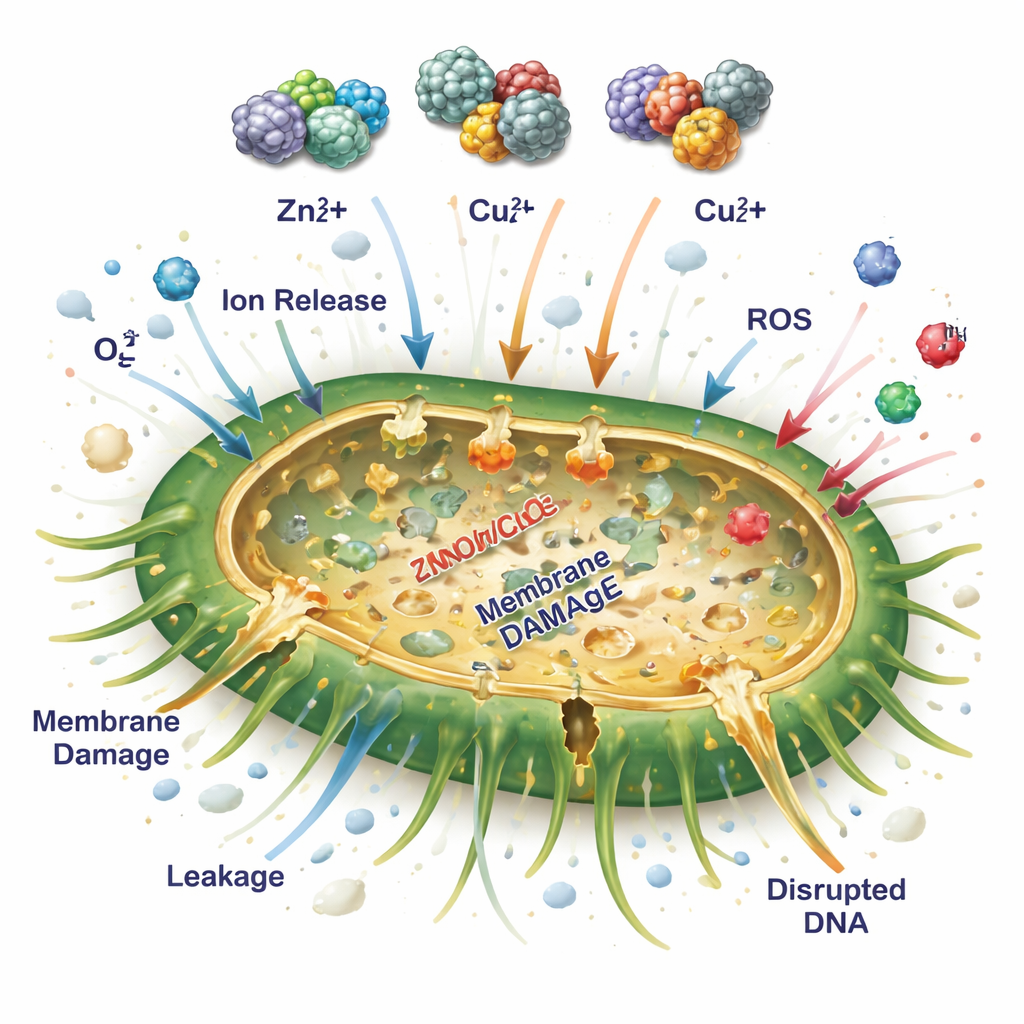
Z naczynia laboratoryjnego do ochrony w rzeczywistym świecie
Dla szerokiego odbiorcy główny przekaz jest taki, że staranne łączenie znanych metali, takich jak cynk, miedź i srebro, w jedną, dobrze ustrukturyzowaną nanocząstkę może przekształcić zwykły składnik w potężne, szerokospektralne narzędzie przeciwbakteryjne. Najskuteczniejszy materiał w tym badaniu zatrzymał niektóre bakterie prawie tak skutecznie, jak standardowy antybiotyk, bez polegania na ekspozycji na światło. Ponieważ te cząstki można wytwarzać jako porowate pianki w stosunkowo prostym procesie, w przyszłości mogłyby zostać skalowane do zastosowań w opatrunkach, powłokach implantów medycznych lub na powierzchniach w szpitalach, które pasywnie tłumią wzrost bakterii. Choć potrzeba dalszych badań potwierdzających bezpieczeństwo i skuteczność w tkankach, badanie wskazuje obiecującą drogę do fizykochemicznych środków przeciwbakteryjnych, które uzupełniają, a nie zastępują, tradycyjne antybiotyki.
Cytowanie: Gebretsadik, A., Reddy, S.G., Gonfa, B.A. et al. Ag-decorated Cu-doped ZnO nanomaterial for enhanced antibacterial application. Sci Rep 16, 5552 (2026). https://doi.org/10.1038/s41598-026-35838-2
Słowa kluczowe: nanomateriały przeciwbakteryjne, nanocząstki tlenku cynku, domieszkowanie miedzią i srebrem, oporność na antybiotyki, heterostrukturalne nanokompozyty