Clear Sky Science · pl
Integracyjne podejście pojedynczych komórek i uczenia maszynowego ujawnia prognostyczne podtypy fibroblastów i konstruuje sygnaturę ryzyka związaną z fibroblastami w gruczolakoraku płuca
Dlaczego „komórki pomocnicze” wokół guzów płuc mają znaczenie
Gruczolakorak płuca jest jedną z najczęstszych i najgroźniejszych postaci raka płuca, a jednak pacjenci z pozornie podobnymi nowotworami mogą mieć bardzo różne rokowania i reakcje na leczenie. W tym badaniu autorzy wykraczają poza same komórki nowotworowe, skupiając się na otaczających je „komórkach pomocniczych” zwanych fibroblastami, które uczestniczą w budowie i przebudowie tkanki. Dzięki analizie tych komórek pojedynczo, a następnie zastosowaniu zaawansowanych modeli komputerowych, badacze pokazują, że fibroblasty występują w odrębnych odmianach, które potrafią przewidywać przebieg choroby oraz odpowiedź guza na nowoczesne immunoterapie.
Uważne przyjrzenie się sąsiedztwu guza
Wykorzystując nowoczesne sekwencjonowanie RNA pojedynczych komórek, zespół przeanalizował ponad 140 000 pojedynczych komórek z nieleczonych próbek gruczolakoraka płuca. Technika ta identyfikuje, które geny są aktywne w każdej komórce, co pozwoliło autorom podzielić guz na głównych mieszkańców: komórki układu odpornościowego, komórki nowotworowe, komórki naczyń krwionośnych oraz fibroblasty. Okazało się, że guzy wykazują dużą zmienność co do udziału poszczególnych typów komórek. Niektóre guzy są wypełnione komórkami odpornościowymi, inne z kolei dominują fibroblasty i tkanka strukturalna. Kolejne analizy wykazały, że każdy z tych typów komórek pełni wyspecjalizowane funkcje, od koordynowania odpowiedzi odpornościowej po budowanie rusztowania strukturalnego guza.
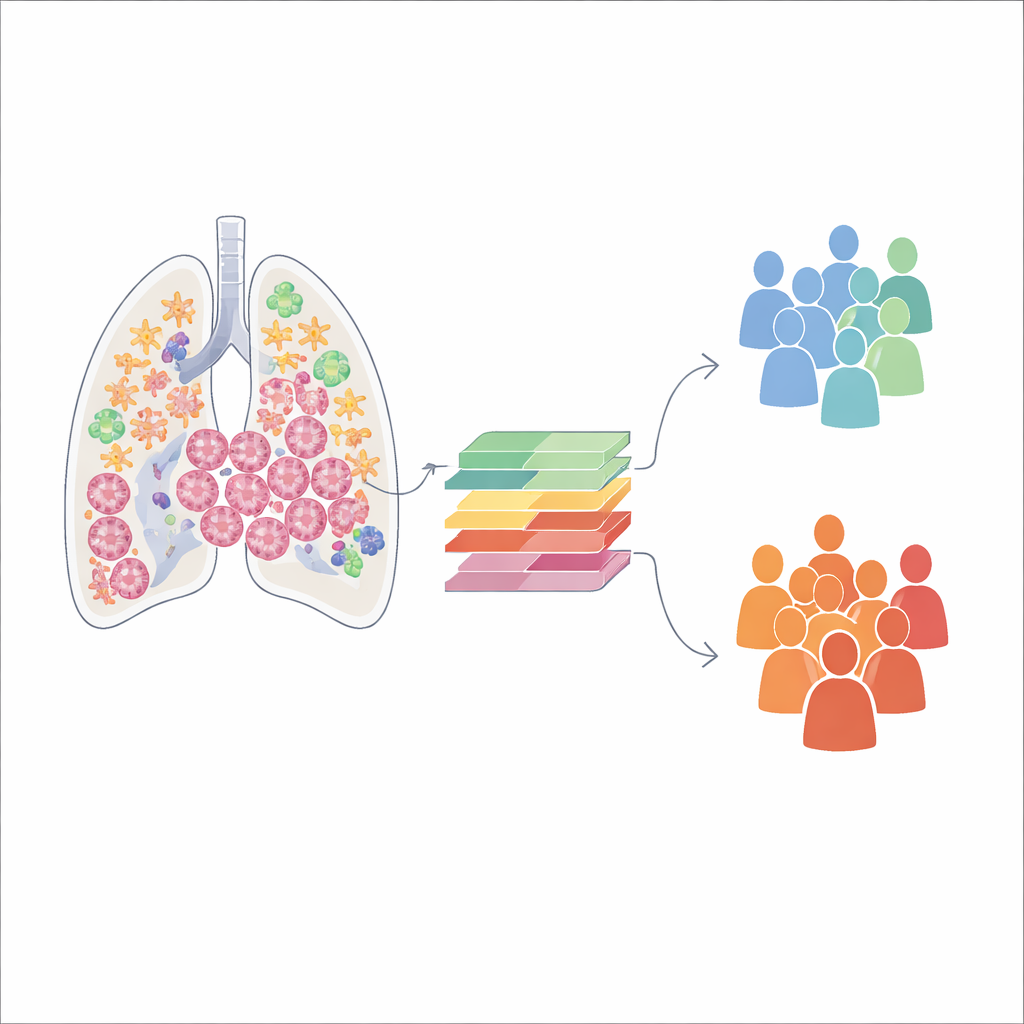
Nie wszystkie fibroblasty są takie same
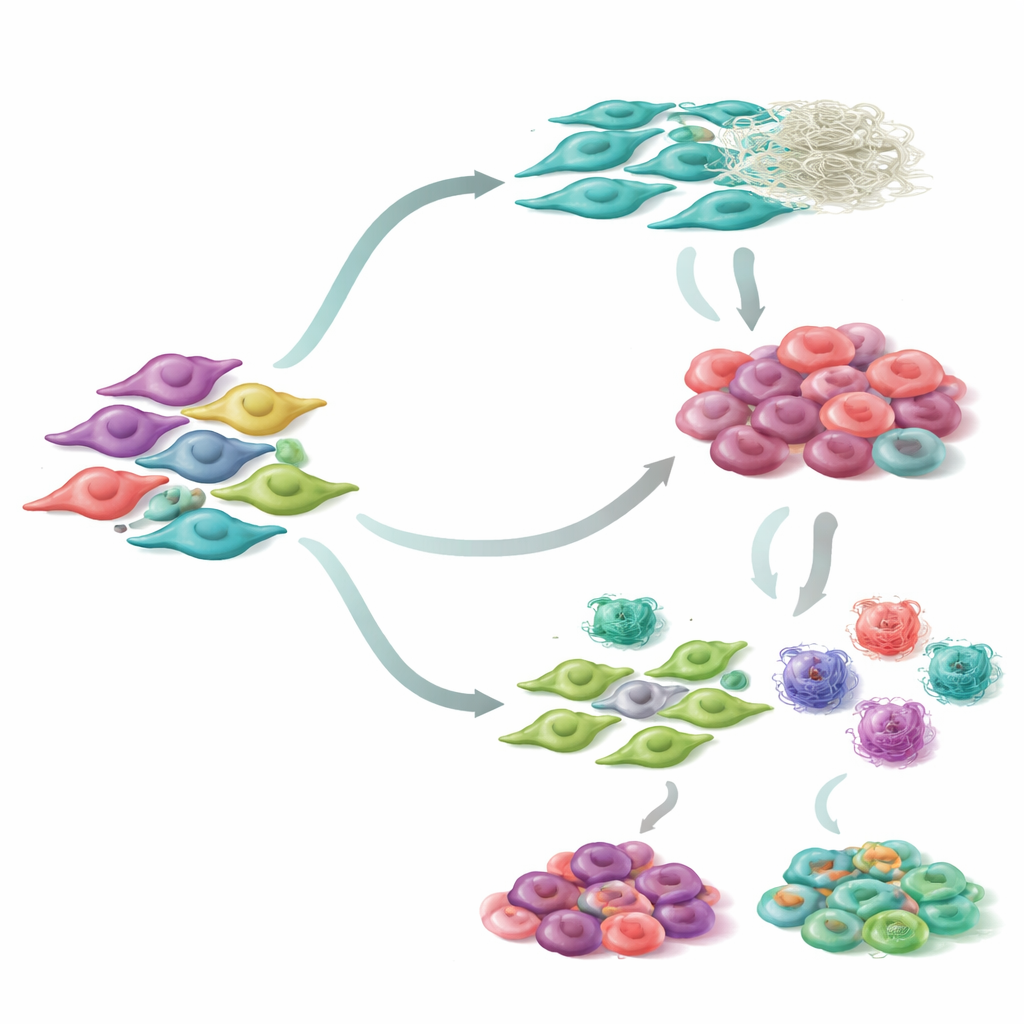
Skupiając się konkretnie na fibroblastach, badacze wyróżnili siedem odrębnych podgrup fibroblastów występujących w guzach płuca. Odtwarzając, jak te komórki zmieniają się w czasie, zaobserwowali dwa główne szlaki rozwojowe. Wzdłuż jednego szlaku fibroblasty stopniowo nabierają cech komórek kurczliwych, zwiększających sztywność tkanki i przekształcających otoczenie guza. Wzdłuż drugiego szlaku fibroblasty angażują się bardziej we współpracę z układem odpornościowym, przyciągając lub tłumiąc komórki odpornościowe. Każda podgrupa wykazywała unikatowe wzorce aktywności genów i była powiązana z różnymi zadaniami biologicznymi, takimi jak skurcz przypominający mięśnie, migracja czy regulacja odporności. Co ważne, pacjenci, których guzy były wzbogacone o konkretne podtypy fibroblastów, mieli tendencję do dłuższego przeżycia, co oznacza, że skład stanów fibroblastów ma realne znaczenie kliniczne.
Budowa wskaźnika ryzyka na podstawie sygnałów od fibroblastów
Aby przekształcić te biologiczne obserwacje w narzędzie możliwe do użycia w praktyce klinicznej, zespół połączył geny-markery fibroblastów z danych pojedynczych komórek z danymi „bulk” tkanek guzowych od setek pacjentów z dużych publicznych baz. Następnie zastosowano zestaw 10 metod uczenia maszynowego, testując 101 kombinacji modeli, by ustalić, który zestaw genów związanych z fibroblastami najlepiej przewiduje przeżycie pacjentów. Zwycięski model, nazwany sygnaturą związaną z fibroblastami (FRS), wykorzystuje 29 genów do przypisania pacjentowi wyniku ryzyka. W głównym zbiorze danych i w sześciu niezależnych kohortach pacjentów osoby z wysokimi punktami FRS konsekwentnie miały gorsze przeżycie niż osoby z niskimi punktami. FRS pozostał także silnym predyktorem po uwzględnieniu wieku, płci i stadium guza oraz poprawiał predykcję w połączeniu ze standardowym systemem TNM.
Wskazówki o ucieczce przed układem odpornościowym i odpowiedzi na leczenie
Ponieważ wielu pacjentów otrzymuje obecnie immunoterapię, autorzy sprawdzili, czy oceniany na podstawie fibroblastów wskaźnik odzwierciedla cechy immunologicznego mikrośrodowiska guza. Stwierdzili, że guzy o niskim FRS miały bogatszą infiltrację komórek zwalczających nowotwór, takich jak limfocyty CD8 i komórki NK, oraz wyższe ekspresje genów zaangażowanych w prezentację fragmentów guza układowi odpornościowemu. Guzy o wysokim FRS wykazywały natomiast mniej korzystnych komórek odpornościowych, większy udział komórek nowotworowych, większą niestabilność genetyczną i cechy wykluczenia immunologicznego, czyli utrzymywania komórek odpornościowych na dystans. Miary symulujące prawdopodobną odpowiedź na leki blokujące punkty kontrolne sugerowały, że pacjenci z niskim FRS mogą bardziej skorzystać z tych terapii, podczas gdy pacjenci z wysokim FRS mogą być bardziej oporni.
Wyróżnienie obiecującego genu docelowego
Wśród genów składających się na FRS zespół zwrócił szczególną uwagę na gen TIMP1 jako silny marker złego rokowania. TIMP1 wykazywał wysoką ekspresję w wielu typach nowotworów i był szczególnie podwyższony w tkance gruczolakoraka płuca w porównaniu z przyległą prawidłową tkanką płuc. W eksperymentach laboratoryjnych obniżenie poziomu TIMP1 w liniach komórkowych raka płuca zmniejszyło zdolność komórek do inwazji przez macierz oraz tworzenia nowych kolonii, co sugeruje, że TIMP1 przyczynia się do wzrostu i rozprzestrzeniania się guza. Wyniki te wskazują na TIMP1 jako kandydat na cel przyszłych leków mających osłabić maszyny strukturalne i immunomodulacyjne guza.
Co to oznacza dla pacjentów
Praca ta pokazuje, że towarzyszące guzowi komórki podporowe, w szczególności fibroblasty, zawierają cenne informacje o zachowaniu choroby i potencjalnej odpowiedzi na leczenie. Łącząc pomiary na poziomie pojedynczych komórek z uczeniem maszynowym, autorzy stworzyli wskaźnik ryzyka oparty na fibroblastach, który pozwala podzielić pacjentów na grupy o wyższym i niższym ryzyku oraz dać wskazówki, które guzy mogą być bardziej oporne na immunoterapię. Choć przed zastosowaniem takiego wskaźnika w codziennej opiece konieczne są dalsze testy, badanie podkreśla, że skuteczne leczenie raka płuca będzie wymagać nie tylko ataku na same komórki nowotworowe, lecz także ograniczenia działania otaczających fibroblastów, które pomagają guzowi rosnąć i ukrywać się.
Cytowanie: Cheng, S., Zhang, H., Mu, Q. et al. Integrative single-cell and machine learning framework reveals prognostic fibroblast subtypes and constructs a fibroblast-related risk signature in lung adenocarcinoma. Sci Rep 16, 7965 (2026). https://doi.org/10.1038/s41598-026-35830-w
Słowa kluczowe: gruczolakorak płuca, fibroblasty związane z nowotworem, sekwencjonowanie pojedynczych komórek, mikrośrodowisko guza, odpowiedź na immunoterapię