Clear Sky Science · pl
Niedożywienie mięśni związane z sepsą łagodzone przez farmakologiczną inhibicję szlaku sygnalizacyjnego STAT3 u myszy
Dlaczego poważne infekcje odbierają siłę
Przeżycie zagrażającej życiu infekcji, takiej jak sepsa, to dopiero połowa sukcesu. Wielu pacjentów wychodzi z oddziału intensywnej opieki tak osłabionych, że chodzenie, wchodzenie po schodach czy nawet podnoszenie ramion staje się wysiłkiem. W tym badaniu zadano proste, lecz pilne pytanie: czy można zatrzymać rozkładanie własnych mięśni przez organizm podczas sepsy, a jeśli tak, to jak? Używając myszy, komórek mięśniowych w hodowli oraz obserwacji pacjentów z oddziału intensywnej terapii, badacze wyśledzili kluczową drogę sygnalizacyjną napędzającą utratę mięśni — i pokazali, że ukierunkowany lek może częściowo zablokować ten proces.
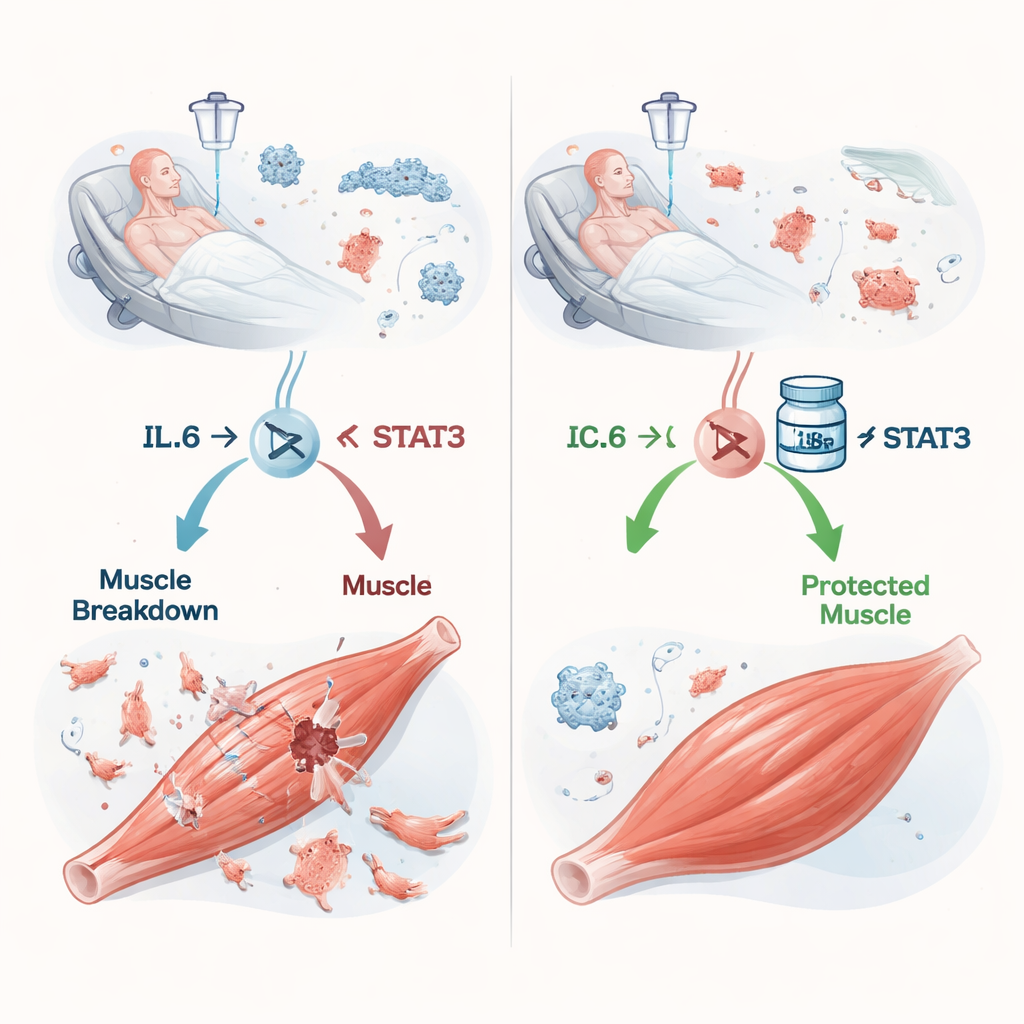
Reakcja łańcuchowa od infekcji do utraty mięśni
Sepsa występuje, gdy odpowiedź organizmu na infekcję wymyka się spod kontroli, zalewając krwiobieg cząsteczkami zapalnymi. Jedną z najważniejszych jest interleukina‑6 (IL‑6). Wcześniejsze prace sugerowały, że IL‑6 może nakłaniać mięśnie do rozkładu własnych białek, ale szczegóły były niejasne. Autorzy skupili się na STAT3, białku wewnątrzkomórkowym przekazującym sygnał IL‑6 do jądra komórkowego, gdzie geny są włączane lub wyłączane. U myszy otrzymujących zawiesinę wyrostka robaczkowego — zasadniczo kontrolowaną infekcję mieszaną bakterii — poziomy IL‑6 we krwi i w mięśniach nóg gwałtownie wzrosły w miarę pogarszania się sepsy. Jednocześnie w mięśniach aktywował się STAT3, a zwierzęta traciły na wadze, masie mięśniowej i sile chwytu w sposób zależny od nasilenia choroby, co wiernie odzwierciedlało obserwacje u pacjentów w stanie krytycznym.
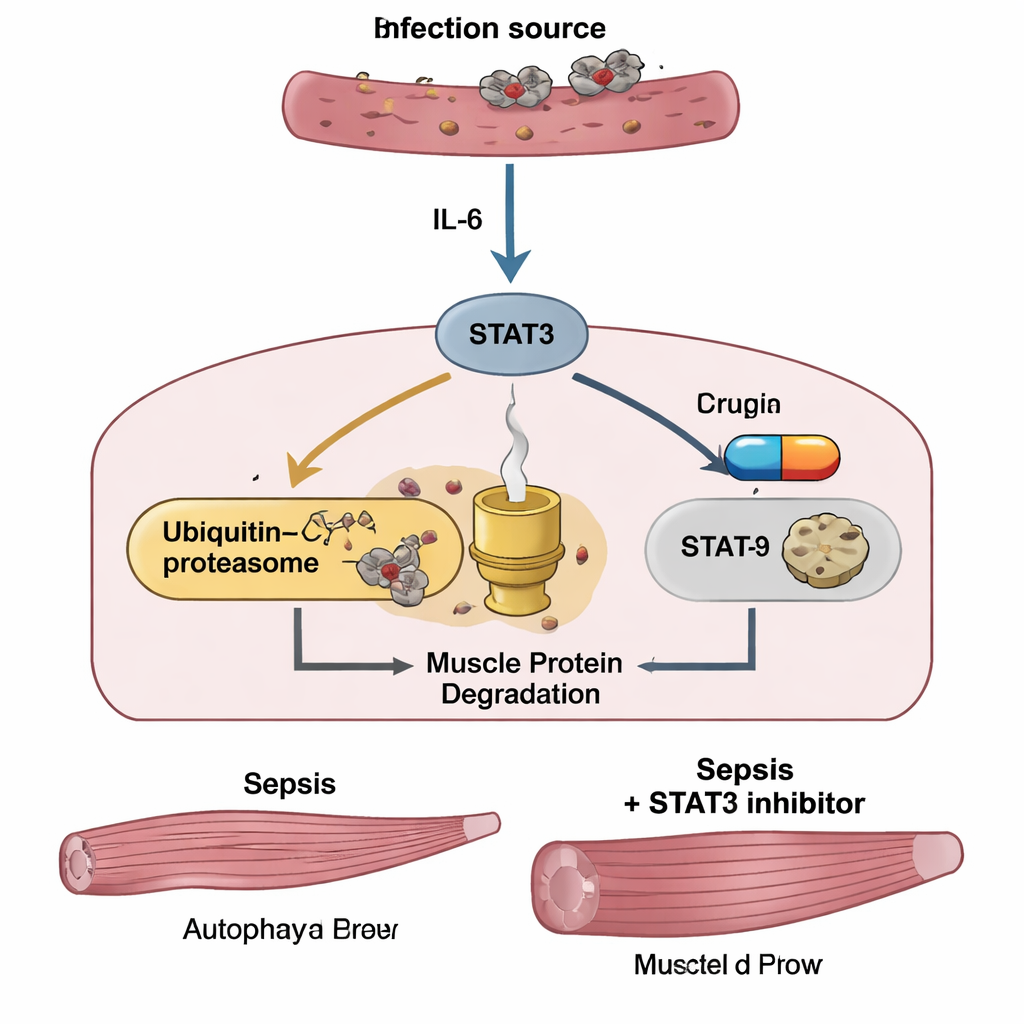
Jak sepsa przeprogramowuje komórki mięśniowe
Aby zrozumieć, co sepsa robi wewnątrz włókien mięśniowych, zespół przeanalizował aktywność genów w mięśniu piszczelowym przednim (tibialis anterior), ważnym mięśniu nogi. W tysiącach genów zaobserwowano zmiany aktywności u myszy septycznych w porównaniu ze zdrowymi kontrolami. Włączone zostały szlaki związane z zapaleniem, stresem komórkowym i zwłaszcza sygnalizacją IL‑6/STAT3. Wzrósł poziom dwóch głównych systemów usuwania białek: układu ubikwityna–proteasom, który oznacza konkretne białka mięśniowe do zniszczenia, oraz autofagii, bardziej ogólnego procesu recyklingu. Kluczowe enzymy „rozkrawające” mięśnie, MuRF1 i atrogin‑1, znacząco się zwiększyły, podczas gdy szlaki sprzyjające wzrostowi i klasyczne sygnały prowadzące do śmierci komórkowej pozostały w dużej mierze niezmienione. W równoległych eksperymentach hodowane mysi komórki mięśniowe wystawione na lipopolisacharyd (LPS), składnik ścian Gram‑ujemnych bakterii, wykazały ten sam wzorzec: aktywację IL‑6 i STAT3, wzrost MuRF1 i atrogin‑1, nasilenie autofagii oraz widoczne przerzedzenie włókien mięśniowych.
Blokowanie kluczowego przełącznika w ochronie mięśni
Główny eksperyment sprawdzał, czy wyłączenie STAT3 może oszczędzić mięśnie. Myszy z sepsą otrzymywały małocząsteczkowy inhibitor STAT3 o nazwie C188‑9, rozpoczynając godzinę po zakażeniu, a następnie codziennie. Lek nie złagodził początkowego „sztormu cytokin” — stężenia IL‑6 i innego czynnika zapalnego, TNF‑α, we krwi pozostawały wysokie, a masa ciała i apetyt nie wróciły szybko do normy. Mimo to C188‑9 wyraźnie chronił mięśnie szkieletowe: myszy leczone zachowały więcej masy mięśnia tibialis, miały silniejszy chwyt i większe włókna mięśniowe w mikroskopie niż nieleczone myszy septyczne. W mięśniach C188‑9 znacznie zmniejszył aktywowany STAT3 i obniżył poziomy MuRF1 i atrogin‑1, pozostawiając markery autofagii w dużej mierze niezmienione. W eksperymentach w hodowli wstępne leczenie komórek mięśniowych C188‑9 podobnie tłumiło aktywację STAT3 i wzrost MuRF1 oraz atrogin‑1, zapobiegając zmniejszaniu się włókien wywołanemu przez LPS, ponownie bez zahamowania autofagii.
Wskazówki od pacjentów na oddziale intensywnej terapii
Aby sprawdzić, czy te mechanizmy mają znaczenie u ludzi, badacze obserwowali 67 dorosłych z sepsą przyjętych na oddział intensywnej terapii w Japonii. Badania krwi przy przyjęciu wykazały, że pacjenci z wstrząsem septycznym mieli szczególnie wysokie poziomy IL‑6. W całej grupie IL‑6 — ale nie TNF‑α — silnie korelował z punktacją nasilenia sepsy oraz z markerami zapalenia i uszkodzenia mięśni we krwi. W podgrupie 45 pacjentów, którzy przeszli dwa badania CT jamy brzusznej, poziomy IL‑6 przy przyjęciu przewidywały, o ile zmniejszy się mięsień lędźwiowy (psoas) przy dolnym odcinku kręgosłupa w ciągu następnego jednego do trzech tygodni. Osoby, które straciły najwięcej mięśni, miały wyraźnie gorsze przeżycie w ciągu dwóch lat niż ci, którzy zachowali więcej masy mięśniowej, co podkreśla, że zanik mięśni związany z sepsą to nie tylko kwestia estetyczna — wiąże się on z długoterminową śmiertelnością.
Co to może znaczyć dla przyszłych terapii
W całości dane z myszy, komórek i ludzi kreślą wiarygodną opowieść: podczas sepsy gwałtownie rosnące IL‑6 aktywuje STAT3 w mięśniach, co z kolei nakręca system degradacji białek, który pozbawia włókna mięśniowe ich aparat kontrakcyjny. Autofagia również się zwiększa, ale wydaje się być mniej bezpośrednio kontrolowana przez STAT3. Poprzez farmakologiczne zablokowanie STAT3 za pomocą C188‑9 badacze byli w stanie przerwać tę drogę „samozjadania” u myszy i w hodowlach komórkowych, zachowując siłę nawet gdy infekcja i zapalenie trwały. Chociaż prace te pozostają przedkliniczne i nie dowodzą, że inhibitory STAT3 pomogą pacjentom, wskazują oś IL‑6/STAT3 jako obiecujący cel dla leków mających zapobiegać lub zmniejszać głębokie osłabienie mięśni, które dotyka wielu ocalonych po sepsie.
Cytowanie: Ono, Y., Saito, M., Yoshihara, I. et al. Sepsis-associated skeletal muscle wasting is ameliorated by pharmacological inhibition of the STAT3 signaling pathway in mice. Sci Rep 16, 5008 (2026). https://doi.org/10.1038/s41598-026-35815-9
Słowa kluczowe: sepsa, zanik mięśni, STAT3, zapalenie, powrót do zdrowia po ciężkiej chorobie