Clear Sky Science · pl
Lekki SwiM-UNet z wielowymiarowym adapterem dla efektywnej segmentacji obrazów medycznych na urządzeniach
Inteligentniejsze badania przy łóżku pacjenta
Obrazowanie mózgu może ujawnić zagrażające życiu guzy, ale przekształcenie surowych skanów w wyraźne kontury, na których lekarze mogą działać, wciąż bywa powolne i wymagające obliczeniowo. W tym badaniu przedstawiono SwiM-UNet, nowy algorytm potrafiący segmentować guzy mózgu ze skanów MRI 3D z dokładnością na poziomie stanu wiedzy, działając jednocześnie efektywnie na urządzeniach lokalnych — przybliżając precyzyjną analizę obrazów do łóżka pacjenta lub nawet do mobilnych klinik. 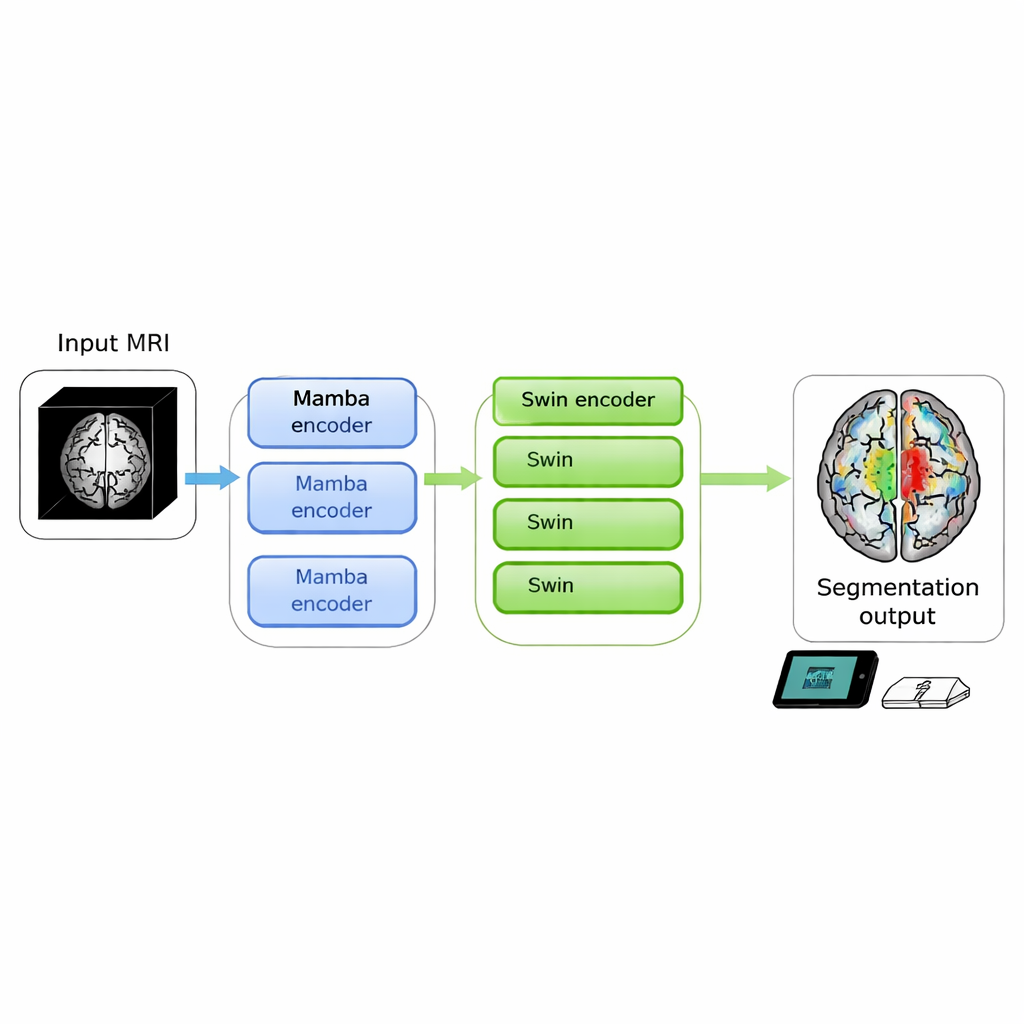
Dlaczego precyzyjne kontury guzów mają znaczenie
Nowoczesna medycyna w dużej mierze opiera się na obrazowaniu przy planowaniu operacji, radioterapii i terapii farmakologicznej. W przypadku guzów mózgu lekarze potrzebują nie tylko potwierdzenia ich obecności, lecz także dokładnej informacji, gdzie zaczynają się i kończą ich różne części. Zadanie to, zwane segmentacją, zwykle wykonuje się lub koryguje ręcznie przez specjalistów kawałek po kawałku — co zabiera dużo czasu, może opóźniać decyzje i różnić się między ekspertami. Narzędzia automatycznej segmentacji oparte na uczeniu głębokim poprawiły tę sytuację, ale najbardziej precyzyjne z nich często wymagają dużych procesorów graficznych, co utrudnia ich bezpośrednie zastosowanie w klinice, szczególnie na mniejszych lub przenośnych maszynach.
Dwie potężne idee, które trudno zmieścić na małych urządzeniach
Ostatnie przełomy w wizji komputerowej pochodzą głównie z dwóch rodzin modeli. Systemy oparte na transformatorach, takie jak Swin Transformer, znakomicie wychwytują globalne wzorce w całym skanie 3D i napędzały najlepsze segmentery guzów mózgu. Jednak ich podstawowa operacja, zwana samo‑uwagą (self-attention), staje się ekstremalnie kosztowna wraz ze wzrostem rozmiaru obrazu, co ogranicza ich użycie w czasie rzeczywistym lub na zwartej platformie sprzętowej. Nowsza rodzina, znana jako Mamba i oparta na modelach stanu (state‑space models), oferuje sprytne rozwiązanie: przetwarza sekwencje w zasadzie w czasie liniowym, redukując liczbę potrzebnych obliczeń. Wczesne eksperymenty w obrazowaniu medycznym pokazały, że modele w stylu Mamba są szybkie i wydajne, ale zwykle ustępują transformatorom pod względem jakości segmentacji, zwłaszcza przy złożonych kształtach guzów.
Połączenie szybkości i dokładności w jednym projekcie
Autorzy postanowili połączyć mocne strony obu podejść w jednym modelu 3D. Ich SwiM-UNet zachowuje znaną, litą litery U architekturę powszechnie stosowaną w obrazowaniu medycznym, z enkoderem kompresującym informacje i dekoderem odtwarzającym szczegółowe segmentacje. We wczesnych etapach, gdy skan jest nadal duży i wysokiej rozdzielczości, wykorzystują wydajne bloki Mamba, aby utrzymać obciążenie obliczeniowe na umiarkowanym poziomie. Głębiej w sieci, po downsamplingu danych, przechodzą do uproszczonych bloków Swin Transformer, które dzięki mniejszym rozmiarom reprezentacji mogą modelować długodystansowe zależności bez przeciążania sprzętu. Niestandardowy mostek zwany MS-adapter łączy te dwa tryby. Analizuje cechy wzdłuż szerokości, wysokości i głębokości wolumenu osobno, a także w poprzek kanałów, i dzięki małym jednostkom bramkującym uczy się, jak bardzo każdy z tych widoków powinien wpływać na ostateczną reprezentację. 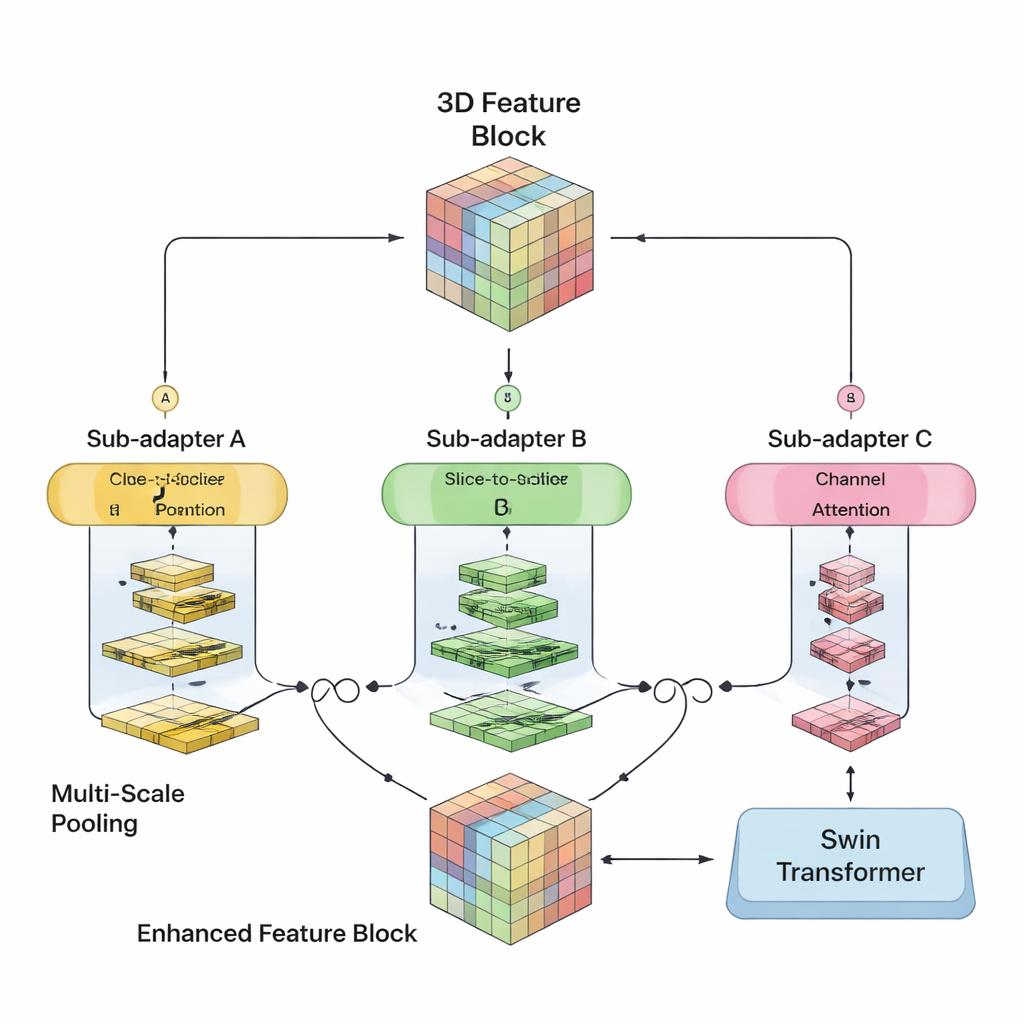
Więcej przy mniej obliczeń
Ponad samą hybrydową strukturą zespół ograniczył nadmiar obliczeń, stosując niskorzędowe warstwy w pełni połączone oraz dekoder, który celowo zmniejsza liczbę kanałów, które musi obsługiwać. Przetestowali kilka wariantów z różnymi kombinacjami warstw Mamba i Swin i stwierdzili, że użycie Mamba w pierwszych trzech etapach enkodera i Swin tylko na najgłębszym etapie daje najlepszą równowagę między szybkością a dokładnością. Na dwóch dużych publicznych zbiorach danych dotyczących guzów mózgu z wyzwań BraTS 2023 i 2024, SwiM-UNet osiągnął wyższą dokładność i precyzyjniejsze granice niż czołowe modele oparte wyłącznie na transformatorach, wyłącznie na Mamba i wcześniejsze modele hybrydowe, przy jednoczesnym wykorzystaniu znacznie mniejszej liczby operacji zmiennoprzecinkowych i skróceniu czasu wnioskowania do około 45 milisekund na łatę skanu na nowoczesnej karcie graficznej.
Gotowy na urządzenia w realnym świecie
Aby sprawdzić, czy te zyski mają znaczenie poza laboratorium, autorzy porównali wymagania obliczeniowe modelu z możliwościami typowych klinicznych systemów brzegowych — przenośnych konsol MRI, komputerów punktu opieki i stacji roboczych w salach operacyjnych. Ich analiza sugeruje, że w przeciwieństwie do cięższych modeli transformatorowych, SwiM-UNet mieści się komfortowo w ograniczeniach mocy, pamięci i szybkości takich urządzeń, często spełniając wymagania czasu rzeczywistego. Model dobrze sprawdził się także na osobnym zbiorze danych CT jamy brzusznej, co wskazuje, że podejście może uogólniać się poza guzy mózgu, a nawet poza MRI.
Co to oznacza dla pacjentów i klinicystów
W praktyce SwiM-UNet pokazuje, że można zbliżyć się do dokładności najbardziej zaawansowanych modeli segmentacyjnych, jednocześnie utrzymując obciążenie obliczeniowe na tyle niskie, by pracować bezpośrednio na urządzeniu. To może umożliwić szybsze i bardziej spójne wyznaczanie konturów guzów na oddziałach ratunkowych, w szpitalach wiejskich czy w mobilnych jednostkach obrazowania, bez wysyłania wrażliwych skanów do odległych serwerów. Choć potrzebne są dalsze prace nad dopasowaniem metody do różnych skanerów i warunków, ta hybrydowa koncepcja wskazuje w kierunku przyszłości, w której analiza obrazów wysokiej jakości działa tam, gdzie jest pacjent, a nie tylko w centrach danych.
Cytowanie: Noh, Y., Lee, S., Jin, S. et al. Lightweight SwiM-UNet with multi-dimensional adaptor for efficient on-device medical image segmentation. Sci Rep 16, 5807 (2026). https://doi.org/10.1038/s41598-026-35771-4
Słowa kluczowe: segmentacja guza mózgu, AI w obrazowaniu medycznym, hybrydowe sieci neuronowe, wnioskowanie na urządzeniu, analiza 3D MRI