Clear Sky Science · pl
Warianty splicingowe KChIP1 modulują kanały Kv4, promując cechy inaktywacji typu P/C
Jak maleńkie pory kształtują elektryczny rytm mózgu
Każda myśl, pamięć i ruch w mózgu zależy od szybkich sygnałów elektrycznych w komórkach nerwowych. Sygnały te są precyzyjnie regulowane przez mikroskopijne pory — kanały jonowe — które pozwalają na przepływ naładowanych cząstek. Niniejszy artykuł bada, jak subtelne warianty białka pomocniczego KChIP1 mogą dramatycznie zmieniać zachowanie jednej z rodzin tych kanałów (Kv4), przesuwając podatność neuronów do wywoływania powtarzających się wybuchów aktywności elektrycznej.
Kanały potasowe jako hamulec mózgu
Kanały Kv4 przewodzą tzw. prąd potasowy typu A, który włącza się i wyłącza szybko w ciele komórki i jej rozgałęzieniach. Ten prąd pomaga ustalać, jak łatwo neuron wyzwala impulsy i jak wiernie może śledzić napływające sygnały, zwłaszcza przy niskich częstotliwościach wyładowań. Kanały Kv4 nie działają samodzielnie: montują się z białkami pomocniczymi w kompleksie trójskładnikowym, obejmującym białka DPP i KChIP. Partnerzy ci wpływają na to, jak szybko kanały się zamykają i jak szybko są gotowe do ponownego otwarcia. Do tej pory większość badań sugerowała, że KChIP zwykle przyspieszają odzyskiwanie kanałów Kv4 po ich wyłączeniu, umożliwiając neuronom szybkie reagowanie na powtarzane sygnały.
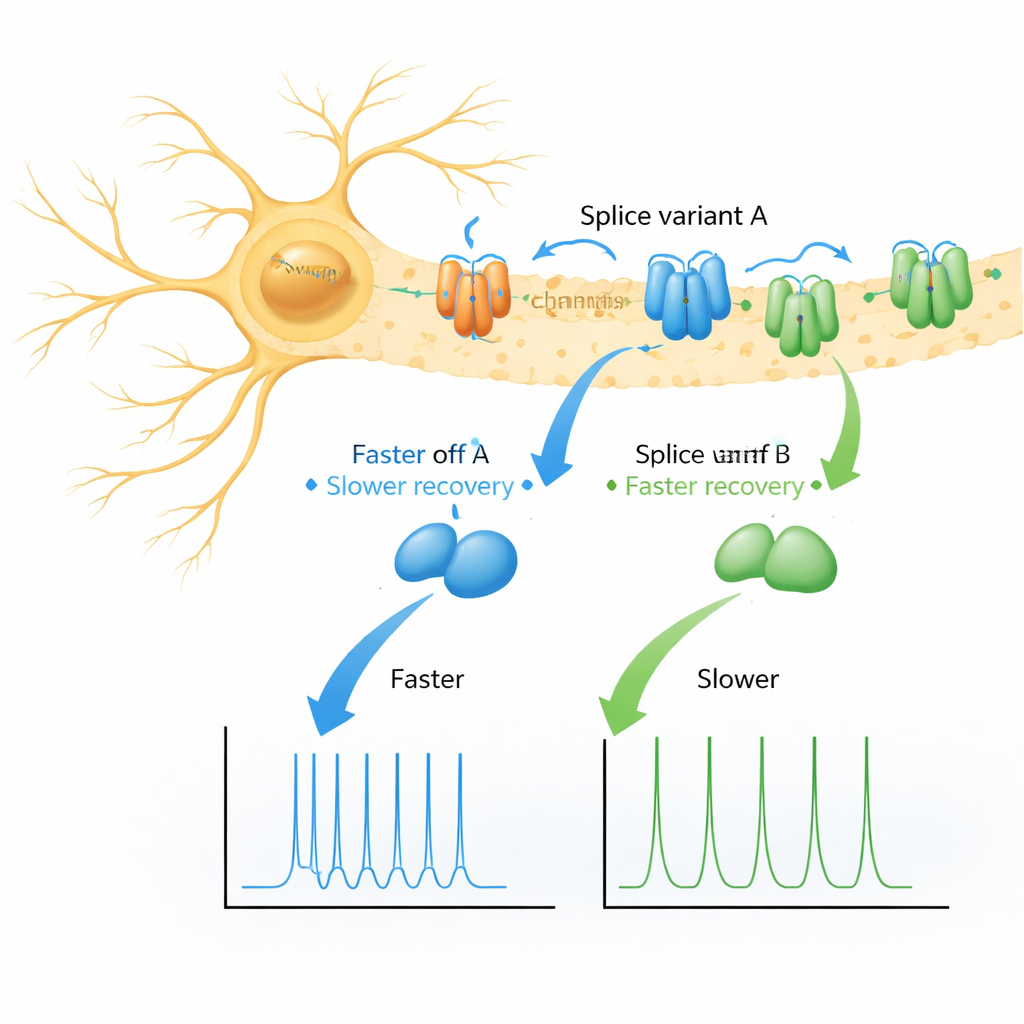
Dwa warianty białka, dwa sposoby odzyskiwania
Autorzy skupili się na dwóch niemal identycznych wersjach (wariantach splicingowych) KChIP1, nazwanych 1a i 1b, które różnią się jedynie krótkim aromatycznym „ogonkiem” na początku 1b. Używając komórek jajowych żaby jako kontrolowanego modelu eksperymentalnego, wyrażali kilka typów kanałów Kv4 osobno, z każdym wariantem KChIP1, z DPP lub z obiema pomocnicami jednocześnie. Jak można się było spodziewać, zarówno 1a, jak i 1b delikatnie zmieniały sposób, w jaki kanały wyłączały się podczas skoku napięcia, nie powodując spektakularnych efektów. Zaskoczenie pojawiło się przy badaniu odzyskiwania po wyłączeniu: zamiast jednorodnego, gładkiego powrotu do stanu gotowości, kanały w parze z 1a lub 1b wykazywały dwa odrębne etapy odzyskiwania — szybki i znacznie wolniejszy — przy czym wolna droga była znacznie wyraźniejsza dla 1b.
Ujawniona ukryta, wolna ścieżka
Gdy kanały Kv4 były wyrażane bez KChIP1, odzyskiwały się prostą, szybką ścieżką, a DPP jeszcze to przyspieszał. Dodanie KChIP1 zmieniło ten wzorzec. W obecności 1a większość kanałów nadal odzyskiwała się szybko, ale niewielka część obracała się poprzez powolny objazd z powrotem do stanu gotowości. W przypadku 1b znacznie większa frakcja wchodziła w tę wolną drogę, wydłużając odzyskiwanie do skali sekund. Efekt ten zaobserwowano we wszystkich testowanych podtypach Kv4 i utrzymywał się nawet przy obecności DPP, co sugeruje, że wolna ścieżka jest wbudowaną cechą kompleksów zawierających KChIP1, a nie artefaktem konkretnego kanału czy ustawienia eksperymentalnego. Autorzy zauważyli także, że 1b przesunął zakres napięć „wyłączających” kanały w kierunku bardziej ujemnych wartości, jeszcze bardziej predysponując je do bycia niedostępnymi podczas trwającej aktywności.
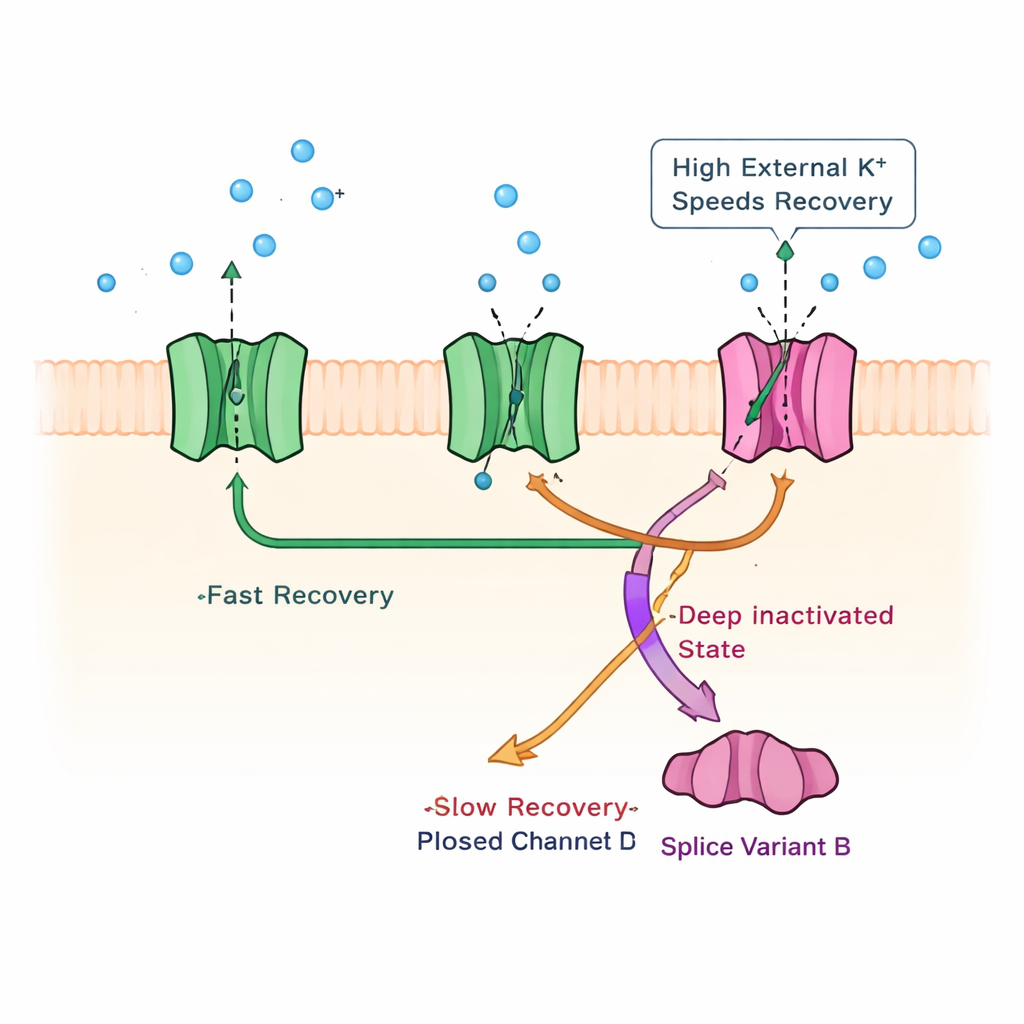
Odkrycie uśpionego mechanizmu inaktywacji
Aby ustalić, jaka fizyczna zmiana w kanale leży u podstaw tego wolnego odzyskiwania, zespół przebadał znane mechanizmy inaktywacji z innych kanałów potasowych. Wykluczyli klasyczny mechanizm „kula-i-łańcuch” przy zewnętrznym ujściu kanału, odcinając część wewnętrznego ogona kanału; faza wolna utrzymywała się. Następnie zastosowali wysokie stężenia jonów potasu na zewnątrz, trick znany z modyfikowania inaktywacji opartej na porze w innych kanałach. W tych warunkach zamykanie prądu stało się szybsze, ale co istotne, sama wolna faza odzyskiwania przyspieszyła specyficznie, jakby wysokie potas uwalniało kanały z głębokiego, długotrwałego stanu zablokowania. Celowe mutacje w segmencie bramkującym kanału dodatkowo potwierdziły ideę, że KChIP1b promuje inaktywację zlokalizowaną w porze — normalnie słabą w kanałach Kv4 — współistniejącą z ich zwykłą, szybszą inaktywacją w stanie zamkniętym.
Dlaczego to ma znaczenie dla aktywności mózgu
Wyniki sugerują, że poprzez wybór między KChIP1a, KChIP1b lub ich mieszankami neurony mogą precyzyjnie dostroić, jak szybko prądy typu A odzyskują gotowość między impulsami. W komórkach bogatych w KChIP1b znaczna część kanałów Kv4 zostaje „zaparkowana” w głębokim, wolno odwracalnym stanie inaktywacji, ograniczając ich dostępność podczas szybkiego wyładowywania. Może to pozwolić niektórym interneuronom — komórkom, które koordynują i hamują aktywność w obwodach mózgowych — na wyładowywanie się z wyższą częstotliwością lub z odmiennymi wzorcami czasowymi. W istocie, mała różnica splicingowa w jednym białku pomocniczym odblokowuje ukryty tryb hamowania w kanałach potasowych, dodając nową warstwę elastyczności do sposobu, w jaki mózg kontroluje własne rytmy elektryczne.
Cytowanie: Cao, W., Tachtsidis, G. & Bähring, R. KChIP1 splice variants modulate Kv4 channels by promoting P/C-type inactivation features. Sci Rep 16, 2632 (2026). https://doi.org/10.1038/s41598-026-35770-5
Słowa kluczowe: Kanały potasowe Kv4, Warianty splicingowe KChIP1, Prąd typu A, Pobudliwość neuronów, Inaktywacja kanału