Clear Sky Science · pl
Rola receptora nikotynowego α7 acetylocholinowego w promowaniu polaryzacji makrofagów do fenotypu M2 w miejscach zapalenia
Jak nerwy pomagają uciszyć wymykające się spod kontroli zapalenie
Kiedy skaleczymy palec lub zwalczamy infekcję, nasz organizm uruchamia reakcję zapalną, by nas chronić. Jeśli jednak ta reakcja trwa zbyt długo, może uszkadzać zdrowe tkanki i prowadzić do chorób przewlekłych. W tym badaniu zbadano, jak specyficzny receptor „uspokajający” na komórkach odpornościowych, zwany receptorem nikotynowym α7 acetylocholiny (α7nAChR), pomaga przesuwać odpowiedź zapalną w stronę gojenia zamiast szkody, co daje wskazówki do nowych terapii w chorobach takich jak sepsa, choroby jelit czy artretyzm.
Dwie twarze układów sprzątających układu odpornościowego
Makrofagi to komórki odpornościowe pełniące rolę ekipy sprzątającej i naprawczej. Mogą przełączać się między dwoma głównymi trybami. W trybie „atakującym”, często określanym jako M1, wydzielają agresywne związki, by zabijać drobnoustroje i usuwać szczątki. W trybie „leczącym”, znanym jako M2, wypuszczają sygnały łagodzące, które wyciszają zapalenie i sprzyjają naprawie tkanek. Prawidłowa odpowiedź zaczyna się od przewagi komórek M1, a potem stopniowo przesuwa się ku M2, gdy zagrożenie mija. Autorzy chcieli sprawdzić, czy α7nAChR — receptor pierwotnie znany z roli w komunikacji nerwowej i w działaniu nikotyny w mózgu — również pomaga kierować makrofagi w stronę gojącego fenotypu M2 podczas zapalenia.
Nerwowe przełączenie w stronę gojenia
Aby to zbadać, badacze użyli myszy, które miały albo nie miały receptora α7nAChR, i wywołali zapalenie w jamie brzusznej na dwa sposoby: za pomocą składnika bakteryjnego (imitującego infekcję) oraz poprzez delikatne manipulacje jelitami (imitując uraz chirurgiczny bez zakażenia). Mierzono molekularne markery rozróżniające zachowania M1 i M2 oraz liczbę każdego typu makrofagów za pomocą cytometrii przepływowej. U myszy normalnych wczesna faza zapalenia dominowała przez sygnały M1, lecz w ciągu następnych jednego–dwóch dni pojawiły się markery M2, odzwierciedlając naturalne przesunięcie ku naprawie. U myszy pozbawionych α7nAChR jednak markery prozapalne były wyższe, markery gojenia niższe, a udział makrofagów M2 w obszarze zapalnym był stale zredukowany, przesuwając lokalną równowagę ku dominacji M1 i bardziej szkodliwemu stanowi.
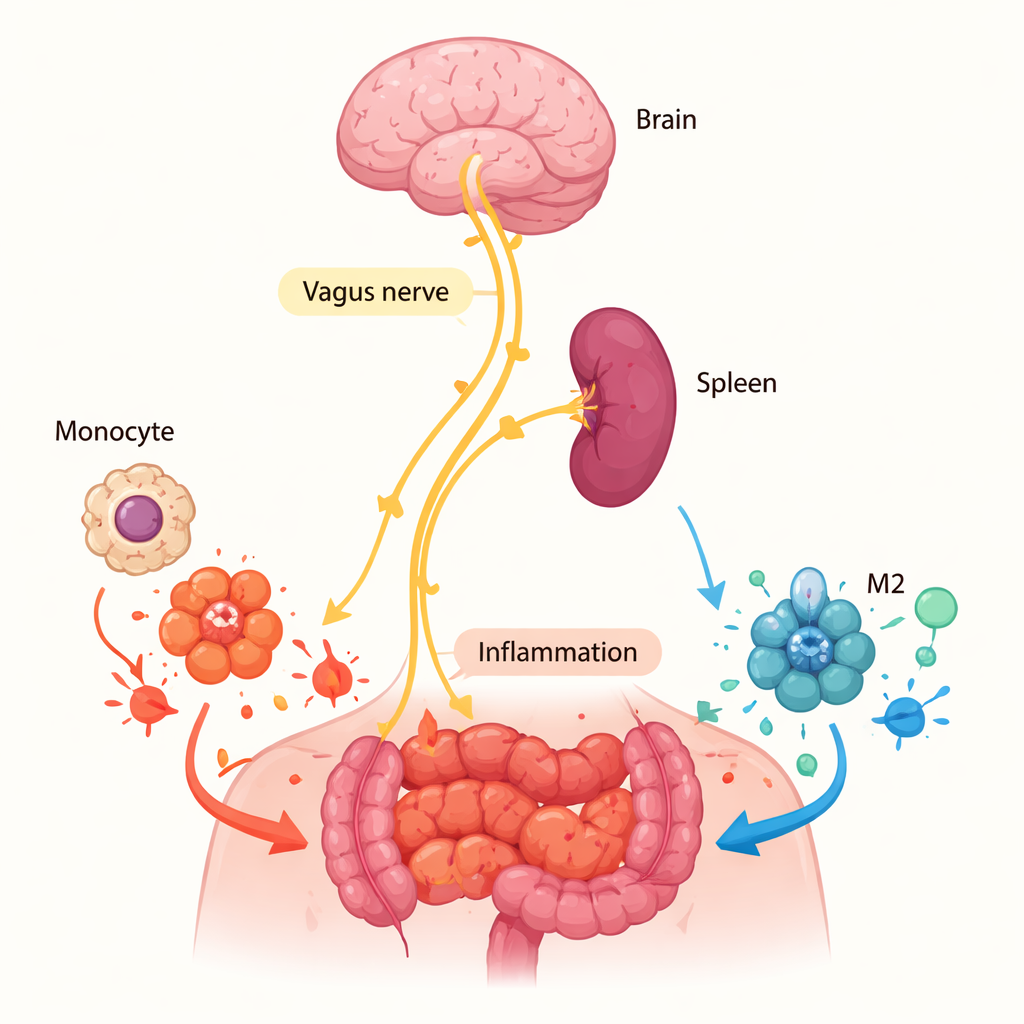
Dlaczego śledziona ma większe znaczenie niż rana
Zespół zapytał następnie, gdzie α7nAChR wykonuje tę pracę. Mógł działać bezpośrednio w miejscu zapalenia, gdyby lokalne komórki wydzielały acetylocholinę — związek aktywujący receptor. Pomiar acetylocholiny w płynie otrzewnowym i w hodowlach komórek z tkanki zapalnej dał jednak zasadniczo wynik ujemny, co przemawiało przeciw silnemu lokalnemu sygnałowi. Zamiast tego uwaga zwróciła się na śledzionę, kluczowy narząd odpornościowy już wcześniej powiązany z „cholinergiczną ścieżką przeciwzapalną” kontrolowaną przez nerw błędny. Gdy badacze chirurgicznie usunęli śledzionę u myszy normalnych, a następnie wywołali zapalenie otrzewnej, udział makrofagów M2 w jamie otrzewnej spadł, a ogólna liczba makrofagów zmalała. Wzorzec ten powielał obserwacje u myszy pozbawionych α7nAChR, co sugeruje, że sygnały nerwowe działające w śledzionie „przygotowują” monocyty — prekursorowe komórki makrofagów — do stania się komórkami M2 zanim te dotrą do zapalonej tkanki.
Testowanie przełącznika w komórkach ludzkich
Aby sprawdzić, czy ten sam receptor potrafi modulować komórki ludzkie, naukowcy użyli monocytów hodowlanych z linii białaczkowej (THP-1) oraz z oddanej krwi ludzkiej. Ukierunkowali te komórki, aby rozwinęły się w makrofagi typu M1 lub M2 za pomocą standardowych sygnałów immunologicznych, a następnie dodali specyficzny lek aktywujący α7nAChR. W obu źródłach ludzkich komórek włączenie α7nAChR nie zwiększało markerów M1, ale wyraźnie podnosiło kluczowe cechy zachowania M2, w tym białko powierzchniowe CD206 oraz przeciwzapalną interleukinę-10. Eksperymenty te wspierają koncepcję, że α7nAChR działa jak przełącznik preferencyjny, ułatwiając rozwijającym się makrofagom przyjęcie tożsamości naprawczej, bez całkowitego wyłączania odpowiedzi immunologicznej.
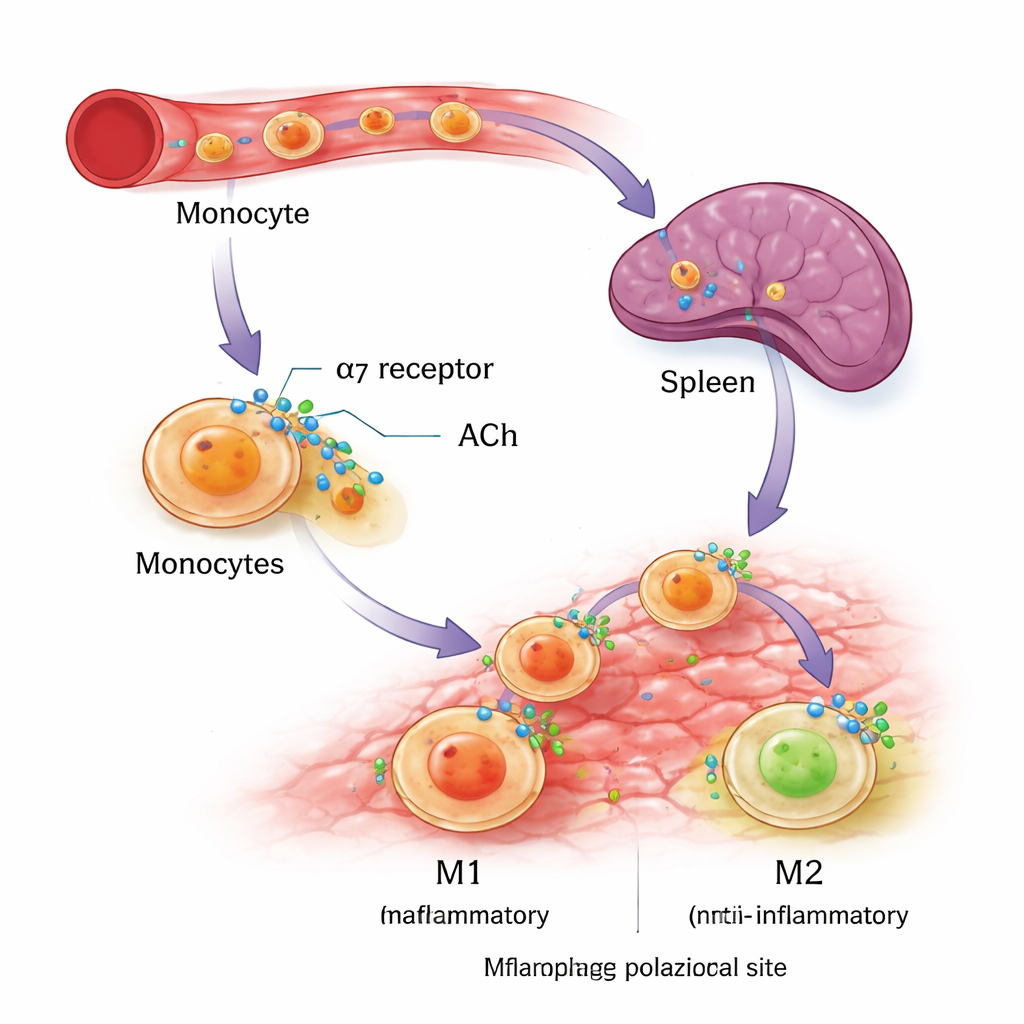
Od wskazówek związanych z nikotyną do przyszłych terapii
Wyniki pomagają wyjaśnić kilka zagadkowych obserwacji, takich jak to, dlaczego stymulacja nerwu błędnego może poprawiać przebieg chorób zapalnych i dlaczego palacze, mimo wielu zagrożeń zdrowotnych, wydają się mieć nieco niższe ryzyko niektórych schorzeń jelitowych — nikotyna aktywuje α7nAChR. Zamiast jedynie blokować związki prozapalne, α7nAChR wydaje się pomagać organizmowi przekształcać ekipy sprzątające układu odpornościowego w bardziej ukierunkowane na naprawę komórki M2, szczególnie poprzez „szkolenie” monocytów w śledzionie. Dla laika oznacza to, że nasz układ nerwowy robi więcej niż odczuwa ból czy kontroluje mięśnie; cicho instruuje także komórki odpornościowe, kiedy mają walczyć, a kiedy leczyć. Nauczenie się bezpiecznego przełączania tego wbudowanego mechanizmu za pomocą leków lub celowanej stymulacji nerwowej może otworzyć nowe drogi do łagodzenia szkodliwego zapalenia przy jednoczesnym zachowaniu zdolności obronnych organizmu.
Cytowanie: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Słowa kluczowe: polaryzacja makrofagów, zapalenie, nerw błędny, receptor nikotynowy acetylocholiny, regulacja odporności