Clear Sky Science · pl
Fizjologicznie relewantne formy radioaktywnych śledzików Tc- i Re-pirofosforanowych oraz podstawa ich czułości względem amyloidu transthyretyny
Dlaczego ta historia obrazowania serca ma znaczenie
Wiele osób z wiekiem gromadzi w sercu utajone złogi źle sfałdowanych białek, zwane amyloidami. Niektóre z tych złogów, szczególnie te utworzone z krwiowego białka nazwanego transthyretyną, mogą usztywniać serce i prowadzić do poważnych chorób. Lekarze coraz częściej polegają na radiznaczu znanym jako pirofosforan technetu‑99m (99mTc‑PYP), by zobaczyć te złogi w badaniach. A jednak, co zaskakujące, dokładna postać tego znacznika w organizmie i powód, dla którego „preferuje” pewne typy amyloidu, nie były jasne. Artykuł łączy teorię i eksperyment, aby odkryć, jak wygląda znacznik w warunkach przypominających organizm i w jaki sposób ta forma może kierować go ku szkodliwym włóknom transthyretyny.
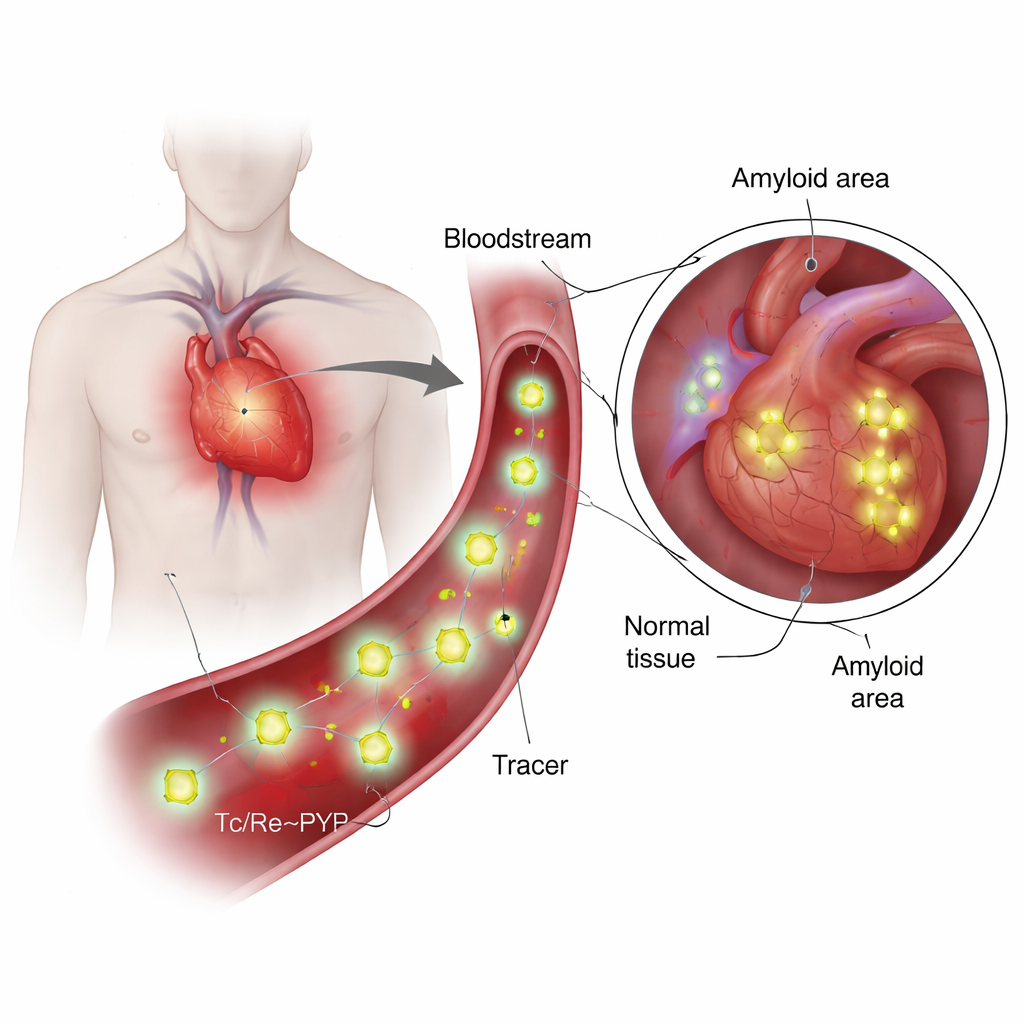
Co to są te śledziki i dlaczego są wyjątkowe?
99mTc‑PYP jest używany od dziesięcioleci do obrazowania kości, ponieważ ma skłonność do gromadzenia się tam, gdzie jest wysoka wymiana wapnia i minerałów. Ostatnio lekarze odkryli, że potrafi też rozróżniać dwa główne rodzaje kardiomiopatii amyloidowej: jedną zbudowaną ze łańcuchów lekkich przeciwciał (AL) i drugą z transthyretyny (ATTR). W ATTR serce często silnie „świeci” w badaniach PYP, podczas gdy przypadki AL zwykle pozostają słabe, nawet gdy nagromadzenie wapnia wygląda podobnie. Ta niezgodność postawiła kluczowe pytanie: czy znacznik przylega tylko do wapnia, czy też wchodzi w bezpośrednią interakcję z samym białkiem amyloidowym? Odpowiedź wymaga znajomości rzeczywistej struktury chemicznej znacznika w warunkach przypominających krew, czego wcześniejsze prace jedynie ogólnie zarysowały.
Użycie bezpieczniejszego zamiennika, żeby zobaczyć to, co niewidoczne
Ponieważ technet jest radioaktywny i występuje jedynie w śladowych ilościach w przygotowaniach medycznych, trudno go badać bezpośrednio wieloma technikami laboratoryjnymi. Autorzy użyli zatem renu, blisko spokrewnionego pierwiastka o niemal identycznym rozmiarze i preferencjach wiązań, ale bardziej wygodnej chemii, jako zamiennika. Przygotowali mieszaniny renu‑pirofosforanu w warunkach naśladujących kliniczne zestawy PYP, a następnie zbadali je szeregiem metod: zaawansowanymi obliczeniami kwantowymi, absorpcją w ultrafiolecie‑widzialnym, różnymi spektroskopiami drganiowymi (podczerwień i Raman), magnetycznym rezonansem jądrowym, spektrometrią mas oraz spektroskopią Mössbauera cyny. Razem te metody pozwoliły przetestować wiele kandydackich struktur i zawęzić, które gatunki prawdopodobnie występują przy obojętnym pH, podobnym do pH krwi.
Elastyczny, ale rozpoznawalny kształt molekularny
Zebrane dowody wskazują na wspólną „strukturę rdzeniową”: kompleks oktaedryczny, w którym atom technetu lub renu w stopniu utlenienia +4 jest związany z dwiema grupami pirofosforanowymi i dwiema cząsteczkami wody. Mówiąc prościej, metal siedzi w centrum niemal oktaedrycznej klatki utworzonej przez atomy tlenu, przy czym pirofosforany pełnią rolę kotwic z wieloma „ząbkami”, a wody zajmują pozostałe pozycje. Ta podstawowa jednostka diaqua dipirofosforanowa nie jest sztywna. Ponieważ ramiona pirofosforanowe mogą się skręcać i tworzyć wewnętrzne wiązania wodorowe z związanymi wodami, cząsteczka przyjmuje wiele nieco różnych kształtów w roztworze. Obliczenia i widma sugerują, że te wariacje przesuwają jej sygnatury absorpcji światła i drgań, wyjaśniając, dlaczego pasma eksperymentalne są szerokie i dlaczego wcześniejsze badania miały trudność z ustaleniem jednej, czystej struktury.
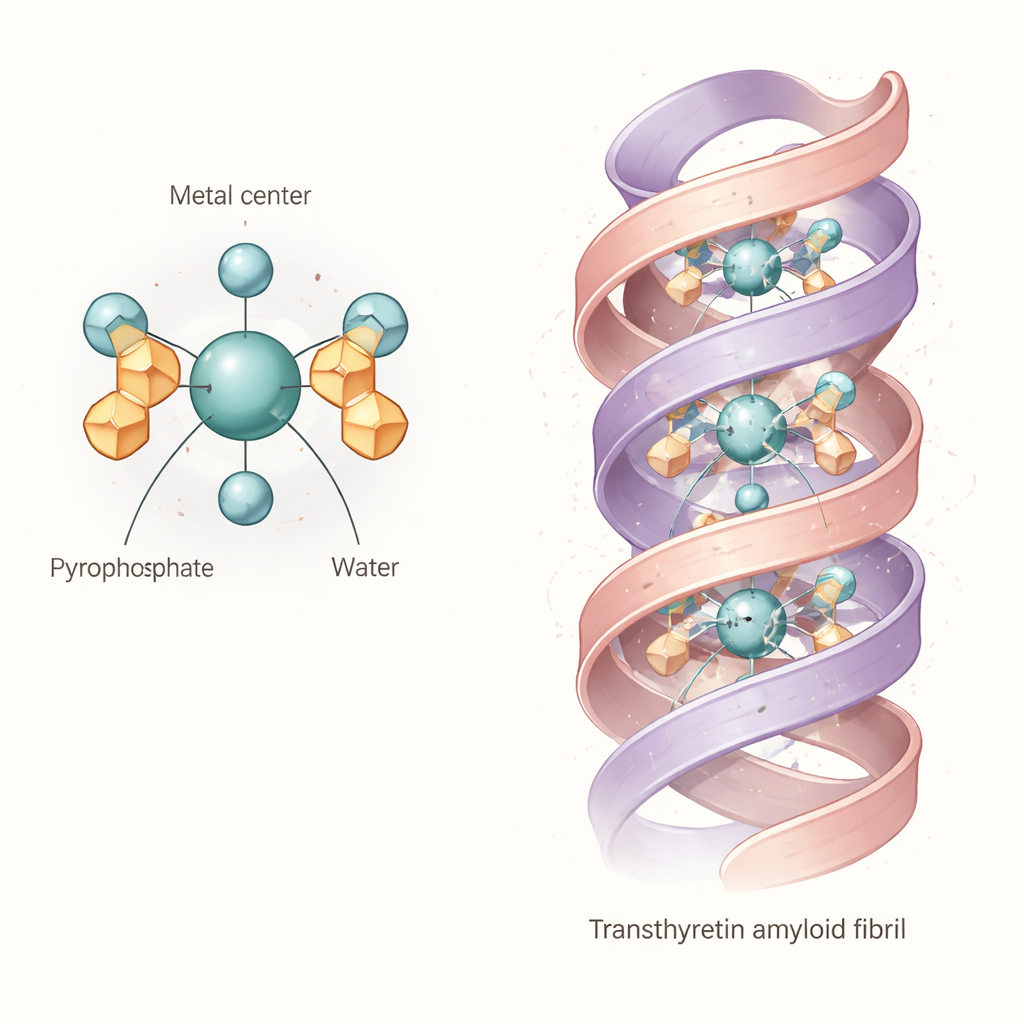
Co to oznacza dla wiązania z amyloidem serca
Następnie autorzy zapytali, czy ten elastyczny kompleks mógłby realnie zagnieździć się bezpośrednio we włóknach amyloidu transthyretyny. Wykorzystując szczegółową strukturę fibrila ludzkiej transthyretyny uzyskaną metodą krio‑elektronowej mikroskopii, przeprowadzili poszukiwania dokowania komputerowego z modelowanym kompleksem technetu‑pirofosforanu. Wyniki pokazują, że jednostka diaqua dipirofosforanowa może zmieścić się w centralnym kanale biegnącym wzdłuż fibrila, tworząc wielokrotne wiązania wodorowe i mostki solne z naładowanymi łańcuchami bocznymi wyściełającymi wnękę. Sugeruje to, że przynajmniej dla niektórych kształtów włókien transthyretyny, znacznik nie tylko znakują osady mineralne w pobliżu; może być zaciskany bezpośrednio przez białkowy szkielet. „Ustępliwość” struktury znacznika prawdopodobnie pomaga mu dopasować się do nieco różnych kieszeni i wzorców ładunków w fibrilach pochodzących od prawdziwych pacjentów.
Implikacje dla diagnostyki i przyszłych znaczników
Dla czytelnika nietechnicznego wniosek jest taki, że szeroko stosowane badanie serca PYP opiera się na znaczniku, który jest bardziej subtelny i „świadomy” białka, niż sądzono wcześniej. W warunkach fizjologicznych najlepiej myśleć o nim jako o małej, wodonośnej metalowo‑pirofosforanowej klatce, która może się zginać i tworzyć wiele punktów styku z kanałami amyloidu transthyretyny. Ta wnikliwość pomaga wyjaśnić, dlaczego znacznik daje silne sygnały w niektórych chorobach amyloidowych, a nie w innych, i dlaczego drobne zmiany w białku lub jego środowisku mogą powodować zagadkowe utraty czułości. Poprzez wyjaśnienie kształtu roboczego i wzorca ładunku znacznika, badanie tworzy podstawę do projektowania następnej generacji środków obrazujących lub terapeutycznych, które bardziej selektywnie rozpoznają chorobotwórcze włókna w sercu i poza nim.
Cytowanie: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Słowa kluczowe: amyloidoza serca, transthyretyna, pirofosforan technetu, obrazowanie molekularne, chemia radiznaczników