Clear Sky Science · pl
Synergistyczne działanie anty-persisterowe, hamujące pompowanie oraz przeciwbiofilmowe postbiotyków pochodzących od Lactobacillus pochwy przeciw UPEC: w kierunku nowej terapii zakażeń dróg moczowych
Dlaczego uporczywe zakażenia dróg moczowych mają znaczenie
Infekcje dróg moczowych (UTI) należą do najczęstszych zakażeń bakteryjnych, zwłaszcza u kobiet, i wiele osób doświadcza ich wielokrotnie mimo stosowania antybiotyków. W tym badaniu zbadano nowe, oszczędzające antybiotyki podejście do zwalczania tych uporczywych, nawrotowych infekcji: wykorzystanie pożytecznych bakterii pochwy i ich produktów metabolicznych, by powstrzymać kłopotliwego E. coli zanim się zadomowi, ukryje i odnowi.
Ukryci ocaleni stojący za nawrotami
Standardowe antybiotyki mogą zniszczyć większość bakterii, jednak mała subpopulacja znana jako „komórki persister” przetrwa, przechodząc w stan uśpienia o niskiej aktywności. Ci „śpiochy” nie są genetycznie oporne, lecz tolerują bardzo wysokie dawki antybiotyków i mogą się potem obudzić, powodując przewlekłe i nawrotowe UTI. Badacze pracowali z powszechnie występującym szczepem wywołującym UTI, E. coli UTI89, i pokazali, że silne antybiotyki takie jak kolistyna i meropenem łatwo wywołują powstawanie tych persisterów. W testach laboratoryjnych, odtwarzających warunki moczu, niewielkie ułamki populacji E. coli przetrwały ekstremalną ekspozycję na antybiotyki, potwierdzając, jak łatwo mogą pojawić się persistery i dlaczego standardowe schematy leczenia często nie zapewniają trwałej ulgi.
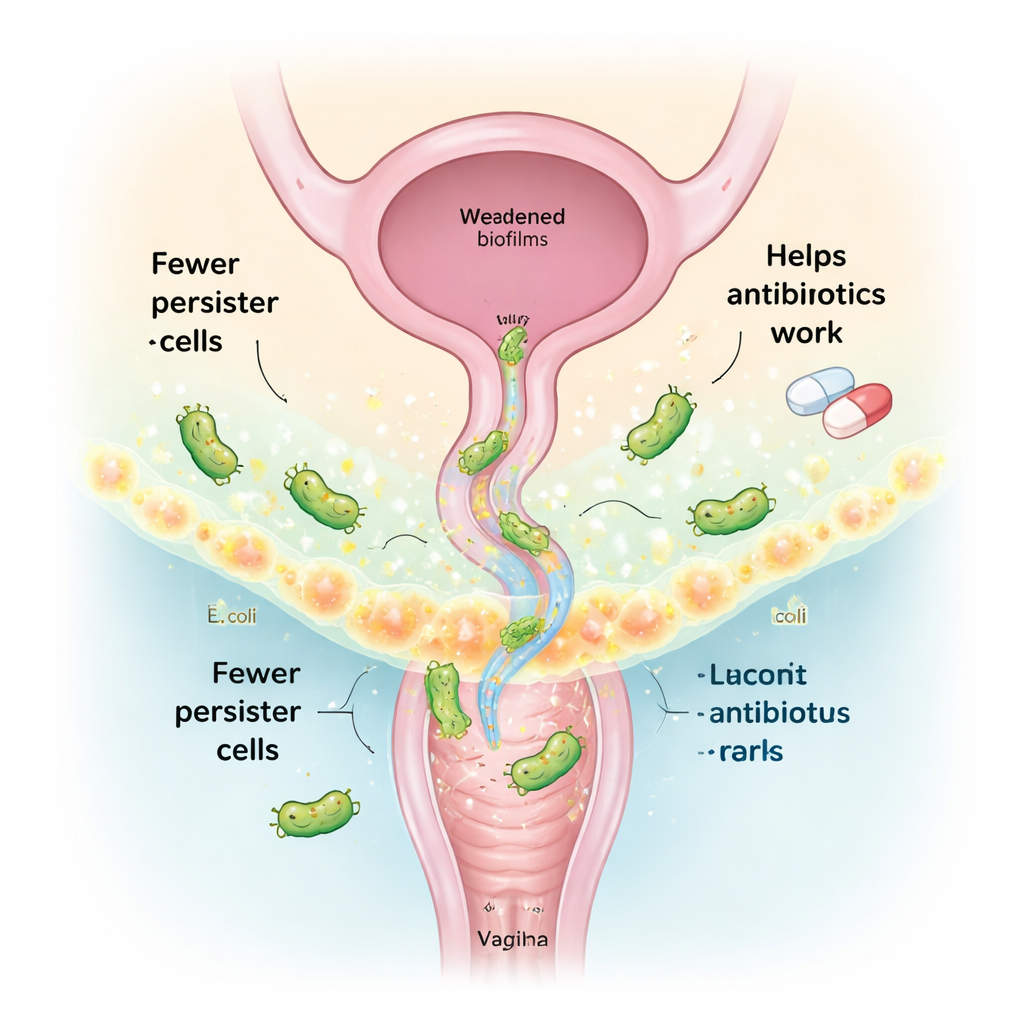
Przekształcanie przyjaznych bakterii pochwy w terapię
Zdrowa pochwa jest zwykle zdominowana przez gatunki Lactobacillus, które pomagają ograniczać szkodliwe mikroby. Zamiast używać żywych bakterii „probiotycznych”, w tym badaniu skupiono się na ich pozakomórkowym supernatancie — zasadniczo koktajlu cząsteczek, które wydzielają, zwanym postbiotykami. Z izolatów Lactobacillus pochodzących od zdrowych kobiet zespół wyodrębnił i przeanalizował te wydzielane związki. Dwa kluczowe metabolity, anhrydryt itakonowy i (−)-terpinen-4-ol, wyróżniły się zdolnością do współdziałania i znaczącego zmniejszania liczby komórek persister E. coli w połączeniu z antybiotykami. Trzeci związek, tryptamina, wcześniej wykazany jako rozkładający śluzową matrycę biofilmu, dodano, by wzmocnić działanie przeciwbiofilmowe.
Jak nowa mieszanka osłabia trudne do zabicia bakterie
Naukowcy stwierdzili, że cząsteczki pochodzące od Lactobacillus atakują persistery E. coli na kilku frontach jednocześnie. Po pierwsze, zwiększają produkcję reaktywnych form tlenu — chemicznie reaktywnych postaci tlenu, które uszkadzają składniki bakteryjne — czyniąc antybiotyki znacznie bardziej zabójczymi dla komórek w stanie uśpienia. Dodanie przeciwutleniaczy zmniejszyło ten efekt zabijania, podkreślając rolę stresu oksydacyjnego. Po drugie, związki te czynią zewnętrzne błony bakterii bardziej „przeciekającymi”, co pokazały barwniki fluorescencyjne wnikające do komórek łatwiej po leczeniu. Po trzecie, hamują „pompy efflux” komórek, maleńkie maszyny eksportujące, które normalnie wypychają antybiotyki z powrotem na zewnątrz. Przy zablokowanych pompach więcej leku zostaje wewnątrz bakterii i mniej persisterów przetrwa. W sumie te zmiany zmniejszyły uprzednio utworzone biofilmy E. coli nawet o dziesięć rzędów wielkości w testach laboratoryjnych, nie szkodząc przy tym komórkom układu odpornościowego ssaków w stosowanych dawkach.
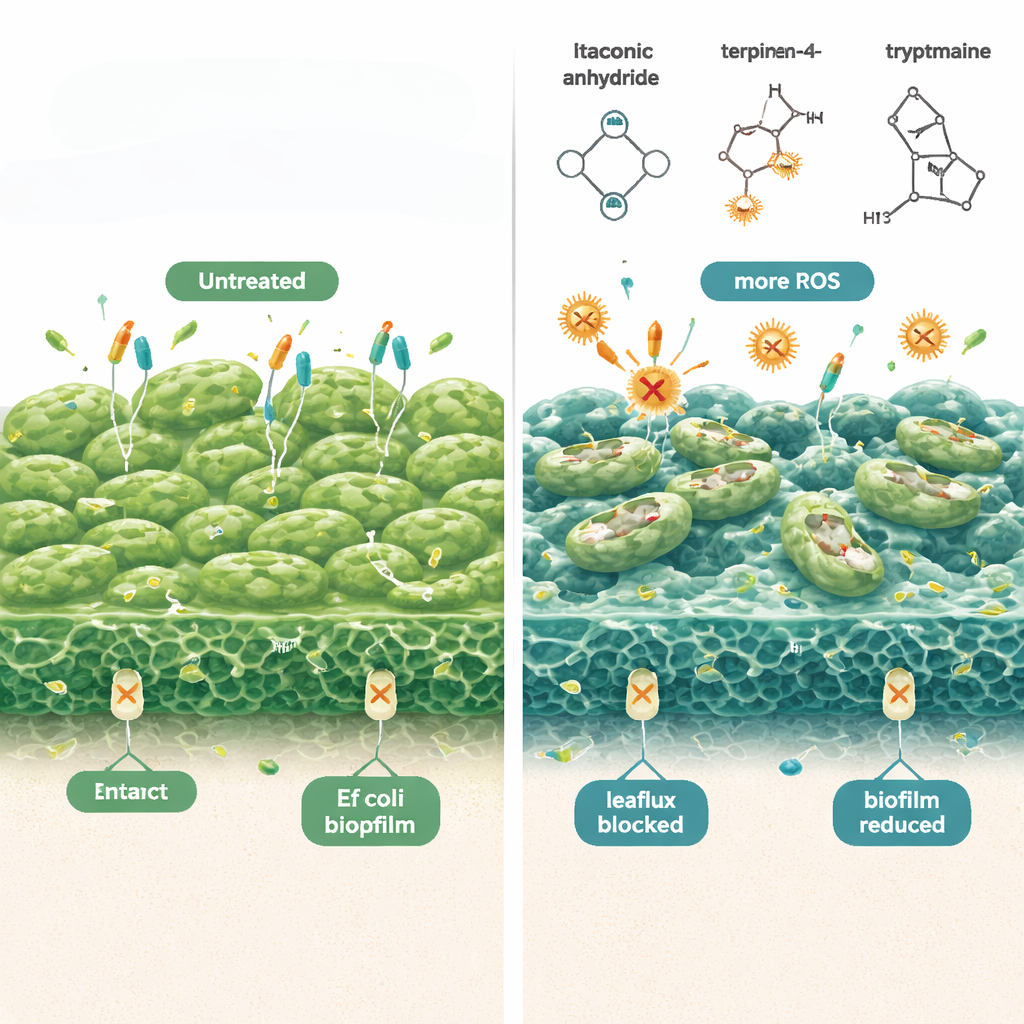
Z pracy w laboratorium do praktycznego płynu do irygacji pochwy
Aby przekształcić te wyniki w produkt użyteczny w codziennym życiu, zespół zaprojektował spersonalizowany płyn do irygacji pochwy wykorzystujący termoczułą żelową bazę zwaną poloksamerem 407. W temperaturze pokojowej zachowuje się jak ciecz dla łatwej aplikacji, a następnie łagodnie gęstnieje w temperaturze ciała, poprawiając kontakt ze ścianami pochwy. Żel niesie zdefiniowaną, bezpieczną kombinację anhydrydu itakonowego, (−)-terpinen-4-olu i tryptaminy. W płytkach laboratoryjnych formuła ta działała w zakresie wartości pH podobnym do warunków pochwy, silnie hamując tworzenie biofilmów E. coli i redukując liczbę żywych bakterii o około dziewięć rzędów wielkości. Pozostała stabilna i biologicznie aktywna przez co najmniej trzy miesiące w przechowywaniu w chłodzie oraz wykazała szerokie działanie przeciw innym problematycznym bakteriom, takim jak Klebsiella, MRSA i Pseudomonas.
Testowanie bezpieczeństwa i ochrony na myszach
Następnie badacze ocenili płyn w modelu myszy zakażonej E. coli w pochwie. Myszy zostały zainokulowane świecącym (znakowanym GFP) E. coli, a następnie leczone albo nowym płynem z metabolitami, płynem probiotycznym zawierającym żywe Lactobacillus, komercyjnym płynem do irygacji pochwy lub bazą placebo. Zwierzęta otrzymujące spersonalizowany płyn z metabolitami wykazały wyraźnie mniejsze zapalenie pochwy, utrzymanie masy ciała i dramatycznie niższe liczby bakterii w wydzielinie pochwowej w porównaniu z innymi grupami. Co najbardziej uderzające, u leczonych myszy nie wykryto E. coli w moczu, pęcherzu, nerkach ani tkance pochwy, a funkcja nerek pozostała prawidłowa, co wskazuje, że formuła nie tylko zmniejszyła miejscowe zakażenie, ale także zapobiegła rozprzestrzenieniu się do górnych dróg moczowych.
Co to może znaczyć dla osób z nawrotowymi UTI
Badanie konkluduje, że płyn do irygacji pochwy zbudowany z precyzyjnie dobranych metabolitów wytwarzanych przez naturalnie ochronne gatunki Lactobacillus może osłabić wywołującą UTI E. coli na wiele sposobów: zmniejszając populacje persisterów, zaburzając biofilmy i zwiększając skuteczność standardowych antybiotyków. Ponieważ podejście opiera się na nieżywych cząsteczkach, a nie na żywych bakteriach ani długotrwałych kursach leków systemowych, może być bezpieczniejsze, bardziej stabilne i łatwiejsze do regulacji. Chociaż wciąż potrzebne są badania na ludziach, płyn oparty na metabolitach wskazuje na przyszłość, w której nawrotowe UTI będą zapobiegane nie tylko silniejszymi antybiotykami, lecz także poprzez inteligentne wzmocnienie własnej mikrobiologicznej obrony organizmu u źródła.
Cytowanie: Nair, V.G., Chellappan, D.R., Durai, R.D. et al. Synergistic antipersister, efflux inhibitory & antibiofilm activities of vaginal Lactobacillus-derived postbiotics against UPEC: toward a novel therapeutic for utis. Sci Rep 16, 5005 (2026). https://doi.org/10.1038/s41598-026-35736-7
Słowa kluczowe: infekcja dróg moczowych, mikrobiom pochwy, postbiotyki Lactobacillus, tolerancja na antybiotyki, biofilmy bakteryjne