Clear Sky Science · pl
Vpr wirusa HIV wywołuje demetylację promotora antysensownego SNCA, prowadząc do upośledzenia funkcji poznawczych
Dlaczego HIV wciąż może wpływać na mózg
Ludzie żyjący z HIV dzięki nowoczesnym lekom antyretrowirusowym żyją dłużej i w lepszym zdrowiu. Mimo to wielu z nich wciąż ma problemy z pamięcią, koncentracją i ruchem, nawet gdy wirus we krwi jest dobrze kontrolowany. Badanie to przygląda się, dlaczego tak się dzieje, skupiając uwagę na małym białku wirusowym zwanym Vpr oraz na białku mózgowym — alfa‑synukleinie — które odgrywa kluczową rolę także w chorobie Parkinsona. Zrozumienie, jak te dwie cząsteczki oddziałują, może wyjaśnić, dlaczego HIV przyspiesza starzenie mózgu i zasugerować nowe sposoby jego ochrony.
Białko mózgowe na skrzyżowaniu HIV i Parkinsona
Alfa‑synukleina to białko, które pomaga komórkom nerwowym komunikować się, szczególnie w obszarach mózgu kontrolujących ruch i pamięć. Gdy alfa‑synukleiny jest za dużo, tworzy ona skupiska, które uszkadzają synapsy, obciążają mitochondria produkujące energię i napędzają zapalenie. Takie agregaty są cechą charakterystyczną choroby Parkinsona. Autorzy wykazują, że alfa‑synukleina gromadzi się także w związku z normalnym starzeniem u myszy, a białko Vpr wirusa HIV dodatkowo zwiększa jej poziomy w komórkopodobnych neuronach. To stawia alfa‑synukleinę na skrzyżowaniu między związanymi z HIV problemami poznawczymi a klasycznymi zaburzeniami ruchowymi.
Jak białko wirusowe przepisauje „interpunkcję” komórkową
Każda komórka używa chemicznych znaczników na DNA — często opisywanych jako molekularne znaki interpunkcyjne — aby włączać lub wyłączać geny. W tej pracy zespół skupił się na mało znanym przełączniku wewnątrz genu alfa‑synukleiny, zwanym promotorem antysensownym. W zdrowych komórkach ten przełącznik jest silnie znakowany grupami metylowymi, co utrzymuje go w stosunkowo cichej formie. Naukowcy odkryli, że Vpr usuwa te znaczniki w określonych miejscach tej domeny, proces znany jako demetylacja. Po usunięciu tych znaków promotor antysensowny staje się bardziej aktywny i pobudza nadprodukcję alfa‑synukleiny, co sprzyja powstawaniu szkodliwych agregatów.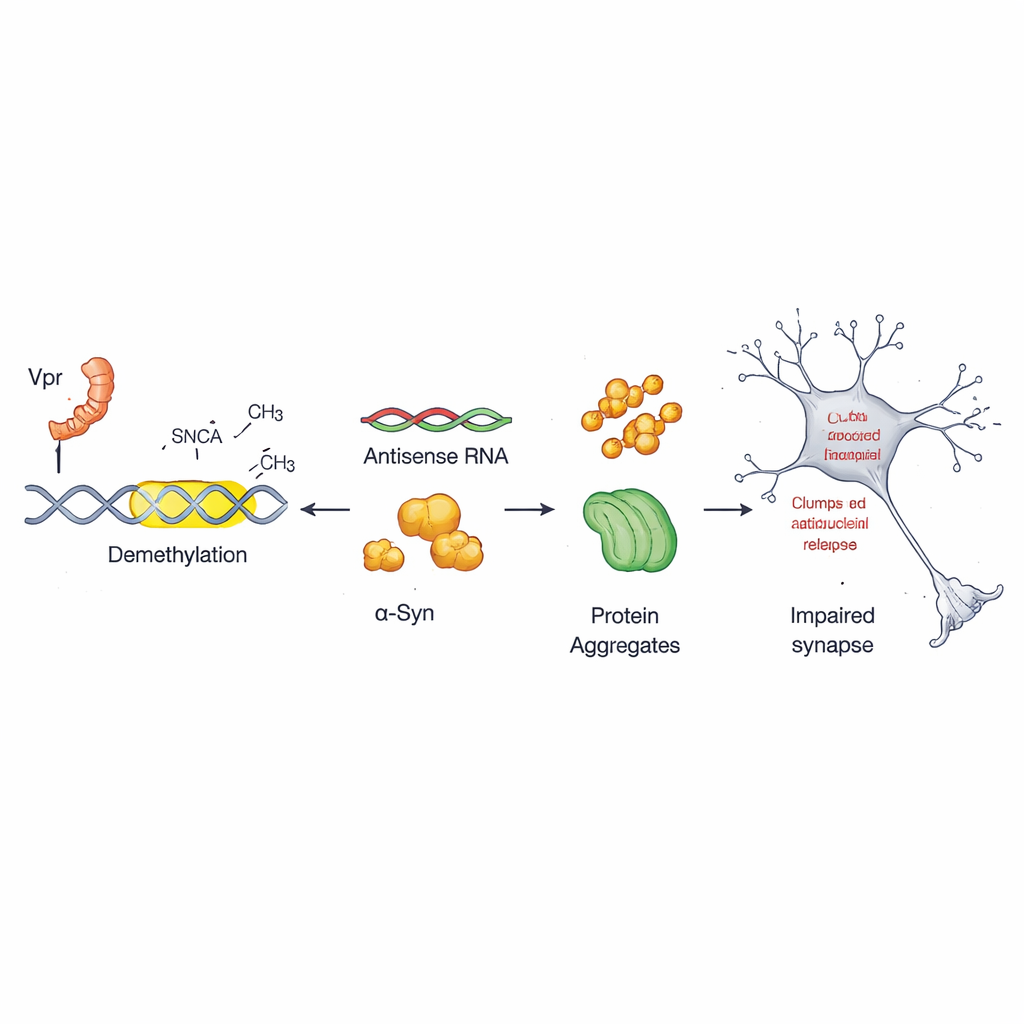
Dowody z komórek, myszy i ludzkich mózgów
Używając hodowanych ludzkich komórek o cechach neuronów oraz pierwotnych neuronów mysich, autorzy pokazali, że dodanie Vpr podnosi poziomy mRNA i białka alfa‑synukleiny w czasie. Lek, który szeroko promuje demetylację DNA, odtworzył część tych efektów, podkreślając rolę kontroli epigenetycznej. Natomiast związek o nazwie DMOG, który blokuje enzymy demetylujące, uniemożliwił Vpr pełne aktywowanie promotora antysensownego. Zespół sięgnął następnie po próbki ludzkiego mózgu od osób z HIV i bez niego. Mózgi dawców HIV‑dodatnich — zarówno przed leczeniem antyretrowirusowym, jak i po nim — miały mniej znaczników metylowych w tym samym regionie DNA oraz wyższe poziomy alfa‑synukleiny i jej transkryptu antysensownego, szczególnie u dawców z demencją związaną z HIV. Sugeruje to, że wirus pozostawia trwały ślad epigenetyczny w mózgu.
Od zmian molekularnych do problemów z pamięcią
Aby połączyć te molekularne zmiany z zachowaniem, badacze sprawdzili, jak Vpr wpływa na obwody mózgowe u myszy. Gdy zastosowali Vpr na plastrach hipokampa mysiego, regionu kluczowego dla pamięci, podstawowa siła sygnału między neuronami nie uległa zmianie, ale zdolność wzmacniania połączeń — proces zwany długotrwałym wzmocnieniem (long‑term potentiation) — była osłabiona. U żywych myszy celowane wstrzyknięcia Vpr do hipokampa prowadziły do gorszych wyników w zadaniu pamięci przestrzennej, w którym zwierzęta muszą zapamiętać położenie obiektów. Razem te eksperymenty sugerują, że zmiany alfa‑synukleiny wywołane przez Vpr to nie tylko ciekawostki biochemiczne; przekładają się one na osłabione synapsy i mierzalne deficyty pamięci.
Co to oznacza dla osób żyjących z HIV
Badanie proponuje jasny łańcuch zdarzeń: HIV uwalnia Vpr, Vpr przeprogramowuje kluczowy przełącznik DNA kontrolujący alfa‑synukleinę, białko gromadzi się i tworzy skupiska, a neurony stopniowo tracą zdolność do komunikacji i wspierania pamięci. Ponieważ podobne problemy z alfa‑synukleiną leżą u podstaw choroby Parkinsona, praca sugeruje, że HIV i klasyczne choroby neurodegeneracyjne mają nakładające się mechanizmy. Co ważne, wyniki wskazują możliwe nowe strategie — takie jak leki stabilizujące metylację DNA przy promotorze antysensownym lub ograniczające nagromadzenie alfa‑synukleiny — które mogłyby spowolnić lub zapobiec poznawczemu pogorszeniu i zaburzeniom ruchu związanym z HIV.
Cytowanie: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
Słowa kluczowe: zaburzenia neurokognitywne związane z HIV, alfa-synukleina, epigenetyka, metylacja DNA, objawy podobne do choroby Parkinsona