Clear Sky Science · pl
Racjonalne przeprojektowanie wysokoaktywnej DNAzymy G-kwadrupleksowej poprzez modyfikacje zasad w obrzeżach i pętlach
Małe maszyny DNA o dużym potencjale
Wyobraźmy sobie zastąpienie kruchych enzymów białkowych niewielkimi nićmi DNA, które przetrwają wysoką temperaturę, substancje chemiczne i szorstkie obchodzenie się, a mimo to będą prowadzić użyteczne reakcje chemiczne. Niniejsze badanie bada właśnie taką ideę. Naukowcy modyfikują specjalne struktury DNA, aby zachowywały się jak miniaturowe enzymy czyszczące, potrafiące wykorzystać nadtlenek wodoru do wygenerowania silnego sygnału. Te bardziej odporne, szybsze „maszyny” z DNA mogą sprawić, że przyszłe testy medyczne, czujniki środowiskowe i przenośne diagnostyki będą tańsze, bardziej niezawodne i prostsze w użyciu poza laboratoriem.
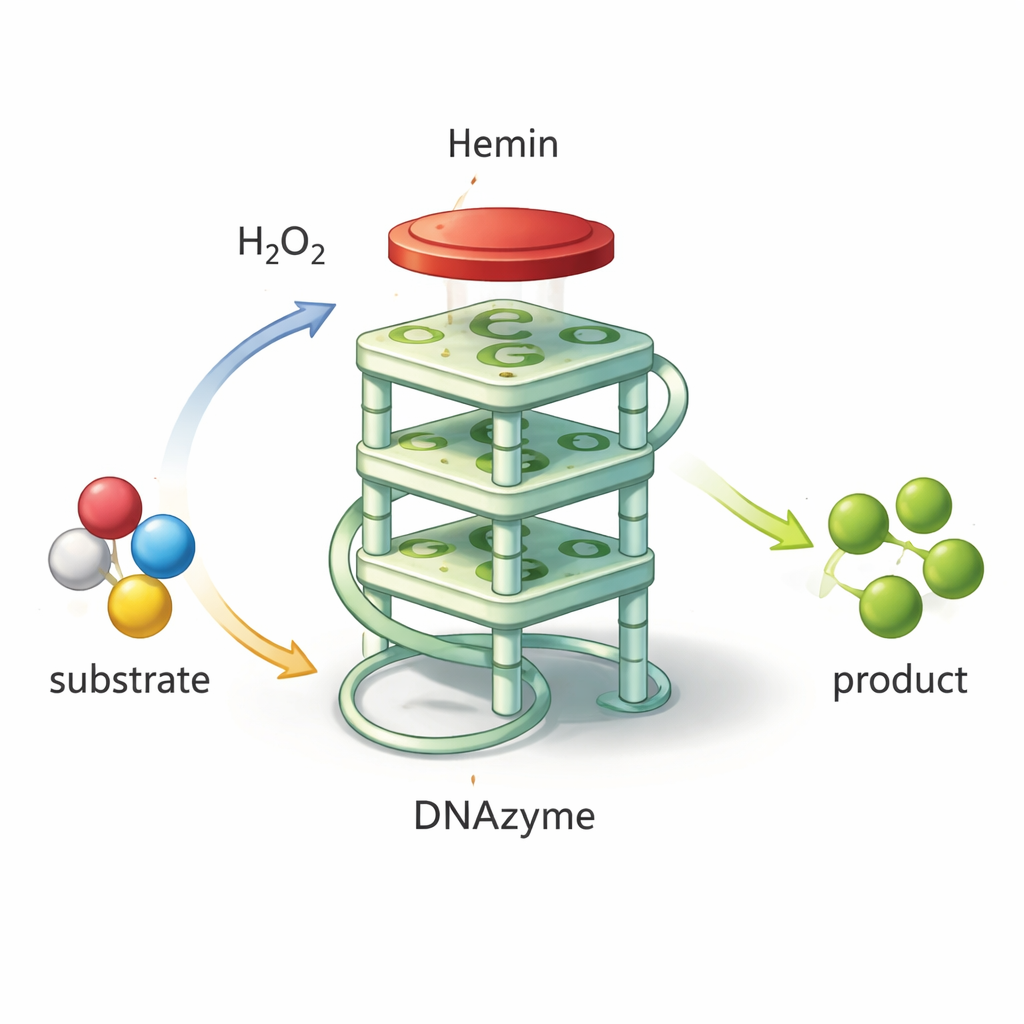
Przekształcanie DNA w maleńkie narzędzie chemiczne
Nie całe DNA jest tylko biernym nośnikiem informacji genetycznej. Niektóre krótkie sekwencje mogą składać się w nietypowe kształty, które chwytają określone cząsteczki lub nawet przyspieszają reakcje chemiczne. Jedną z takich form jest G-kwadrupleks, w którym bogate w guaninę fragmenty DNA tworzą zwarty, czterowarstwowy układ. Gdy mała cząsteczka zawierająca żelazo, zwana heminą, osiada na wierzchu tej struktury, para działa jak „DNAzyma”: katalizator oparty na DNA naśladujący naturalne peroksydazy. Może ona wykorzystać nadtlenek wodoru do utlenienia barwotwórczego związku, wytwarzając silny zielony sygnał łatwy do zmierzenia. Ponieważ takie DNAzymy są tanie w produkcji, wysoce stabilne i proste do przeprojektowania, stanowią obiecujący materiał budulcowy dla biosensorów wykrywających patogeny, toksyny lub markery chorób.
Dlaczego obecne enzymy DNA wymagają ulepszenia
Mimo obiecujących cech większość DNAzym nadal działa wolniej i mniej wydajnie niż naturalne enzymy białkowe. Istniejące biosensory często muszą wzmacniać cel metodami takimi jak PCR lub dodawać dodatkowe pomocnicze związki, co podnosi koszty i złożoność. Wcześniejsze próby poprawy DNAzym obejmowały łączenie dwóch jednostek DNA, trwałe przyłączanie heminy lub otaczanie miejsca reaktywnego dodatkowymi grupami chemicznymi. Te sztuczki czasami pomagają, ale mogą też wprowadzać objętość, która przeszkadza, lub wymagać złożonej chemii. Kluczowym pytaniem pozostawało, w jaki sposób proste zmiany pobliskich zasad DNA — zwłaszcza takich, które nie naruszają rdzenia G-kwadrupleksu — mogą przewidywalnie i „projektowalnie” regulować aktywność.
Przeprojektowanie wysoko wydajnej DNAzymy
Zespół skupił się na szczególnie aktywnej DNAzymie znanej jako B730, która już plasuje się wśród najlepszych niezmodyfikowanych katalizatorów G-kwadrupleksowych. Systematycznie zmieniali DNA tuż poza jej rdzeniem, dodając lub przestawiając powszechne zasady, takie jak adenina, tymina i cytozyna, w regionach pętli i ogona. Jedna z przeprojektowanych wersji, nazwana B730‑1.2, łączyła dodane adeniny w pętlach z krótką parą tymina–cytozyna na jednym końcu nici. W umiarkowanych warunkach nadtlenku wodoru ten wariant potroił początkową prędkość reakcji i w przybliżeniu poczwórzył całkowitą ilość barwnego produktu w porównaniu z oryginalnym B730. Wyraźnie przewyższał też dwie inne dobrze znane DNAzymy, AS1411 i CatG4, w testach porównawczych.
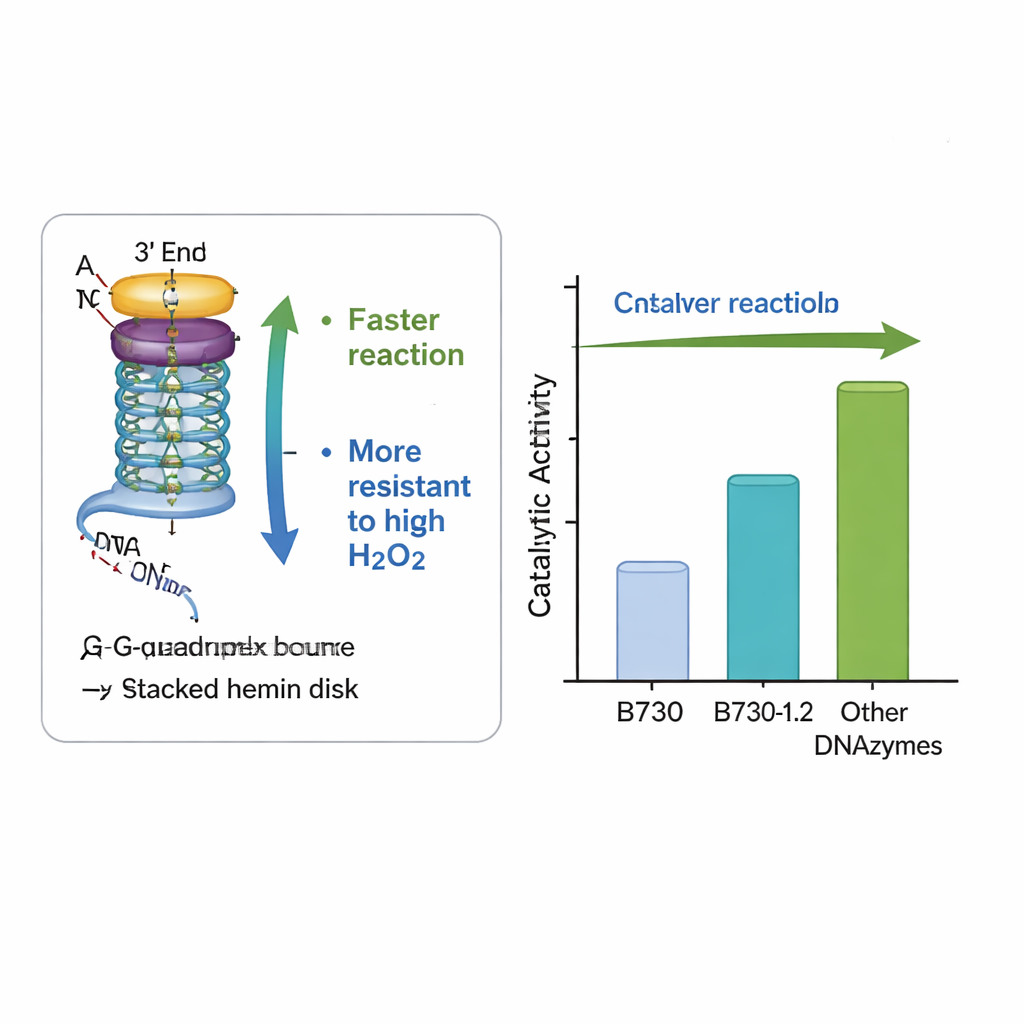
Zaprojektowane, by wytrzymać surowe warunki
Ważną praktyczną przeszkodą zarówno dla naturalnych, jak i sztucznych peroksydaz jest to, że wysokie stężenia nadtlenku wodoru — samego składnika napędzającego reakcję — mogą zniszczyć enzym i zatrzymać proces. Przeprojektowana DNAzyma B730‑1.2 wykazała niezwykłą odporność: utrzymywała, a nawet zwiększała aktywność przy poziomach nadtlenku, które zwykle inaktywują podobne systemy. Pomiary absorpcji światła potwierdziły, że zmodyfikowane DNA sprzyjało szybszemu powstawaniu kluczowego reaktywnego pośrednika — tak zwanego związku I (Compound I) — nie zaburzając przy tym ogólnego kształtu G-kwadrupleksu. Innymi słowy, subtelne zmiany w otaczających zasadach stworzyły bardziej korzystne lokalne warunki dla reakcji, przyspieszając użyteczne etapy i pomagając jednocześnie chronić centrum katalityczne przed autodestrukcją.
Co to oznacza dla przyszłych czujników
Dla osoby niebędącej specjalistą przekaz jest prosty: poprzez staranne dopracowanie zaledwie kilku „liter” po obu stronach już dobrego enzymu DNA, autorzy stworzyli wersję działającą szybciej i utrzymującą sprawność w trudniejszych warunkach. Ich strategia modyfikowania zasad w obrzeżach i pętlach oferuje prosty, niskokosztowy przepis na budowę wydajniejszych katalizatorów opartych na DNA bez uciekania się do złożonych modyfikacji chemicznych. Takie wytrzymałe, efektywne DNAzymy mogą stać w sercu testów następnej generacji i przenośnych urządzeń, które szybko zamieniają niewidoczne sygnały biologiczne — jak śladowe ilości wirusa czy zanieczyszczeń — w łatwo czytelne zmiany barwy.
Cytowanie: Adeoye, R.I., Babbudas, N., Birchenough, M. et al. Rational redesign of high-activity G-quadruplex DNAzyme through flanking and looping of nucleobases. Sci Rep 16, 5060 (2026). https://doi.org/10.1038/s41598-026-35686-0
Słowa kluczowe: DNAzyma G-kwadrupleksowa, mimetyk peroksydazy, biosensing, inżynieria aptamerów, kataliza nadtlenkiem wodoru