Clear Sky Science · pl
Badanie jonowych cieczy na bazie Acoramidisu jako potencjalnych stabilizatorów transthyretyny przy użyciu obliczeń DFT, dokowania molekularnego i badań ADMET
Dlaczego opracowanie tabletki na rzadką chorobę serca jest tak trudne
Amyloidoza transthyretynowa (ATTR) to poważna choroba, w której białko krwi odkłada się w sercu i nerwach, stopniowo je uszkadzając. Nowy lek, Acoramidis, może pomóc powstrzymać to odkładanie, ale istnieje praktyczny problem: lek słabo rozpuszcza się w wodzie, co utrudnia jego wchłanianie po podaniu doustnym. W pracy tej badano sprytne podejście polegające na przekształceniu Acoramidisu w nowe formy przypominające sole, zwane jonowymi cieczami, które mogłyby ułatwić przyjmowanie leku i zwiększyć jego skuteczność.
Przekształcenie obiecującego leku w formę nadającą się do spożycia
Aby tabletka zadziałała, najpierw musi rozpuścić się w wodnistych płynach żołądka i jelit, a następnie przejść przez ścianę jelita do krążenia. Acoramidis skutecznie stabilizuje białko transthyretynę (TTR), co pomaga zapobiegać szkodliwemu agregowaniu białek związanych z ATTR, lecz ma niską rozpuszczalność i słabą biodostępność po podaniu doustnym. Badacze postanowili rozwiązać ten problem, chemicznie łącząc Acoramidis z różnymi naładowanymi partnerami, tworząc trzy nowe wersje jonowych cieczy (IL1, IL2 i IL3). Wersje te zaprojektowano tak, by zachowywały się bardziej jak płynne sole niż sztywne kryształy, co potencjalnie poprawi rozpuszczalność i dystrybucję leku w organizmie. 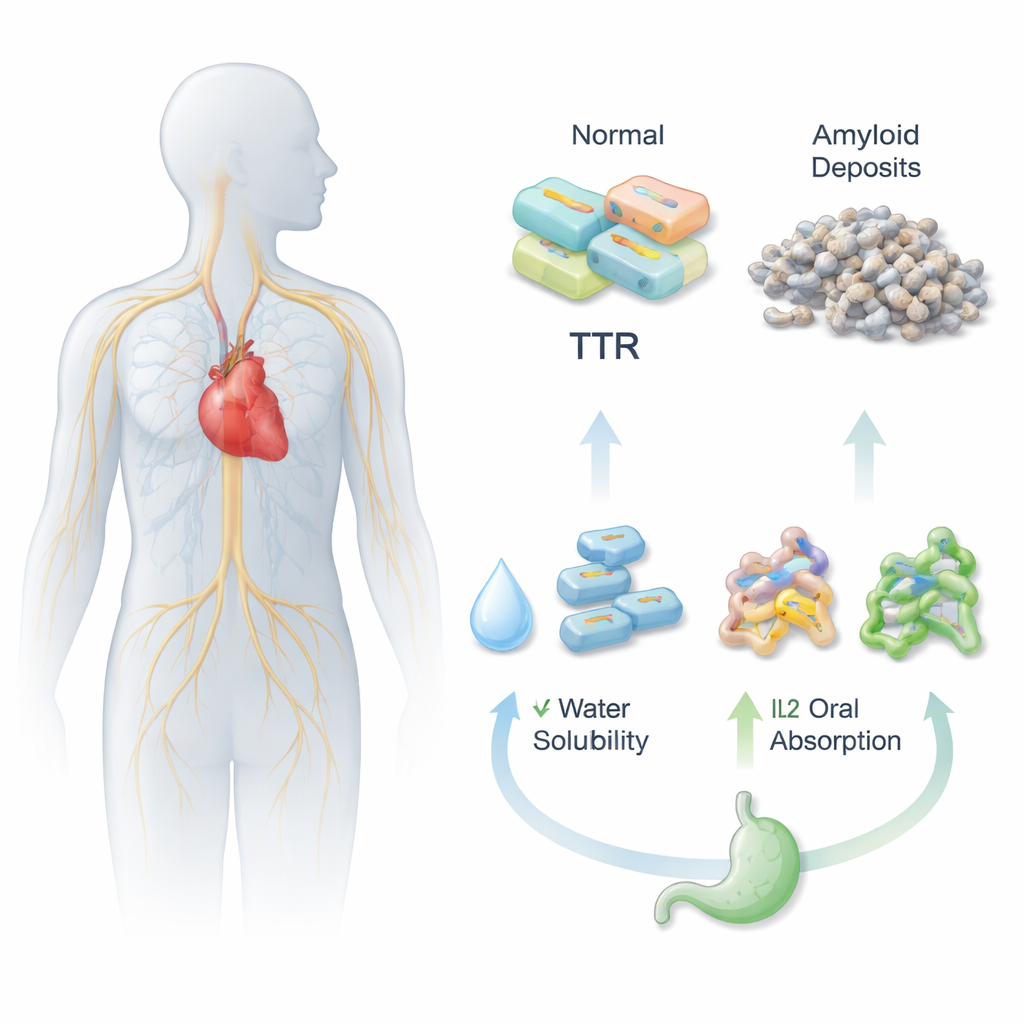
Badanie nowych cząsteczek za pomocą komputera
Zamiast od razu przechodzić do badań na zwierzętach czy ludziach, zespół użył zaawansowanych metod komputerowych, by przewidzieć zachowanie nowych form. Obliczenia chemii kwantowej oszacowały polarność każdej cząsteczki — kluczowy wskaźnik rozpuszczalności w wodzie — oraz łatwość przesunięcia elektronów, co wiąże się z potencjalnymi interakcjami z białkami. IL1 wyróżniał się największym momentem dipolowym i najsilniejszą reaktywnością elektronową, co sugeruje lepszą rozpuszczalność w wodzie i silniejsze, bardziej elastyczne oddziaływania z docelowymi białkami. Obliczenia energetyczne wskazały również, że IL1 jest bardziej stabilny termicznie niż lek wyjściowy i pozostałe dwie jonowe ciecze, co oznacza, że powinien być mniej podatny na rozpad zanim dotrze do miejsca działania.
Jak mocno lek może chwycić swój cel
Następnie badacze zastosowali dokowanie molekularne — wirtualny test „zamek-i-klucz” — aby sprawdzić, jak dobrze Acoramidis i jego trzy formy jonowe mieszczą się w kanale wiążącym białka TTR. Wszystkie cztery związki dokowały do właściwego regionu TTR, ale IL1 utworzył najszlachetniejsze wiązanie, z najkorzystniejszą energią wiązania i kilkoma stabilizującymi kontaktami — szczególnie wiązaniami wodorowymi — z kluczowymi aminokwasami białka. Silniejsze wiązanie sugeruje, że IL1 może być nawet lepszy niż związek rodzicielski w utrzymywaniu TTR w bezpiecznej, czterołańcuchowej strukturze, pomagając zapobiegać niebezpiecznemu rozpadowi i nieprawidłowemu pofałdowaniu prowadzącemu do złogów amyloidowych.
Czy organizm wchłonie i oczyści te nowe formy?
Na koniec zespół użył internetowych narzędzi farmakologicznych, by zbadać, jak organizm mógłby sobie poradzić z tymi związkami — jak dobrze się rozpuszczają, przechodzą przez ścianę jelita, krążą we krwi i są w końcu usuwane. Wszystkie trzy jonowe ciecze przewidywano jako bardziej rozpuszczalne w wodzie niż Acoramidis, przy czym IL3 wykazywał najwyższą surową rozpuszczalność. Wskaźniki przepuszczalności jelitowej i ogólnego wchłaniania doustnego poprawiły się dla wszystkich trzech jonowych cieczy, a IL1 i IL2 dały najlepszą równowagę pomiędzy przenikaniem przez jelito a przewidywaną biodostępnością. Wiązanie z białkami we krwi, szybkości klirensu i okresy półtrwania również uległy zmianom w sposób sugerujący, że formy jonowych cieczy mogłyby zapewnić bardziej stabilną ekspozycję po podaniu doustnym, przy czym IL1 ponownie wykazuje szczególnie korzystny profil. 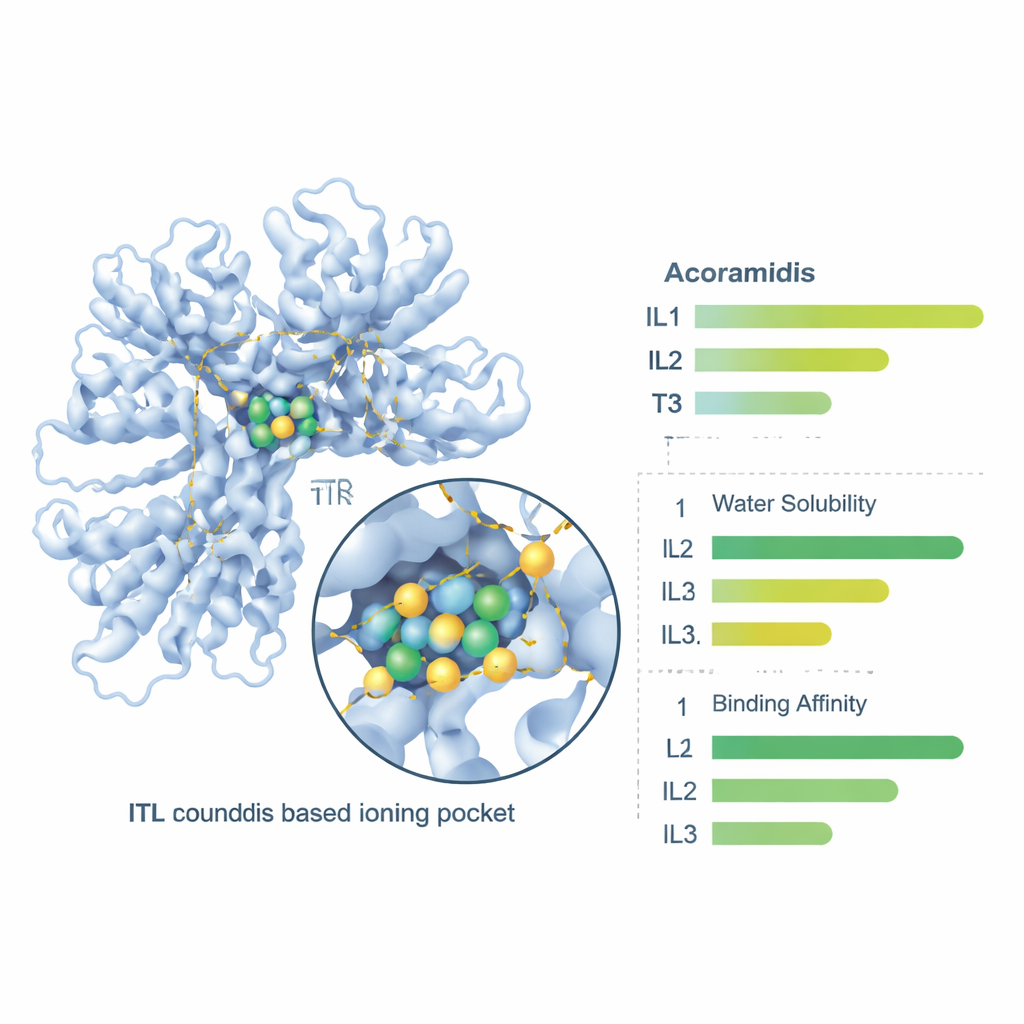
Co to może oznaczać dla przyszłych terapii ATTR
Dla czytelnika niebędącego specjalistą główny wniosek jest taki, że lek Acoramidis już wygląda obiecująco w leczeniu rzadkiej, lecz poważnej choroby serca i nerwów, jednak jego słaba rozpuszczalność ogranicza skuteczność w formie doustnej. Przekształcenie Acoramidisu w specjalnie zaprojektowane jonowe ciecze pokazuje — wyłącznie na podstawie testów komputerowych — że możliwe jest stworzenie wersji, które lepiej się rozpuszczają, silniej wiążą z docelowym białkiem i są wydajniej wchłaniane. Spośród trzech kandydatów IL1 wydaje się oferować najlepszą równowagę stabilności, siły wiązania, rozpuszczalności i przewidywanego doustnego wchłaniania, co czyni go silnym kandydatem do dalszych badań laboratoryjnych i klinicznych zmierzających do opracowania skuteczniejszych, łatwiejszych w stosowaniu terapii na ATTR.
Cytowanie: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
Słowa kluczowe: amyloidoza transthyretynowa, Acoramidis, jonowe ciecze, pofałdowanie białek, doustne podawanie leku