Clear Sky Science · pl
Projekt in silico wieloepitopowej szczepionki ukierunkowanej na DENV-1 i DENV-3
Dlaczego szczepionki przeciw dengi wciąż są istotne
Gorączka denga nie jest już rzadką tropikalną chorobą; stanowi obecnie zagrożenie dla miliardów ludzi w ponad 100 krajach i regularnie przeciąża szpitale w częściach Azji, Ameryki Łacińskiej i innych regionach. Mimo że na rynku są dwie zatwierdzone szczepionki, ochrona jest nierówna, zwłaszcza u osób, które nigdy wcześniej nie chorowały na dengę, oraz w regionach, gdzie jednocześnie krąży kilka typów wirusa. To badanie stawia aktualne pytanie: czy projektowanie wspomagane komputerowo może pomóc stworzyć bezpieczniejszą, bardziej precyzyjną szczepionkę, ukierunkowaną konkretnie na groźne współzakażenia dwoma typami dengi, które często występują razem?
Dwa podstępne typy wirusa i dlaczego stanowią problem
Wirus dengi występuje w czterech odmianach, zwanych serotypami DENV‑1 do DENV‑4. Zakażenie którymkolwiek z nich może powodować wysoką gorączkę, silny ból, a w niektórych przypadkach zagrażające życiu krwawienia lub wstrząs. Co niepokojące, ponowne zachorowanie spowodowane innym serotypem może czasami pogorszyć przebieg choroby zamiast go złagodzić, ponieważ istniejące przeciwciała mogą ułatwiać wejście nowego wirusa do komórek — zjawisko zwane wzmocnieniem zależnym od przeciwciał. W ostatnich ogniskach epidemii lekarze zgłaszali pacjentów zakażonych jednocześnie DENV‑1 i DENV‑3, kombinacją powiązaną z cięższym przebiegiem choroby i mylącymi wynikami testów. Obecne szczepionki nie zapewniają niezawodnej ochrony we wszystkich grupach wiekowych i przeciw wszystkim serotypom, szczególnie u osób bez wcześniejszej ekspozycji, co pozostawia niebezpieczną lukę w obronie.
Projektowanie szczepionki od poziomu molekularnego
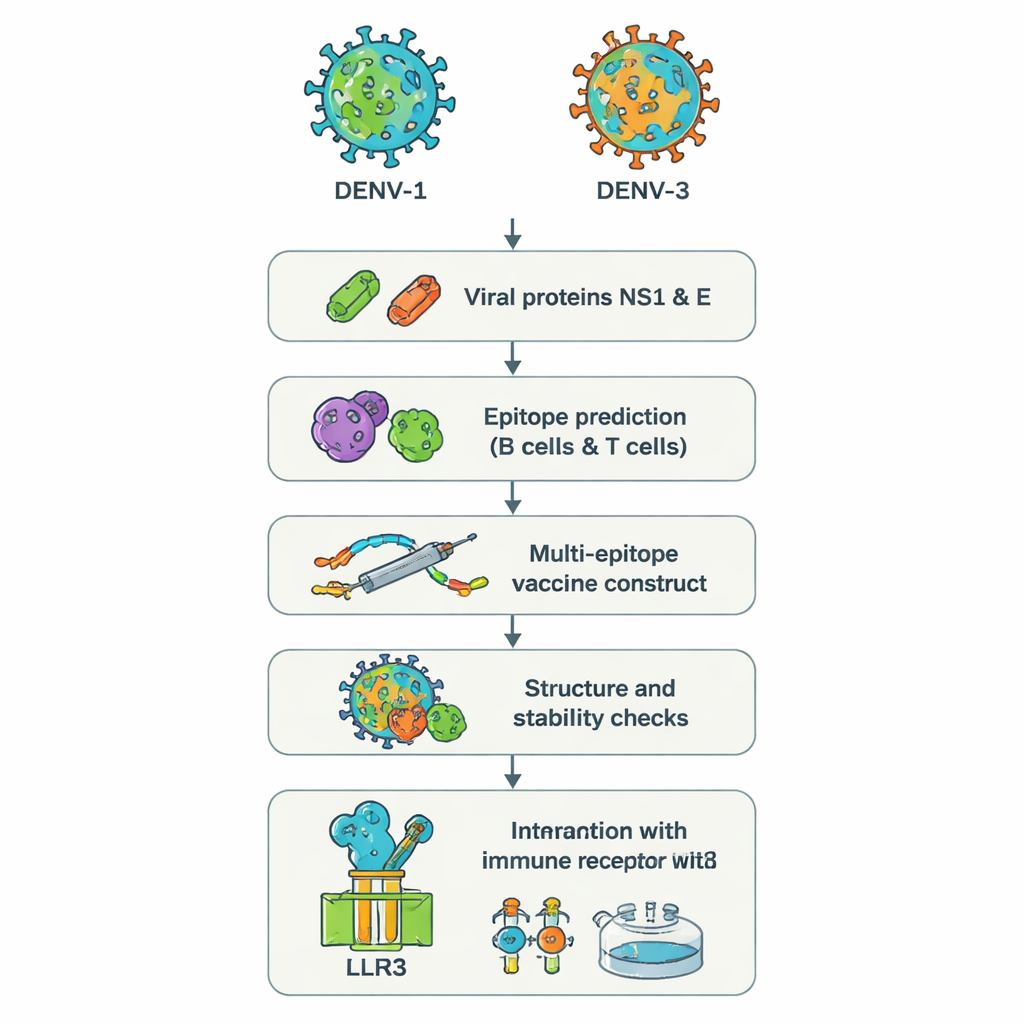
Zamiast hodować całe wirusy w laboratorium, badacze zastosowali podejście zwane czasem „odwrotną wakcynologią”. Wyszli od sekwencji genetycznych dwóch białek dengi, NS1 i E, z DENV‑1 i DENV‑3. Białka te odgrywają kluczową rolę w tym, jak wirus wnika do komórek i jak jest rozpoznawany przez układ odpornościowy. Potężne narzędzia internetowe przeskanowały sekwencje białek, aby zlokalizować krótkie odcinki — epitopy — które najprawdopodobniej zostaną rozpoznane przez ludzkie komórki B (produkujące przeciwciała) i T (niszczące zakażone komórki i koordynujące odpowiedź). Z setek kandydatów zespół wybrał mały zbiór przewidywanych jako wyraźnie widoczny dla układu odpornościowego, wspólny dla obu serotypów i zdolny do wywołania korzystnych sygnałów przeciwwirusowych, takich jak interferon‑gamma.
Budowa jednej wielofunkcyjnej cząsteczki szczepionkowej
Wybrane epitopy zostały następnie cyfrowo zszyte w jedną długą sztuczną cząsteczkę białka — „wieloepitopową” szczepionkę. Krótkie linkery aminokwasowe pełnią rolę elastycznych przestrzeników, dzięki czemu każdy epitope zachowuje swoją strukturę i pozostaje dostępny dla komórek odpornościowych. Dodatkowy fragment, oparty na naturalnym ludzkim peptydzie przeciwbakteryjnym zwanym beta‑defensyną, dodano jako adiuwant w celu wzmocnienia odpowiedzi. Analizy komputerowe przewidywały, że końcowa konstrukcja, zawierająca 575 aminokwasów, będzie stabilna, hydrofilowa (a więc łatwiejsza do rozpuszczenia) i mało prawdopodobna do wywoływania reakcji alergicznych. Kolejne narzędzia do przewidywania struktury wygenerowały model trójwymiarowy i sprawdziły, że większość elementów budulcowych znajduje się w realistycznych pozycjach, podobnych do tych obserwowanych w znanych strukturach białkowych.
Testowanie kandydata w wirtualnym organizmie
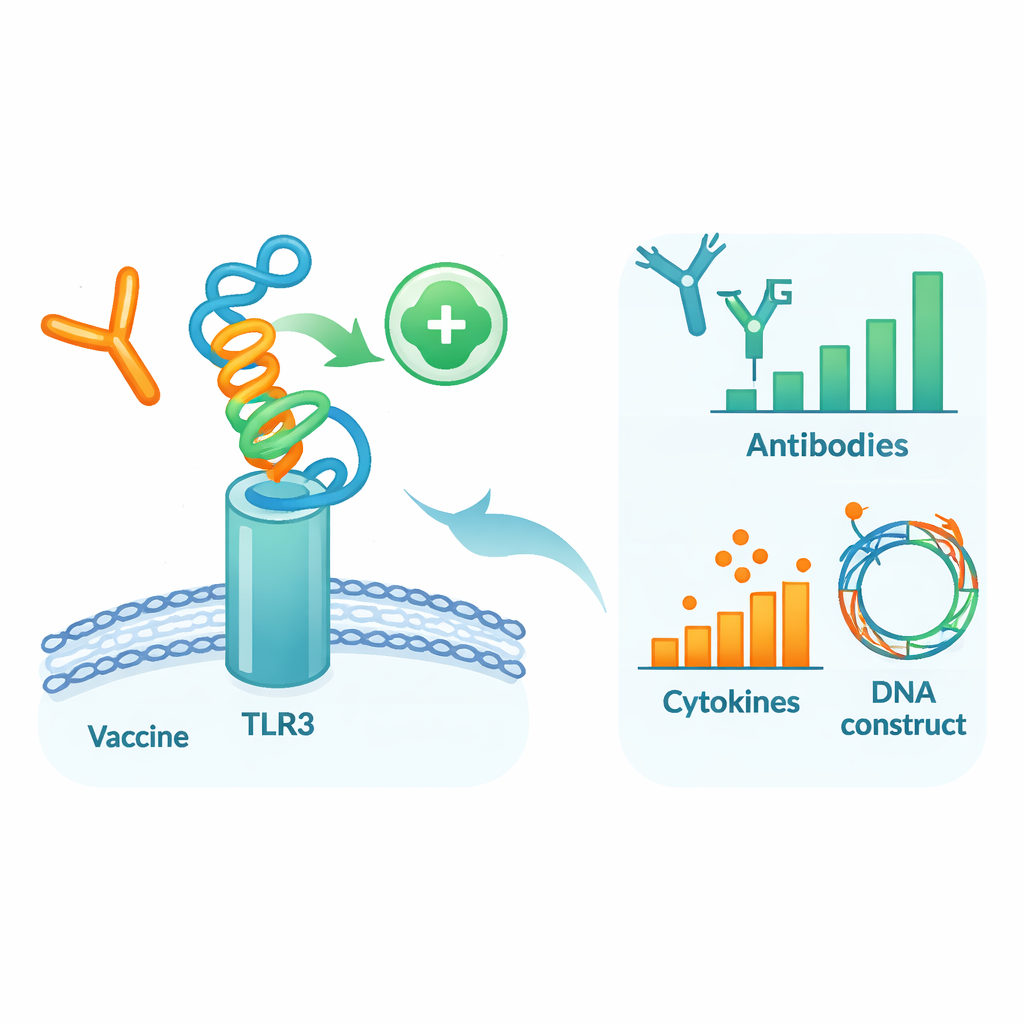
Aby sprawdzić, jak zaprojektowane białko może zachowywać się w środowisku przypominającym organizm ludzki, autorzy przeprowadzili serię szczegółowych symulacji komputerowych. Najpierw zadokowali model szczepionki do TLR3, białka‑sensora na komórkach odpornościowych, które wykrywa materiał wirusowy i pomaga uruchomić wczesne mechanizmy obronne. Symulacje dynamiki molekularnej — wirtualne filmy atomów w ruchu — sugerowały, że szczepionka i TLR3 tworzą stabilny kompleks, wspierany korzystnymi energiami wiązania i licznymi wiązaniami wodorowymi. Dodatkowe analizy ruchu i energii wskazały konkretne rejony obu cząsteczek działające jako „gorące punkty” kontaktu. Następnie użyto symulatora układu odpornościowego, aby odwzorować trzy dawki szczepionki podane w ciągu kilku miesięcy. Wirtualny układ odpornościowy wytworzył silne fale ochronnych przeciwciał IgG, długotrwałą pamięć komórek B i T oraz cząsteczki sygnałowe zgodne z mocną odpowiedzią przeciwwirusową.
Od modelu komputerowego do gotowego planu do laboratorium
Na koniec badacze zoptymalizowali kod genetyczny szczepionki pod kątem efektywnej produkcji w powszechnie stosowanych mikroorganizmach laboratoryjnych i pomyślnie umieścili tę zoptymalizowaną sekwencję DNA w standardowym plazmidzie ekspresyjnym, gotowym do przyszłych testów eksperymentalnych. Mówiąc prosto, ich praca dostarcza szczegółowy plan nowej szczepionki przeciw dengi, która celuje w starannie wybrane fragmenty DENV‑1 i DENV‑3, jest przewidywana jako stabilna i bezpieczna oraz powinna silnie angażować obie gałęzie układu odpornościowego. Chociaż wyniki te są wyłącznie obliczeniowe i muszą zostać potwierdzone w komórkach, zwierzętach, a w końcu u ludzi, pokazują, jak nowoczesna bioinformatyka może szybko generować dopasowane kandydatury szczepionek dla złożonych problemów, takich jak współzakażenia dengi.
Cytowanie: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Słowa kluczowe: szczepionka przeciw dengie, wieloepitopowa, DENV-1, DENV-3, immunoinformatyka