Clear Sky Science · pl
Analiza integracyjna proteomiki i metabolomiki ujawnia zaburzenia metabolizmu aminokwasów w komórkach ostrej białaczki szpikowej opornych na adriamycynę
Dlaczego niektóre leki przeciw białaczce przestają działać
Chemioterapia zrewolucjonizowała leczenie ostrej białaczki szpikowej (AML), szybko postępującego nowotworu krwi. Mimo to u wielu pacjentów choroba nawraca, ponieważ komórki nowotworowe uczą się przetrwać pod wpływem leków zaprojektowanych, by je zniszczyć. W badaniu zadano proste, lecz kluczowe pytanie: co się zmienia w komórkach białaczki, gdy stają się oporne na adriamycynę — jeden z podstawowych leków chemioterapeutycznych — i czy te zmiany mogą wskazać nowe sposoby przywrócenia skuteczności leku?
Wgląd do wnętrza komórek białaczkowych
Aby to zbadać, naukowcy porównali powszechną ludzką linię komórkową AML o nazwie HL60 z siostrzaną linią uodpornioną na adriamycynę (HL60/R). Zamiast analizować pojedynczy gen czy białko, zastosowali dwa szerokie, uzupełniające się podejścia. Proteomika zmierzyła tysiące różnych białek — głównych wykonawców większości zadań w komórce. Metabolomika zmierzyła setki małych cząsteczek biorących udział w metabolizmie komórkowym, w tym tłuszcze, cukry i aminokwasy. Łącząc te warstwy „omiczne”, zespół zbudował szczegółowy obraz różnic między komórkami opornymi a ich wciąż wrażliwymi odpowiednikami.
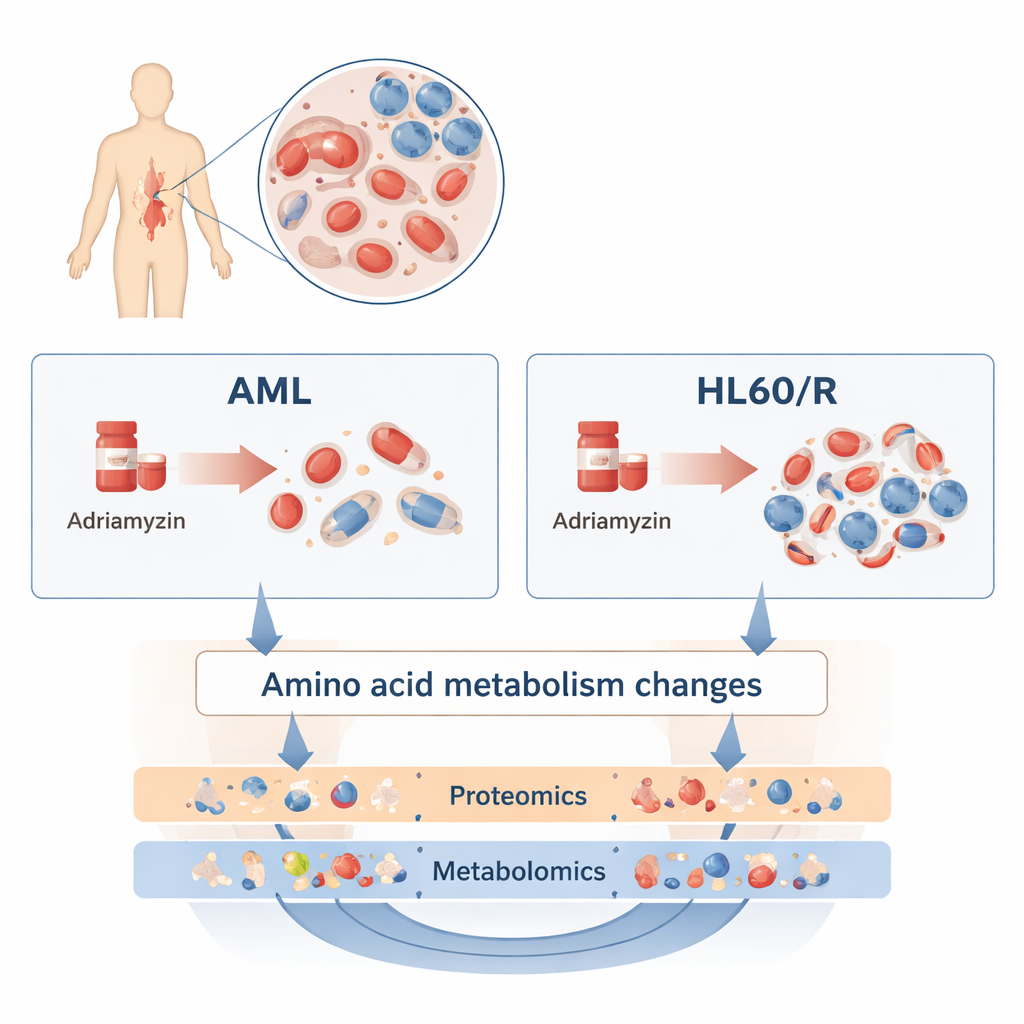
Ogromna przebudowa maszynerii komórkowej
Badanie proteomiczne ujawniło rozległe zmiany: ponad 3200 białek występowało na wyższych lub niższych poziomach w komórkach opornych na adriamycynę w porównaniu z komórkami HL60. Wiele z tych białek skupiało się w szlakach kontrolujących wykorzystanie energii i reakcję na stres. W szczególności zmienione były białka związane ze szlakiem sygnalizacji cAMP, szlakiem HIF‑1 (pomagającym komórkom radzić sobie z niskim stężeniem tlenu) oraz fosforylacją oksydacyjną (głównym procesem wytwarzania energii w mitochondriach). Te przestawienia sugerują, że komórki oporne reprogramują sposób oddychania, wzrostu i komunikacji, by wytrzymać chemioterapię.
Metabolizm przesuwa się w stronę aminokwasów
Analiza metabolomiczna opowiedziała uzupełniającą historię. Z około 1400 wykrytych metabolitów, 260 zmieniło się istotnie w komórkach opornych. Modele statystyczne wyraźnie odróżniały komórki oporne od nieopornych, wskazując na spójny metaboliczny sygnał oporności. Po zmapowaniu zmienionych metabolitów na znane ścieżki biochemiczne, wyeksponowało się kilka dróg. Wiele najsilniej dotkniętych ścieżek wiązało się z aminokwasami, budulcem białek — szczególnie z szlakami obejmującymi alaninę, asparaginian, glutaminian, cysteinę, metioninę i glutation. Zaburzone były także inne sieci, takie jak metabolizm puryn i pirymidyn (ważny dla DNA i RNA) oraz przemiany niektórych tłuszczów, co podkreśla, że oporność wiąże się z szerokim przebudowaniem metabolizmu.
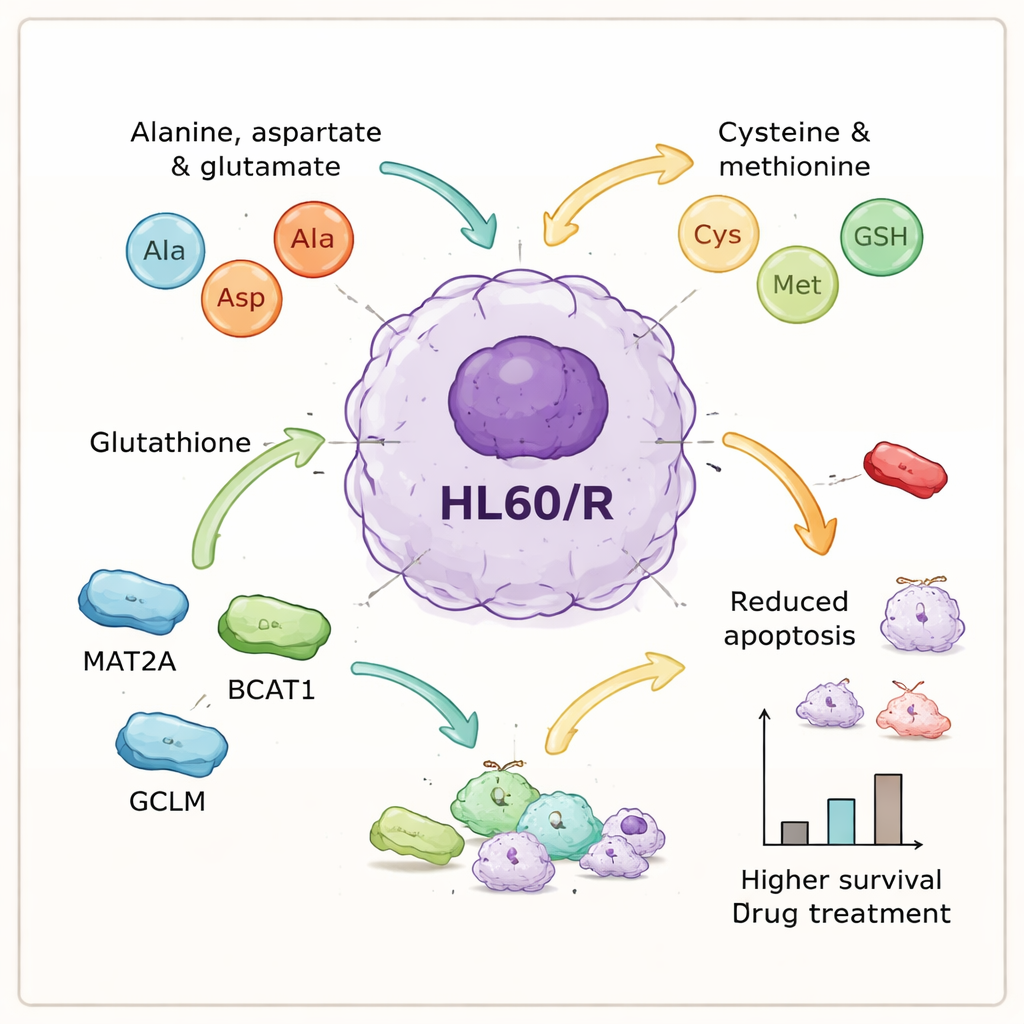
Kluczowe molekularne elementy, które pomagają komórkom nowotworowym przetrwać
Poprzez integrację danych o białkach i metabolitach autorzy zawęzili uwagę do zestawu procesów związanych z aminokwasami, które wydawały się centralne dla oporności. Wybrali sześć białek powiązanych z tymi szlakami — GOT1, GPX1, AHCY, MAT2A, BCAT1 i GCLM — do bliższej analizy. Testy laboratoryjne potwierdziły, że pięć z nich występowało w większej ilości w komórkach opornych, co jest zgodne z hipotezą o zwiększonej aktywności przetwarzania aminokwasów, podczas gdy jedno białko antyoksydacyjne, GPX1, było zmniejszone. Aby zbadać przyczynowość, zespół użył małych interferujących RNA, by obniżyć ekspresję trzech z up‑regulowanych białek — MAT2A, BCAT1 i GCLM — w komórkach opornych. Po ich wyciszeniu komórki wykazywały znacząco więcej zaprogramowanej śmierci po leczeniu, co oznacza, że straciły dużą część uzyskanej ochrony przed adriamycyną.
Co to oznacza dla przyszłych terapii
Podsumowując, te wyniki sugerują, że komórki AML oporne na adriamycynę przetrwają nie tylko z powodu pojedynczych mutacji, lecz dlatego, że przebudowują swoją wewnętrzną chemię, z metabolizmem aminokwasów jako ośrodkiem tej zmiany. Przekierowując więcej zasobów do określonych szlaków aminokwasowych i glutationowych, komórki wydają się lepiej radzić sobie ze stresem, naprawiać uszkodzenia i unikać śmierci po ekspozycji na chemioterapię. Dla osób niebędących specjalistami kluczowy przekaz jest taki, że oporność nie jest przypadkowa: podąża za rozpoznawalnymi wzorcami, które można mierzyć i potencjalnie celować. W dłuższej perspektywie leki zakłócające funkcję konkretnych białek przetwarzających aminokwasy, takich jak MAT2A, BCAT1 czy GCLM, mogłyby być łączone z adriamycyną lub podobnymi środkami, dając klinicystom nowe narzędzia do zapobiegania lub przełamywania oporności u pacjentów z ostrą białaczką szpikową.
Cytowanie: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Słowa kluczowe: ostra białaczka szpikowa, oporność na leki, adriamycyna, metabolizm aminokwasów, wieloomiczne