Clear Sky Science · pl
Funkcjonalny i odporny model komórkowy do przesiewów wysokoprzepustowych modulatorów Piezo1
Dlaczego małe czujniki ciśnienia w naszych komórkach mają znaczenie
Za każdym razem, gdy krew przepływa przez naczynia, albo gdy po prostu przechodzimy przez pokój, nasze komórki odczuwają drobne siły mechaniczne. Kluczowe białko‑„czujnik ciśnienia” o nazwie Piezo1 pomaga komórkom przekształcać te siły w sygnały elektryczne i chemiczne, które utrzymują tkanki w zdrowiu. Ponieważ Piezo1 bierze udział w wzroście naczyń krwionośnych, wytrzymałości kości, funkcjonowaniu układu odpornościowego oraz w rzadkich chorobach genetycznych, poszukiwacze leków chcą znaleźć związki modulujące jego aktywność. Opisana tutaj praca przedstawia nowy, szybszy sposób poszukiwania takich cząsteczek, wykorzystujący zmodyfikowane komórki i optyczne odczyty zamiast powolnych, pracochłonnych technik.
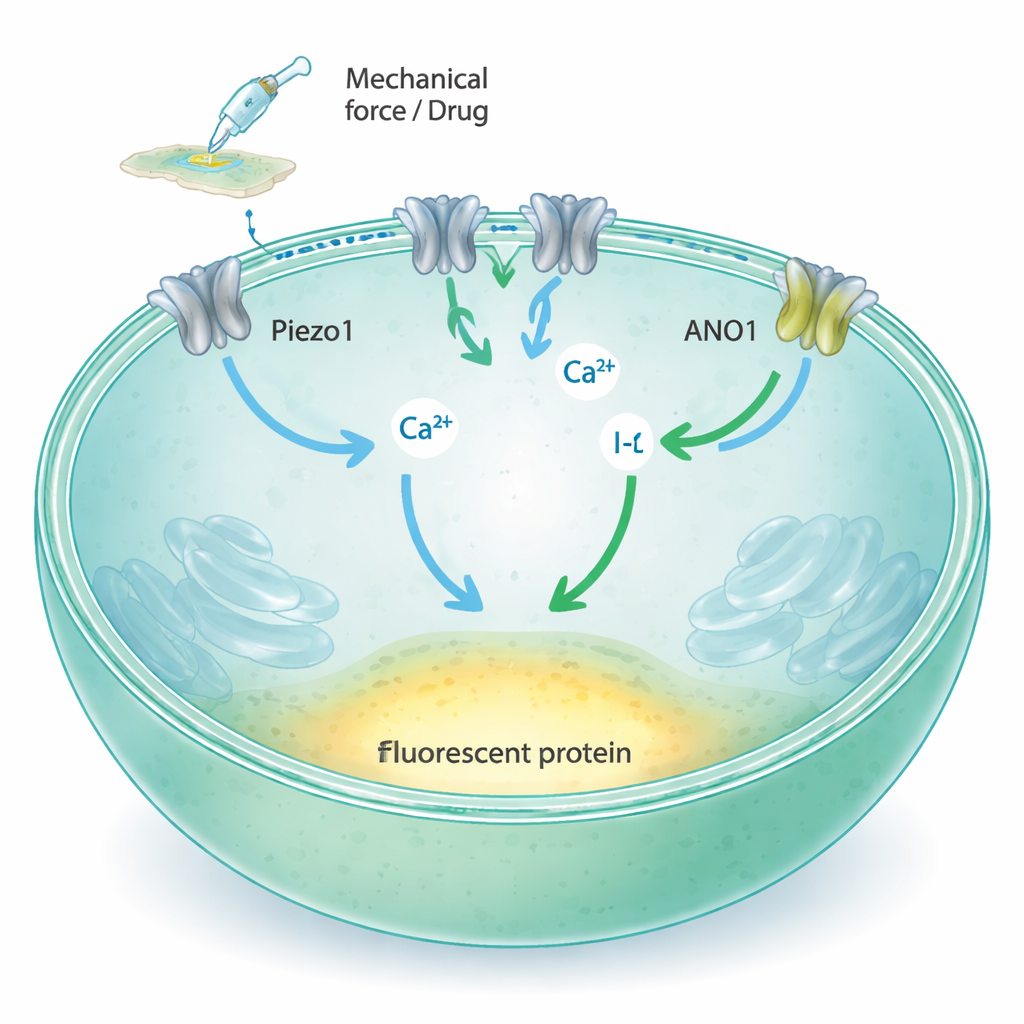
Przekształcanie dotyku w sygnał świetlny
Piezo1 to kanał w błonie komórkowej, który otwiera się, gdy błona jest rozciągana lub naciskana, pozwalając na napływ jonów wapnia i innych naładowanych atomów do wnętrza komórki. Tradycyjne metody badania takich kanałów polegają na cienkich elektrodom szklanych lub wyspecjalizowanych detektorach fluorescencyjnych, które są potężne, ale trudne do skalowania do dziesiątek tysięcy testów wymaganych w nowoczesnym odkrywaniu leków. Autorzy postanowili zamienić aktywność Piezo1 na prostą zmianę światła, którą czytnik płytek może szybko zmierzyć w wielu próbkach jednocześnie. Ich pomysł polegał na połączeniu Piezo1 z dwoma dodatkowymi składnikami: ANO1, innym kanałem jonowym reagującym na wapń, oraz zmodyfikowanym żółtym białkiem fluorescencyjnym, które traci jasność w obecności anionów jodkowych.
Budowa reagującej komórki testowej
Naukowcy zaczęli od komórek tarczycy szczura linii Fischer (FRT), które naturalnie produkują Piezo1 i dobrze przywierają do standardowych płytek plastikowych. Potwierdzili, że te komórki eksprymują Piezo1, ale nie jego bliskiego krewnego Piezo2, i wykazali, że Piezo1 w tych komórkach reaguje na przepływ cieczy i mechaniczne sondowanie poprzez napływ wapnia. Następnie wprowadzili do komórek kanał ANO1 oraz czuły na jodek czujnik fluorescencyjny (YFP‑H148Q/I152L). Gdy wewnątrzkomórkowy poziom wapnia rośnie, ANO1 się otwiera i pozwala na wejście jodku; białko fluorescencyjne wtedy przygasa, gdy jodek się wokół niego kumuluje. Mikroskopia, cytometria przepływowa i zapisy elektryczne pokazały, że zarówno ANO1, jak i czujnik fluorescencyjny występują na wysokim poziomie i działają zgodnie z zamierzeniem.
Od działania leku do mierzalnego blasku
Z tym trzyczęściowym układem zespół stworzył prosty łańcuch przyczyna‑skutek: jeśli badana cząsteczka aktywuje Piezo1, napływa wapń, ANO1 się otwiera, jodek wpada do środka, a sygnał fluorescencyjny maleje; jeśli cząsteczka blokuje Piezo1, sygnał pozostaje jasny. Logikę tę zweryfikowano przy użyciu dobrze znanych aktywatorów Piezo1 (Yoda1, Jedi1, Jedi2) i blokerów (Ruthenium Red, GsMTx4). Aktywatory wywoływały zależne od dawki spadki fluorescencji, z wartościami czułości zgodnymi z wcześniej opublikowanymi danymi. Blokery dawały odwrotny wzorzec, osłabiając odpowiedź wraz ze wzrostem stężenia. Test działał tylko w obecności zarówno wapnia, jak i jodku, co podkreśla, że sygnał rzeczywiście zależał od napływu wapnia przez Piezo1 i następnego napływu jodku przez ANO1. Miary statystyczne, takie jak współczynnik Z i stosunek sygnału do szumu, wskazywały, że metoda jest stabilna i wystarczająco niezawodna do przesiewów na skalę przemysłową.
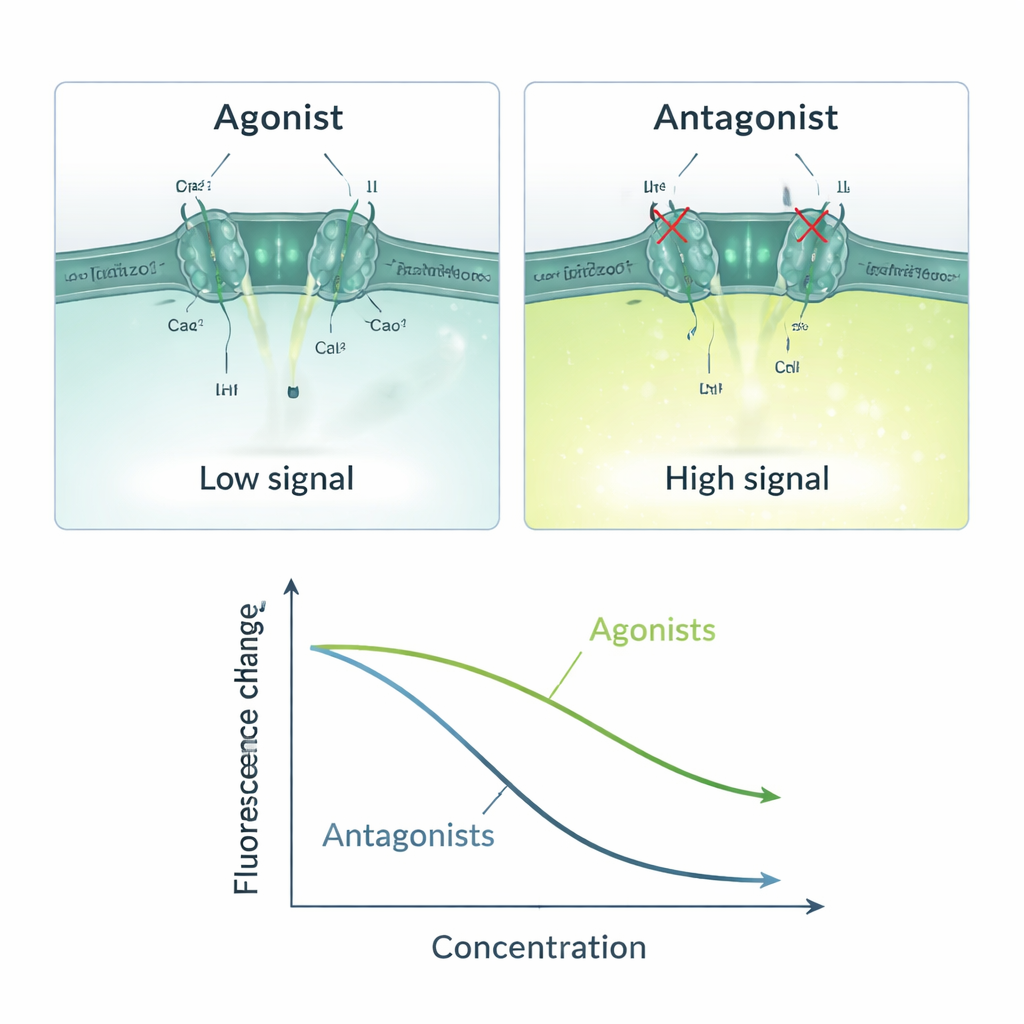
Szybkie, skalowalne testy z pewnymi zastrzeżeniami
Nowy model komórkowy może wykonać pomiar pojedynczej studzienki w około 14 sekund i zeskanować całą płytkę 96‑dołkową w mniej więcej 22 minuty, i można go dostosować do urządzeń odczytujących setki dołków jednocześnie. Zmodyfikowane komórki pozostają stabilne przez wiele pokoleń pod selekcją antybiotykową, co pozwala na powtarzalne eksperymenty w czasie. Ponieważ odczyt jest optyczny i wykorzystuje standardowy sprzęt do mikro płytek, podejście jest stosunkowo tanie i dostępne. Autorzy jednak zauważają, że ich test jest pośredni: każdy związek działający na kroki przed lub po Piezo1 w łańcuchu sygnalizacyjnym — na przykład na sam ANO1 lub inne białka obsługujące wapń — może dawać wynik fałszywie pozytywny. Z tego powodu trafienia z tego przesiewu nadal wymagają potwierdzenia bardziej bezpośrednimi metodami, takimi jak elektrofizjologia.
Co to oznacza dla przyszłych terapii
Mówiąc obrazowo, badacze zbudowali laboratoryjny „alarm dymowy”, który przygasa za każdym razem, gdy związek popycha Piezo1 do otwarcia, i pozostaje jasny, gdy Piezo1 jest zablokowany. Ten alarm jest czuły, szybki i łatwy do przeprowadzenia na dużą skalę, co czyni go dobrze dopasowanym do pierwszego etapu poszukiwania leków modulujących komórkowe czujniki mechaniczne. Chociaż nie zastąpi bardziej szczegółowych testów follow‑up, model komórkowy stanowi potężny punkt wyjścia do odkrywania cząsteczek, które pewnego dnia mogą pomóc w leczeniu zaburzeń naczyń krwionośnych, chorób kości, problemów immunologicznych i innych schorzeń związanych z tym, jak nasze komórki odczuwają i reagują na siły fizyczne.
Cytowanie: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
Słowa kluczowe: Kanał Piezo1, mechanowrażliwe kanały jonowe, przesiewy wysokoprzepustowe, test komórkowy, odkrywanie leków