Clear Sky Science · pl
Synteza, charakteryzacja, analiza DFT, dokowanie molekularne i badania przeciwnowotworowe w raku jelita grubego nowego kompleksu cynk(II) z pyrazolem‑hydrazoną
Dlaczego lek na bazie metalu może łagodniej zwalczać raka jelita
Wiele skutecznych leków przeciwnowotworowych opiera się na cięższych metalach, takich jak platyna. Mogą być efektywne, ale często wiążą się z ostrymi skutkami ubocznymi i narastającą opornością. W tym badaniu rozważono inne podejście: nowy kandydat na lek zbudowany wokół cynku — pierwiastka niezbędnego i obecnego w organizmie — sprzężony z organicznym szkieletem zwanym pyrazolem–hydrazoną. Naukowcy postawili pytanie, czy przyłączenie cynku do tego szkieletu może stworzyć związek, który mocno uderzy w komórki raka jelita, a jednocześnie oszczędzi komórki zdrowe.
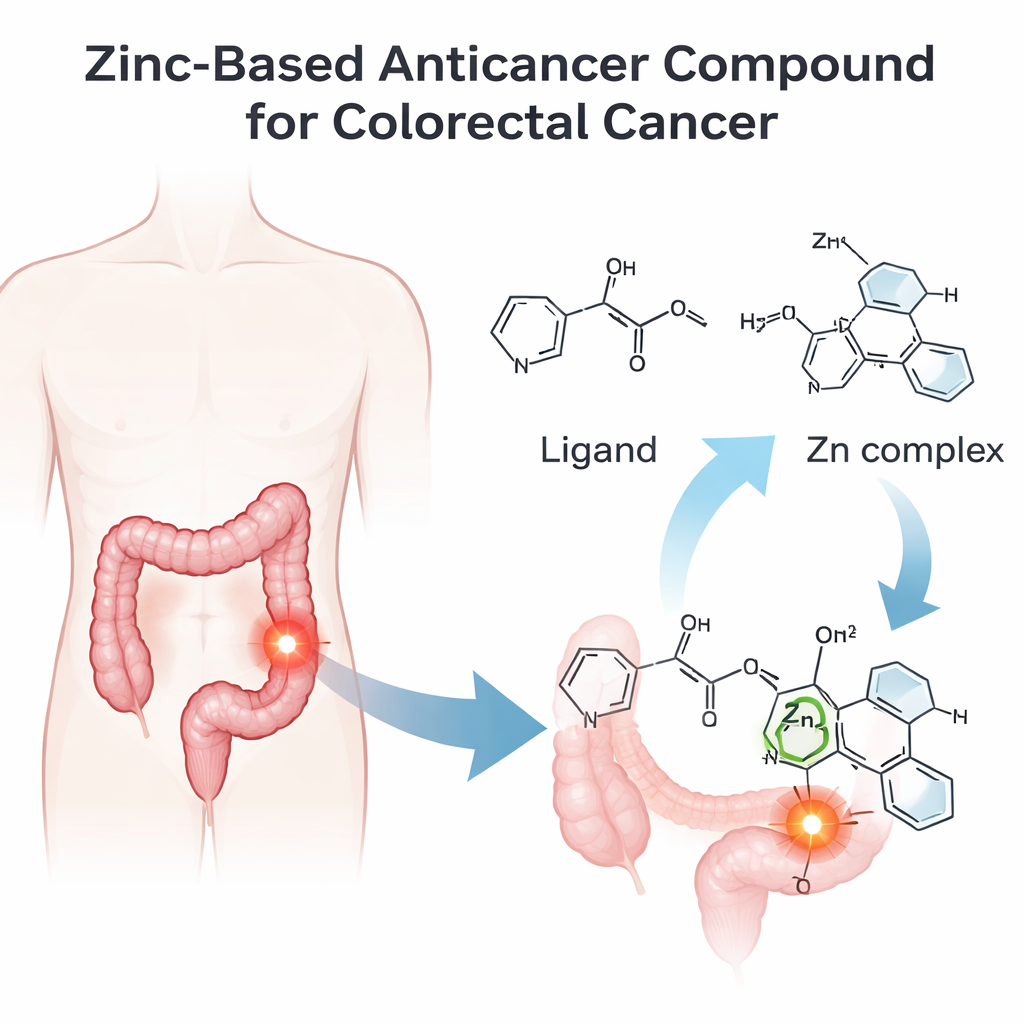
Budowanie „mądrzejszej” cząsteczki na bazie cynku
Zespół najpierw zaprojektował i zsyntezował nową cząsteczkę organiczną, oznaczoną jako IMP, a następnie związano ją z jonem cynku, tworząc kompleks cynkowy nazwany IMP‑Zn. Dokładną strukturę obu związków potwierdzono zestawem technik służących za „odciski palców” molekuł: spektroskopia w podczerwieni do identyfikacji wiązań chemicznych, spektroskopia magnetycznego rezonansu jądrowego do mapowania pozycji atomów, spektrometria mas w celu weryfikacji masy cząsteczkowej oraz spektroskopia UV–vis do badania interakcji z światłem. Te eksperymenty, razem z testami przewodnictwa elektrycznego, wykazały, że cynk jest silnie skoordynowany z trzema kluczowymi atomami w IMP oraz dwiema jonami chlorkowymi, tworząc pojedynczy, dobrze zdefiniowany kompleks z centrum cynkowym.
Zajrzeć w cząsteczkę dzięki chemii obliczeniowej
Aby uzupełnić pomiary laboratoryjne, badacze przeprowadzili szczegółowe symulacje komputerowe wykorzystujące teorię funkcjonału gęstości (DFT). Obliczenia te pozwoliły przewidzieć rozkład elektronów w IMP i IMP‑Zn, stabilność poszczególnych form oraz skłonność cząsteczek do reaktywności chemicznej. Wyniki pokazały, że po przyłączeniu cynku zmniejsza się luka energetyczna między „frontowymi” orbitalami cząsteczki, co oznacza, że elektrony mogą poruszać się łatwiej w strukturze. Zwykle przekłada się to na wyższą reaktywność chemiczną. Kompleks cynkowy wykazał także wyższy tzw. indeks elektrofilowy, sugerując, że jest lepiej przystosowany do interakcji z celami biologicznymi niż wolny ligand IMP.
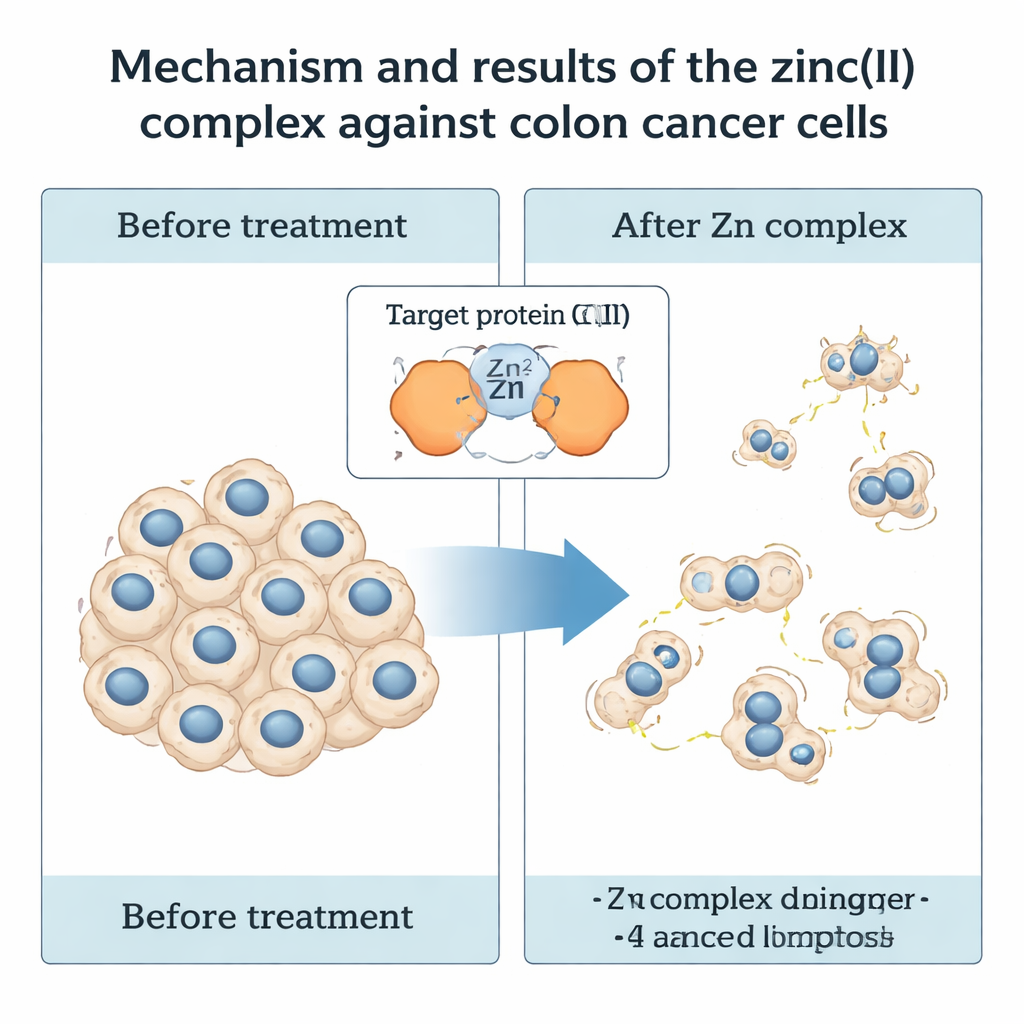
Jak kompleks cynkowy atakuje komórki raka jelita
Prawdziwy test miały badania biologiczne. Naukowcy leczyli ludzkie komórki raka jelita grubego (HCT116) za pomocą IMP i IMP‑Zn w różnych dawkach i w różnych odstępach czasu, a następnie mierzyli przeżywalność komórek. Oba związki hamowały wzrost komórek nowotworowych, ale kompleks cynkowy był wyraźnie silniejszy: po 48 godzinach IMP‑Zn zmniejszał żywotność komórek o połowę przy około 25 µM, podczas gdy sam ligand wymagał znacznie wyższych dawek. Co równie istotne, te same stężenia IMP‑Zn nie wykazywały wykrywalnej toksyczności wobec normalnej linii komórek nerkowych człowieka (HEK293), co wskazuje na pewien stopień selektywności wobec komórek nowotworowych. Gdy zespół obserwował leczone komórki przez dwa tygodnie, stwierdzono, że IMP‑Zn zdecydowanie zmniejsza zarówno liczbę, jak i rozmiar kolonii, które komórki mogły tworzyć, co sugeruje zakłócenie ich długoterminowej zdolności do proliferacji.
Wskazówki, że komórki kierowane są ku zaprogramowanej śmierci
Aby zrozumieć, w jaki sposób kompleks cynkowy szkodzi komórkom nowotworowym, naukowcy przeanalizowali cykl komórkowy — sekwencję etapów, które komórki przechodzą podczas wzrostu i podziału. Po ekspozycji na IMP‑Zn znacznie większy odsetek komórek HCT116 przesunął się do fazy „SubG0”, charakterystycznej dla komórek z fragmentowaną DNA. Ten wzorzec jest zwykle związany z apoptozą, kontrolowaną formą śmierci komórkowej często wywoływaną przez leki przeciwnowotworowe. Symulacje dokowania molekularnego dostarczyły kolejnej cegiełki do układanki: modele in silico sugerowały, że IMP‑Zn wiąże się silniej niż IMP z kilkoma białkami powiązanymi z nowotworem, w tym kinazą receptora czynnika wzrostu, kinazą regulującą cykl komórkowy oraz enzymem metabolizującym leki. Te silniejsze interakcje wspierają hipotezę, że koordynacja cynku pomaga związkowi przyczepiać się do kluczowych elementów komórkowej maszyny i zaburzać przetrwanie komórek nowotworowych.
Co to może oznaczać dla przyszłych terapii
Podsumowując, badanie pokazuje, że „ozdobienie” szkieletem pyrazolu–hydrazony atomem cynku robi więcej niż tylko zmienia chemię związku: przekształca IMP w bardziej reaktywny, silniejszy i zdaje się bardziej selektywny czynnik przeciwko komórkom raka jelita grubego. Choć IMP‑Zn jest wciąż daleki od gotowego leku — nie przeprowadzono jeszcze badań na zwierzętach ani ludziach — jego zdolność do znaczącego spowolnienia wzrostu komórek nowotworowych jelita, skłaniania ich ku apoptozie i oszczędzania komórek normalnych czyni go obiecującym przedstawicielem rosnącej klasy metalo‑leków opartych na cynku. Praca ta sugeruje, że starannie zaprojektowane kompleksy cynkowe mogą w przyszłości stanowić łagodniejsze, ukierunkowane alternatywy lub uzupełnienia tradycyjnej chemioterapii opartej na metalach.
Cytowanie: Mermer, A., Bayrak, A.M., Bolat, Z.B. et al. Synthesis, characterization, DFT analysis, molecular docking and anticancer investigations in colorectal carcinoma of a novel pyrazole-hydrazone zinc(II) complex. Sci Rep 16, 6391 (2026). https://doi.org/10.1038/s41598-026-35664-6
Słowa kluczowe: leki przeciwnowotworowe oparte na cynku, rak jelita grubego, kompleks pyrazol‑hydrazonowy, dokowanie molekularne, apoptoza