Clear Sky Science · pl
Efekty radiosensytyzujące nanocząstek srebra ukierunkowane na angiogenezę i sygnalizację metaloproteinaz macierzy w liniach komórkowych potrójnie ujemnego raka piersi
Uczynienie opornych nowotworów piersi bardziej podatnymi
Potrójnie ujemny rak piersi jest jednym z najtrudniejszych do leczenia typów raka piersi. Ma skłonność do szybkiego wzrostu, wczesnego rozsiewu i brak mu typowych molekularnych „uchwytów”, na które celują współczesne leki. Radioterapia często stanowi część leczenia, ale te guzy bywają oporne. W badaniu postawiono proste, intrygujące pytanie: czy maleńkie cząstki srebra mogą zwiększyć skuteczność promieniowania, jednocześnie hamując zdolność guza do tworzenia nowych naczyń krwionośnych i rozprzestrzeniania się?
Maleńcy pomocnicy ze srebra dla radioterapii
Naukowcy skupili się na nanocząstkach srebra — ultramałych kulkach srebra mierzonych w miliardowych częściach metra. Ponieważ srebro jest gęste i silnie oddziałuje z promieniowaniem rentgenowskim, te cząstki mogą skoncentrować efekty promieniowania dokładnie tam, gdzie się kumulują. Zespół pracował na dwóch powszechnie stosowanych modelach laboratoryjnych potrójnie ujemnego raka piersi, porównując je z linią komórek piersi niezłośliwych. Najpierw przetestowali toksyczność nanocząstek srebra samych w sobie i stwierdzili, że komórki nowotworowe ginęły przy dużo niższych dawkach niż komórki normalne, co sugeruje użyteczne okno terapeutyczne. Przy użyciu metod matematycznych do analizy interakcji między cząstkami a promieniowaniem wykazali, że połączenie obu zabiegów dało wyraźnie silniejszy efekt zabijania komórek niż każde z nich osobno.
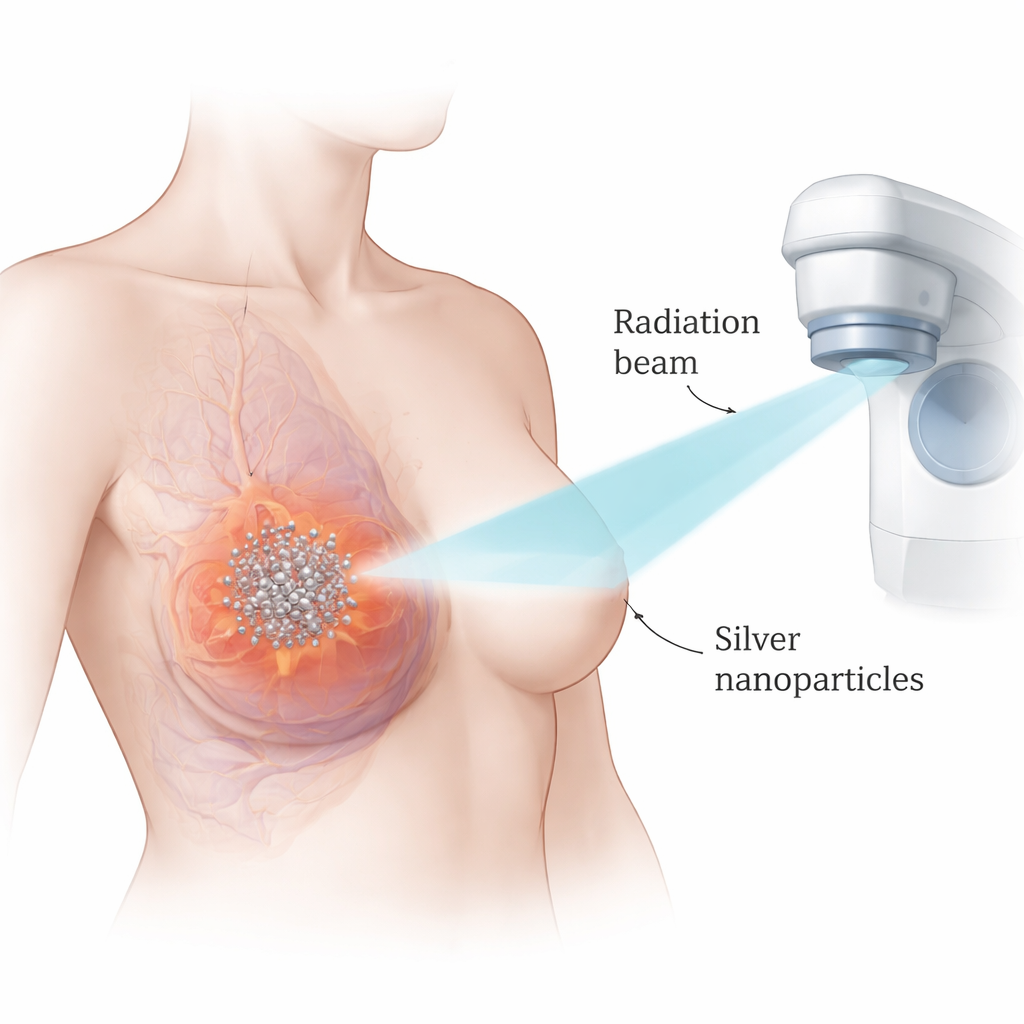
Skłanianie komórek nowotworowych do samobójstwa
Następnie badacze sprawdzili, jak leczenie skojarzone prowadzi do śmierci komórek. Mierzyli apoptozę, formę zaprogramowanej śmierci komórki, oraz śledzili gromadzenie się wysoko reaktywnych cząsteczek zwanych reaktywnymi formami tlenu (ROS). Wiadomo, że promieniowanie działa częściowo poprzez generowanie ROS uszkadzających DNA. W obu liniach potrójnie ujemnego raka piersi nanocząstki srebra same zwiększały poziomy apoptozy i ROS, podobnie jak samo promieniowanie — lecz ich łączne zastosowanie dramatycznie podnosiło oba wskaźniki. Oznacza to, że więcej komórek nowotworowych zostało popchniętych do uporządkowanego trybu samobójczego, zamiast utrzymywać się w uszkodzonym stanie, który czasem sprzyja nawrotom lub oporności.
Odcięcie dopływu krwi i spowolnienie rozprzestrzeniania
Guzy polegają na naczyniach krwionośnych, które dostarczają tlen i składniki odżywcze, a agresywne nowotwory potrafią nawet upodabniać się do naczyń. Zespół przyjrzał się dwóm kluczowym molekularnym przełącznikom zaangażowanym w budowę i stabilizację naczyń guza, nazywanym VEGFR2 i Tie2. W obu liniach komórkowych nanocząstki srebra obniżały aktywność tych genów, a połączenie z promieniowaniem tłumiło je jeszcze silniej. Badano także dwie enzymy, MMP-2 i MMP-9, które pomagają komórkom nowotworowym przeżuwać otaczającą tkankę i migrować. W jednym z modeli komórkowych zarówno promieniowanie, jak i nanocząstki srebra obniżały poziomy tych enzymów, podczas gdy leczenie skojarzone wywołało najsilniejszy efekt. Gdy naukowcy obserwowali, jak komórki nowotworowe przemieszczają się do sztucznego „zadrapania” w naczyniu, oraz testowali, jak dobrze tworzą struktury podobne do naczyń krwionośnych w systemie ko-kultury, leczenie skojarzone naj wyraźniej spowalniało migrację i formowanie rurkowatych struktur.
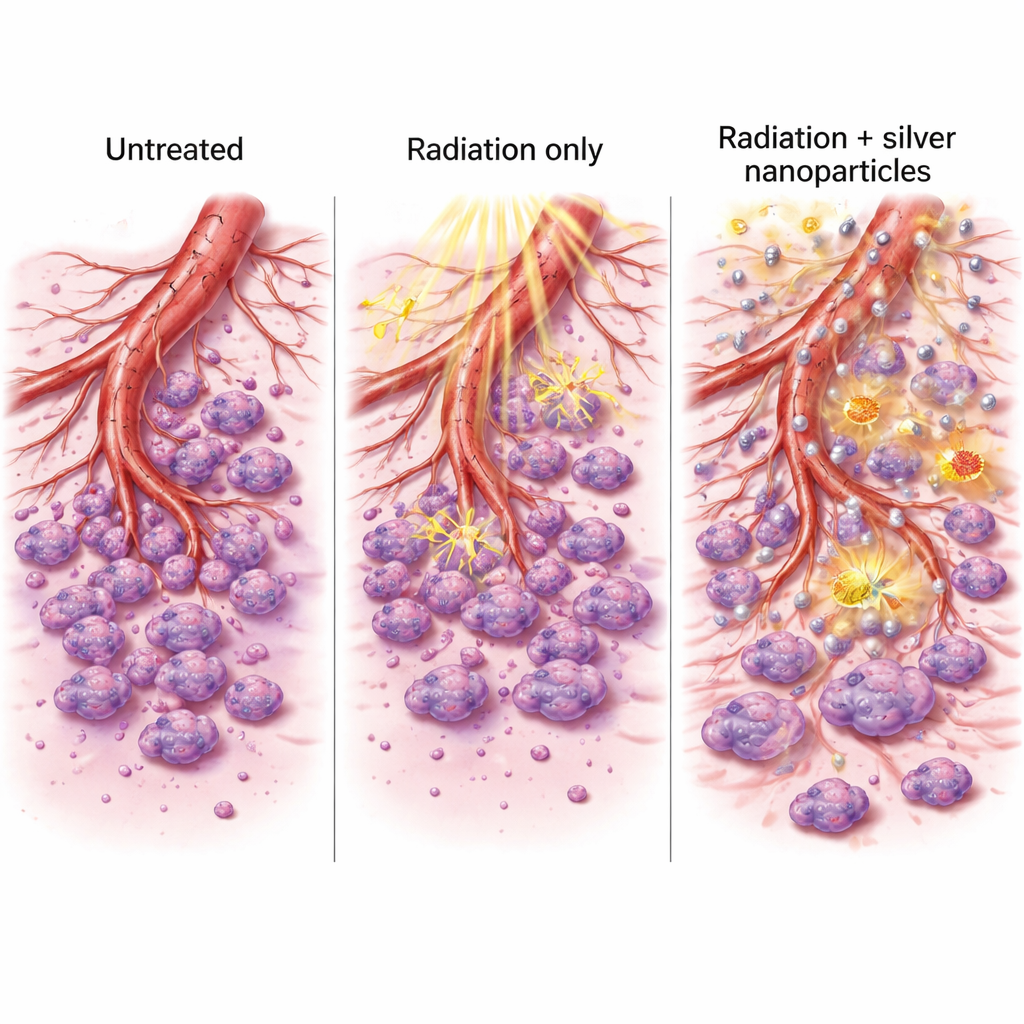
Dlaczego te zmiany mają znaczenie
Poprzez osłabienie genów sprzyjających tworzeniu nowych naczyń i enzymów ułatwiających inwazję, połączenie srebra i promieniowania zrobiło więcej niż tylko zabiło komórki nowotworowe. Zakłóciło również systemy wsparcia, z których guzy korzystają, by się rozrastać i rozsiewać. Komórki po leczeniu słabiej zamykały rany na płytkach laboratoryjnych i gorzej organizowały się w rozgałęzione sieci przypominające wczesne naczynia. W połączeniu z silnym wzrostem śmierci komórek i produkcji ROS, efekty te sugerują dwuetapową korzyść: silniejszy bezpośredni atak na guz i osłabienie narzędzi potrzebnych mu do dalszego wzrostu i przerzutowania.
Co to może znaczyć dla pacjentów
Na razie wyniki pochodzą z badań na komórkach hodowanych w laboratorium, a nie od pacjentów. Mimo to dają obraz z nadzieją. Nanocząstki srebra działały jako radiosensybilizatory, zwiększając skuteczność standardowej radioterapii wobec komórek potrójnie ujemnego raka piersi. Jednocześnie wydawały się utrudniać guzie budowę dopływów krwi i inwazję sąsiednych tkanek. Jeśli przyszłe badania na zwierzętach i badania kliniczne potwierdzą, że te cząstki można dostarczać bezpiecznie i selektywnie do guzów, mogą pomóc lekarzom stosować niższe dawki promieniowania przy jednoczesnym uzyskaniu lepszych wyników, oferując nowy sposób walki z jednym z najbardziej wymagających typów raka piersi.
Cytowanie: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
Słowa kluczowe: potrójnie ujemny rak piersi, nanocząstki srebra, radioterapia, angiogeneza, przerzuty