Clear Sky Science · pl
Chlorowane bis-4-hydroksykumaryny hamują replikację flawiwirusów poprzez inhibicję translacji i replikacji wirusa dengi typu 2
Nowe nadzieje przeciw wirusom przenoszonym przez komary
Wirusy dengi i Zika zakażają setki milionów ludzi rocznie, często w regionach o ograniczonych zasobach medycznych. Szczepionki dają tylko częściową ochronę, a wciąż nie ma powszechnie stosowanego leku przeciwwirusowego, który lekarze mogliby przepisać na wczesnym etapie choroby. Badanie to analizuje rodzinę syntetycznych związków pochodzących od molekuł roślinnych, stawiając proste, ale pilne pytanie: czy którykolwiek z nich potrafi niezawodnie spowolnić te wirusy w ludzkich komórkach, nie szkodząc jednocześnie samym komórkom?
Molekuły inspirowane roślinami jako blokery wirusów
Naukowcy skupili się na kumarynach, klasie związków naturalnych występujących w wielu roślinach i od dawna znanych z właściwości przeciwbakteryjnych i przeciwwirusowych. Przetestowali dwanaście pochodnych „biskumaryn” — dwóch połączonych jednostek kumaryny — przeciw wirusowi dengi typu 2 i wirusowi Zika w hodowlach komórkowych. Mierząc, ile zakaźnych cząstek wirusa powstaje oraz jak zdrowe pozostają komórki, odkryli, że dwie chlorowane wersje, oznaczone jako związek 3 i związek 4, są szczególnie obiecujące. W niskich stężeniach mikro molowych te chlorowane bis-4-hydroksykumaryny zmniejszały produkcję wirusa o ponad 90% przy jednoczesnym zachowaniu większości komórek przy życiu i w dobrej kondycji.
Precyzowanie chemii dla silniejszej ochrony
Nie wszystkie modyfikacje chemiczne działały jednakowo skutecznie. Poprzez systematyczną zmianę atomów wokół pierścieniowej części cząsteczek zespół ustalił, że przyłączenie chloru w określonych pozycjach dawało najlepszą aktywność przeciwwirusową. Podmiana chloru na inne halogeny, takie jak fluor czy brom, albo dodanie różnych grup chemicznych zazwyczaj osłabiało efekt wobec dengi i Zika. Modele komputerowe powiązały siłę działania przeciwwirusowego z prostymi cechami molekularnymi, takimi jak rozkład ładunku w cząsteczce i powierzchnia, jaką eksponuje. Metody uczenia maszynowego uchwyciły te zależności znacznie lepiej niż starsze narzędzia statystyczne, co sugeruje, że sztuczna inteligencja może pomóc w projektowaniu ulepszonych kandydatów na leki przeciw dengie.
Jak związki zaburzają cykl życiowy wirusa
Po wejściu do komórki wirus dengi używa swojego genomu RNA jako planu do wytworzenia długiego poliproteiny, która jest następnie cięta na funkcjonalne elementy, a także kopiuje swoje RNA, by stworzyć nowe wirusy. Badanie pokazuje, że związki 3 i 4 oddziałują głównie na etapy translacji i replikacji. W zakażonych komórkach poziomy kluczowego białka osłonkowego wirusa znacznie spadły w obecności związków, a system raportujący, śledzący replikację RNA wirusa, również osłabł w sposób zależny od dawki. Testy biochemiczne i dokowanie komputerowe wskazały na jeden enzym wirusowy, nazywany metylotransferazą NS5, jako bezpośredni, lecz stosunkowo słaby cel: związki mogły hamować funkcję „kapowania” RNA, choć nie tak silnie jak znany inhibitor referencyjny. Nieco spowalniały też proteazę wirusa, inny enzym używany do cięcia poliproteiny wirusowej.
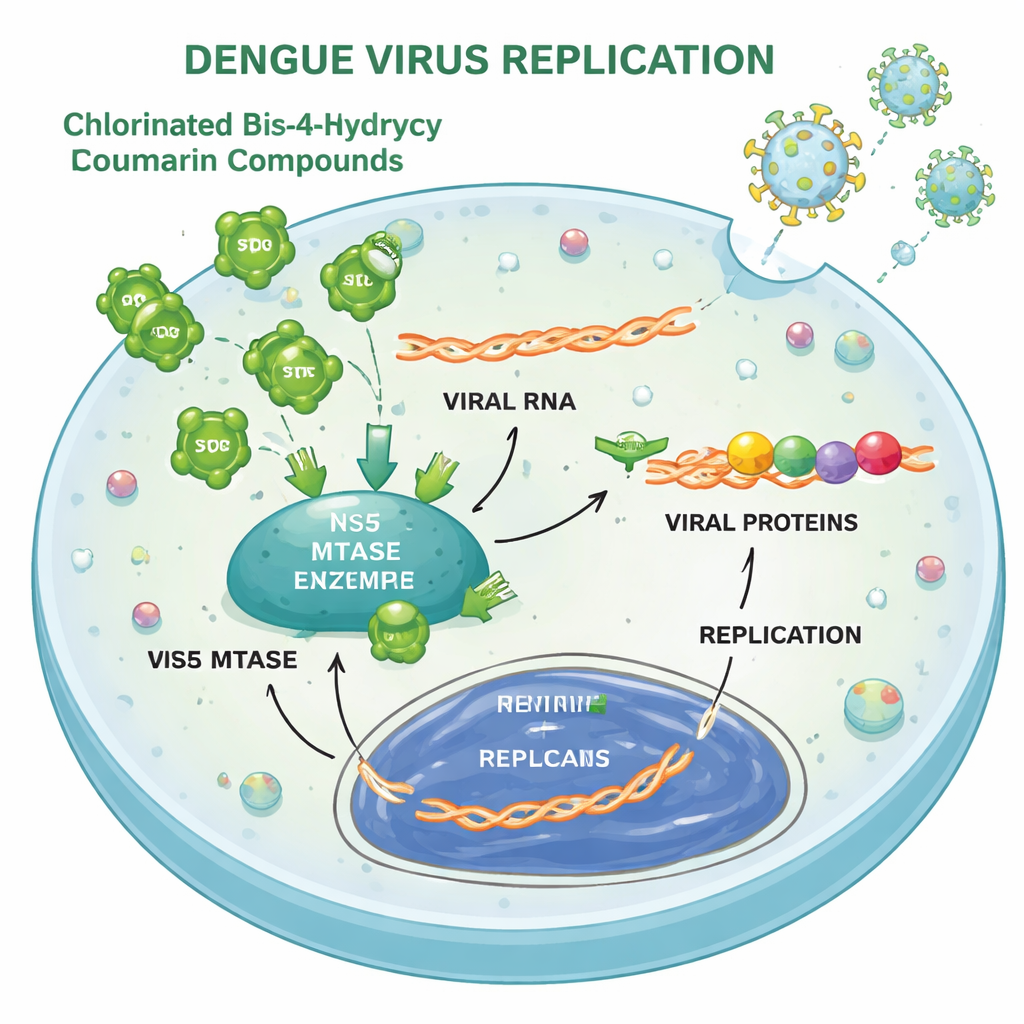
Wirusy mają trudności z adaptacją do ataku
Wirusy często unikają leków przez mutacje. Aby sprawdzić, czy może to zajść tutaj, zespół wielokrotnie hodował wirusa dengi w komórkach wystawionych na działanie nowych związków przez wiele cykli zakażenia. Pojawiło się kilka zmian w innym białku wirusowym, NS4B, które pomaga wyginać błony komórkowe tworząc kieszonki, w których zachodzi replikacja. Co zaskakujące, te zmutowane wirusy nie były mniej wrażliwe na związki niż szczep wyjściowy. Modele komputerowe sugerowały, że ogólny kształt NS4B pozostał w dużej mierze niezmieniony. Ten wzorzec sugeruje, że mutacje były raczej ogólnymi dostosowaniami do życia w warunkach stresu, a nie prawdziwą odpornością. Wspiera to też ideę, że związki działają na wiele elementów machiny replikacyjnej lub na czynniki gospodarza, których wirus nie może łatwo przesterować.
Dlaczego te odkrycia mają znaczenie dla przyszłych terapii
Dla osób niebędących specjalistami główne przesłanie jest takie, że naukowcy odkryli nowy chemiczny „szkielet”, który może spowalniać wirusy dengi i Zika na kilku etapach ich cyklu życiowego, szczególnie gdy wirusy próbują tłumaczyć swoje geny i kopiować RNA w komórkach. Najbardziej obiecująca cząsteczka, związek 3, działa w niskich dawkach, stosunkowo mało uszkadza komórki, działa przeciw wszystkim czterem głównym typom dengi oraz Zika i nie powoduje szybkiego pojawienia się oporności wirusa w warunkach laboratoryjnych. Choć chlorowane bis-4-hydroksykumaryny są wciąż daleko od statusu leku, stanowią solidny punkt wyjścia dla chemików i wirusologów do udoskonalania, testów na zwierzętach i ostatecznego łączenia z innymi lekami — kroki, które mogą przybliżyć nas do długo oczekiwanej pigułki przeciwwirusowej na infekcje przenoszone przez komary.
Cytowanie: Loeanurit, N., Phan, THT., Hengphasatporn, K. et al. Chlorinated bis-4-hydroxycoumarins suppress flavivirus replication by inhibiting dengue virus type 2 translation and replication. Sci Rep 16, 5300 (2026). https://doi.org/10.1038/s41598-026-35654-8
Słowa kluczowe: wirus dengi, wirus Zika, związki przeciwwirusowe, pochodne kumaryny, replikacja wirusowa