Clear Sky Science · pl
Reakcja chemosensoryczna na leki chemioterapeutyczne oparte na Pt poprzez receptory goryczy in vitro ujawnia nowy mechanizm zaburzeń smaku gorzkiego
Dlaczego leki przeciwnowotworowe nagle sprawiają, że wszystko smakuje okropnie
Pacjenci onkologiczni często zgłaszają, że jedzenie zaczyna mieć dziwnie gorzki lub metaliczny smak wkrótce po rozpoczęciu chemioterapii. To nie tylko psuje posiłki: może zmniejszać apetyt, sprzyjać utracie wagi i obniżać jakość życia dokładnie wtedy, gdy pacjenci potrzebują sił najbardziej. To badanie stawia pozornie proste pytanie o dużych praktycznych konsekwencjach: w jaki sposób powszechnie stosowane leki chemioterapeutyczne oparte na platynie zakłócają nasz zmysł smaku i czy można bezpiecznie zmniejszyć ten efekt bez osłabiania leczenia?
Ukryta rola „czujników goryczy” w jelitach i jamie ustnej
Nasze języki i przewód pokarmowy pełne są receptorów smaku gorzkiego, stworzonych, by ostrzegać nas przed potencjalnie szkodliwymi substancjami. Te sensory, znane jako TAS2R, nie ograniczają się do kubków smakowych; występują także w komórkach żołądka. Badacze wykorzystali linię komórkową ludzkiego żołądka (HGT-1), która pełni rolę in vitro detektora goryczy: gdy receptory gorzkie są aktywowane, komórki wydzielają więcej protonów (kwasu), co można zmierzyć jako zmianę tzw. wskaźnika protonów wewnątrzkomórkowych. Poprzez wystawienie tych komórek na dwa szeroko stosowane leki przeciwnowotworowe oparte na platynie — karboplatynę i cisplatynę — zespół mógł bezpiecznie zbadać, jak „gorzkie” te leki wydają się komórkom ludzkim, nie każąc nikomu smakować toksycznego związku. 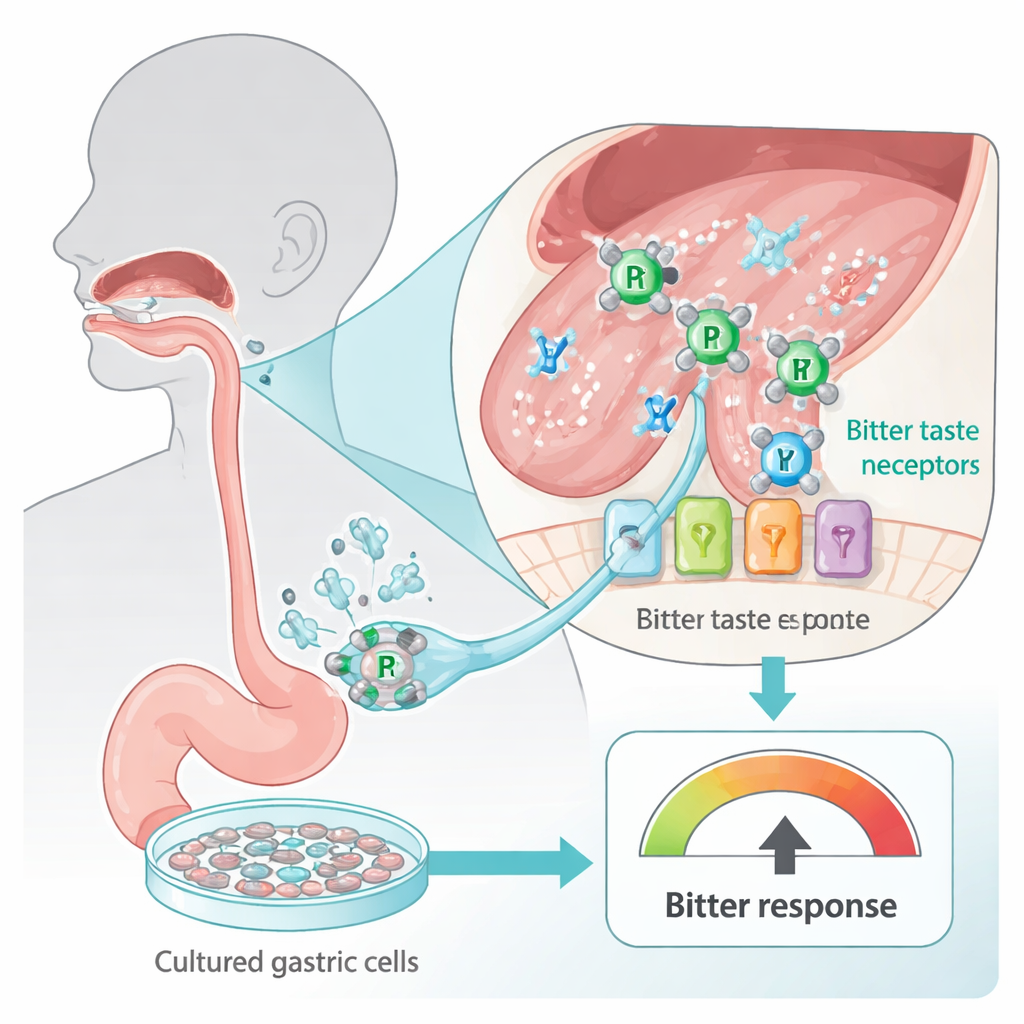
Leki chemioterapeutyczne, które dla komórek smakują gorzko
Gdy komórki żołądkowe były traktowane stężeniami karboplatyny i cisplatyny odpowiadającymi klinicznym, oba leki wywołały wyraźną, zależną od dawki reakcję przypominającą gorycz: im wyższa dawka, tym silniejsza reakcja komórkowa. Cisplatyna jednak powodowała intensywniejszą odpowiedź niż karboplatyna, po uwzględnieniu ich zwykłego terapeutycznego stosunku dawek (około 1:4), co sugeruje, że może ona silniej przyczyniać się do problemów z gorzkim smakiem u pacjentów. Na poziomie genetycznym ekspozycja na te leki zmieniała aktywność wielu genów receptorów gorzkich w komórkach, wskazując, że leki platynowe nie działają przez pojedynczy „przełącznik goryczy”, lecz szeroko przekształcają system wyczuwania goryczy. Wśród tych receptorów wyróżniały się TAS2R4 i TAS2R5 jako zarówno wysoko aktywne, jak i silnie dotknięte leczeniem.
Wyłączanie sygnałów goryczy i testowanie naturalnego blokera goryczy
Aby ustalić, które receptory mają największe znaczenie, zespół selektywnie wyłączał konkretne receptory gorzkie. Usunięcie TAS2R4 lub stłumienie ekspresji TAS2R5 każdorazowo zmniejszało odpowiedź przypominającą gorycz na karboplatynę i cisplatynę, potwierdzając, że te receptory pomagają wykrywać leki. Naukowcy przetestowali następnie obiecujący środek zaradczy: sól sodową homoeriodictyolu (Na-HED), flawanon pierwotnie wyizolowany z północnoamerykańskiej rośliny Herba Santa i już znany z maskowania goryczy innych związków. Gdy Na-HED dodawano razem z lekami platynowymi, wyraźnie stłumił on komórkową odpowiedź goryczową — mniej więcej o trzy czwarte dla obu: karboplatyny i cisplatyny — nie szkodząc przy tym samym komórkom. To pokazuje, że Na-HED może działać bezpośrednio na receptory gorzkie, by osłabić sygnał wywoływany przez leki chemioterapeutyczne.
Gdy wykrywanie goryczy i pobieranie leku się przecinają
Ponad wyjaśnieniem, dlaczego chemioterapia platynowa może smakować gorzko, badanie ujawnia nieoczekiwane zjawisko: te same receptory gorzkie wydają się także wpływać na to, ile tych leków wnika do komórek. Za pomocą wysoce czułej spektrometrii mas badacze zmierzyli zawartość platyny w komórkach po leczeniu. Komórki pozbawione niektórych receptorów, takich jak TAS2R4 lub TAS2R43, gromadziły więcej platyny niż komórki normalne, co sugeruje, że nienaruszone receptory pomagają ograniczać pobieranie lub zatrzymywanie tych toksycznych czynników. Na-HED nie zmieniał wchłaniania karboplatyny, ale zmniejszał ilość cisplatyny wnikającej do komórek i wykazywał bezpośrednią interakcję molekularną z cisplatyną w roztworze. To sugeruje, że związek maskujący gorycz mógłby w niektórych przypadkach także modulować, jak silnie lek oddziałuje na tkanki miejscowe, takie jak komórki smakowe czy gruczoły ślinowe. 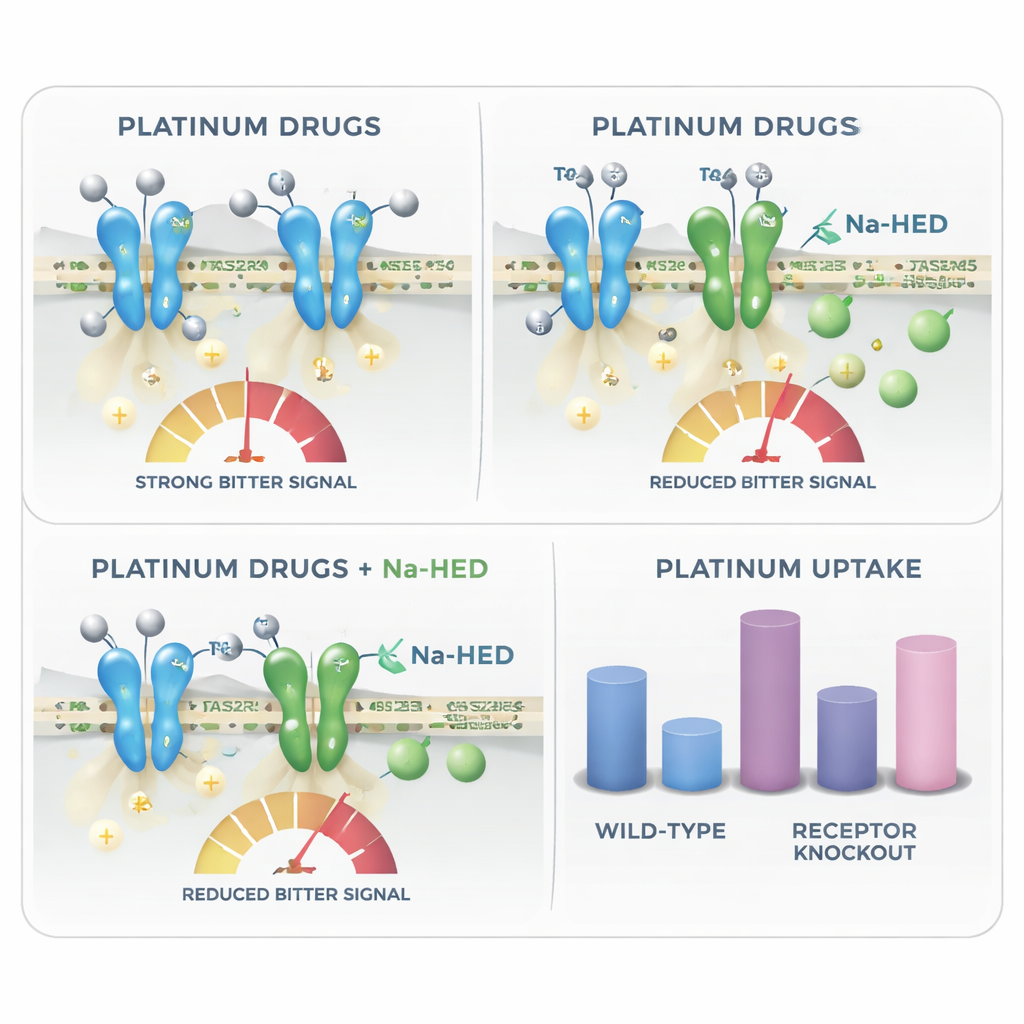
W kierunku łagodniejszych doznań smakowych podczas chemioterapii
Dla pacjentów główne przesłanie jest budujące: chemioterapia oparta na platynie wydaje się wywoływać problemy z gorzkim smakiem przez bezpośrednią aktywację receptorów gorzkich, które występują nie tylko na języku, ale także w komórkach przypominających jelitowe. Cisplatyna wydaje się w tym względzie szczególnie silna. Badanie pokazuje, że Na-HED może znacznie stłumić ten sygnał gorzkiego smaku w kontrolowanym systemie komórkowym i może także ograniczać miejscowe wchłanianie cisplatyny. Choć wyniki te wymagają potwierdzenia u ludzi, wskazują na przyszłe płukanki ustne typu „wypłucz i wypluj” zawierające Na-HED, które mogłyby złagodzić ostre odczucia gorzkie i metaliczne bez zakłócania ogólnoustrojowego działania przeciwnowotworowego leków.
Cytowanie: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Słowa kluczowe: zmiany smaku po chemioterapii, receptory smaku gorzkiego, cisplatyna i karboplatyna, związki maskujące gorycz, odżywianie pacjentów onkologicznych