Clear Sky Science · pl
Obliczenia DFT kompleksowania jonów Ac3+ i Bi3+ z hybrydowym chelatorem 3p-C-DEPA dla celowanej terapii alfa
Dlaczego to badanie ma znaczenie dla leczenia raka
Współczesna medycyna onkologiczna coraz częściej polega na lekach radioaktywnych, które potrafią tropić guzy komórka po komórce. Potężne podejście zwane celowaną terapią alfa wykorzystuje wysokoenergetyczne cząstki, które potrafią precyzyjnie zabić pojedyncze komórki nowotworowe. Aby dostarczyć te cząstki bezpiecznie, metal radioaktywny trzeba zamknąć w maleńkiej molekularnej „klatce”, aby nie przedostał się do zdrowych tkanek. W tym badaniu analizuje się nową molekułę-klatkę, 3p‑C‑DEPA, zaprojektowaną do utrzymywania szczególnie wymagających metali, takich jak aktyn‑225 i bizmut‑213, i stawia pytanie: czy potrafi je wiązać bardziej trwale niż stosowany dziś chelator referencyjny, DOTA?
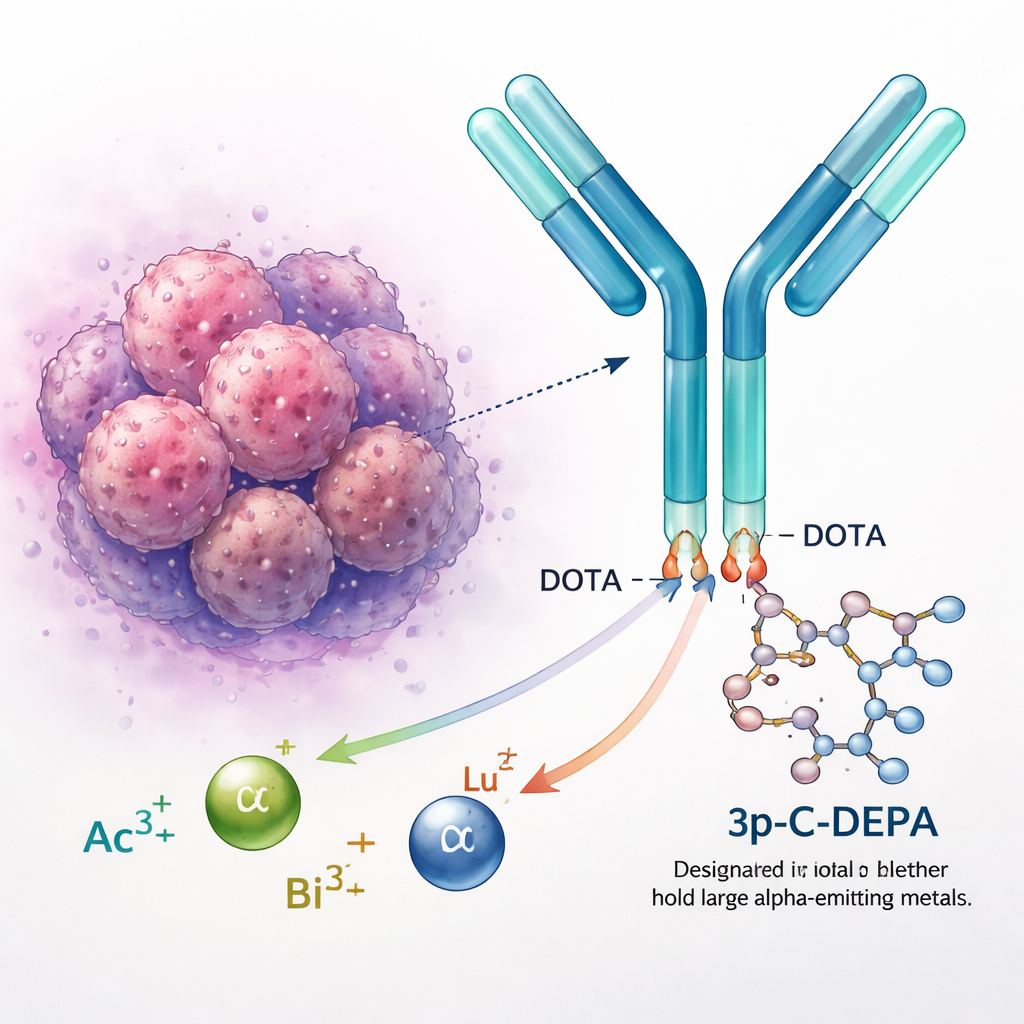
Bezpieczne unieruchamianie metali radioaktywnych
Metale radioaktywne, takie jak aktyn, bizmut i lutet, są wykorzystywane do diagnozy i leczenia raka. Same w sobie dodatnio naładowane jony metali mogą jednak swobodnie oddziaływać w organizmie, potencjalnie uszkadzając zdrowe narządy. Chemicy przyłączają je więc do „chelatorów”, pierścieniowych cząsteczek, które owijają metal i utrzymują go na miejscu. Chelator będący złotym standardem, DOTA, stosowany jest w kilku zatwierdzonych lekach, ale ma trudności z większymi, bardziej rozproszonymi jonami, takimi jak aktyn‑225. Te metale mogą z czasem uciekać, co rodzi obawy dotyczące długoterminowego bezpieczeństwa i ogranicza zastosowanie celowanej terapii alfa.
Hybrydowa klatka stworzona dla większych atomów
Nowy chelator, 3p‑C‑DEPA, łączy cechy dwóch ugruntowanych projektów: sztywną, pierścieniową strukturę DOTA oraz bardziej elastyczną, otwartą architekturę innego chelatora, DTPA. Ta hybrydowa budowa daje 3p‑C‑DEPA dziesięć silnych „rąk” wiążących (atomów azotu i tlenu) w porównaniu do ośmiu w DOTA oraz bardziej przestronną wnękę, która lepiej mieści duże jony metali. Wcześniejsze prace laboratoryjne sugerowały, że 3p‑C‑DEPA może szybko znakować przeciwciała w łagodnych warunkach i stabilnie utrzymywać radionuklidy bizmutu w surowicy krwi. Obecne badanie idzie o krok dalej, wykorzystując obliczenia na poziomie kwantowym do systematycznego porównania, jak dobrze 3p‑C‑DEPA i DOTA wiążą lutet‑177, bizmut‑213 i aktyn‑225.
Zajrzeć w molekularne uściskanie dłoni
Ponieważ praca bezpośrednio z krótkotrwałymi nadawcami alfa jest trudna, badacze sięgnęli po teorię funkcjonału gęstości (DFT) — mocną metodę obliczeniową, która szacuje, jak elektrony są rozmieszczone w cząsteczkach i jak silnie atomy do siebie przyciągają. Modelowali każdy jon metalu w wodzie, następnie jego kompleks z DOTA lub 3p‑C‑DEPA i obliczali zmianę energii swobodnej, gdy metal przechodzi z wody do „klatki” chelatora. Ta zmiana energii jest przekształcana w „stałą stabilności”: im wyższa wartość, tym mocniej chelator trzyma metal. Użyto dwóch różnych podejść DFT i dwóch modeli solwatacji, aby odwzorować realistyczne warunki roztworu i sprawdzić, czy obserwowane trendy są odporne na wybór pojedynczego ustawienia obliczeniowego.
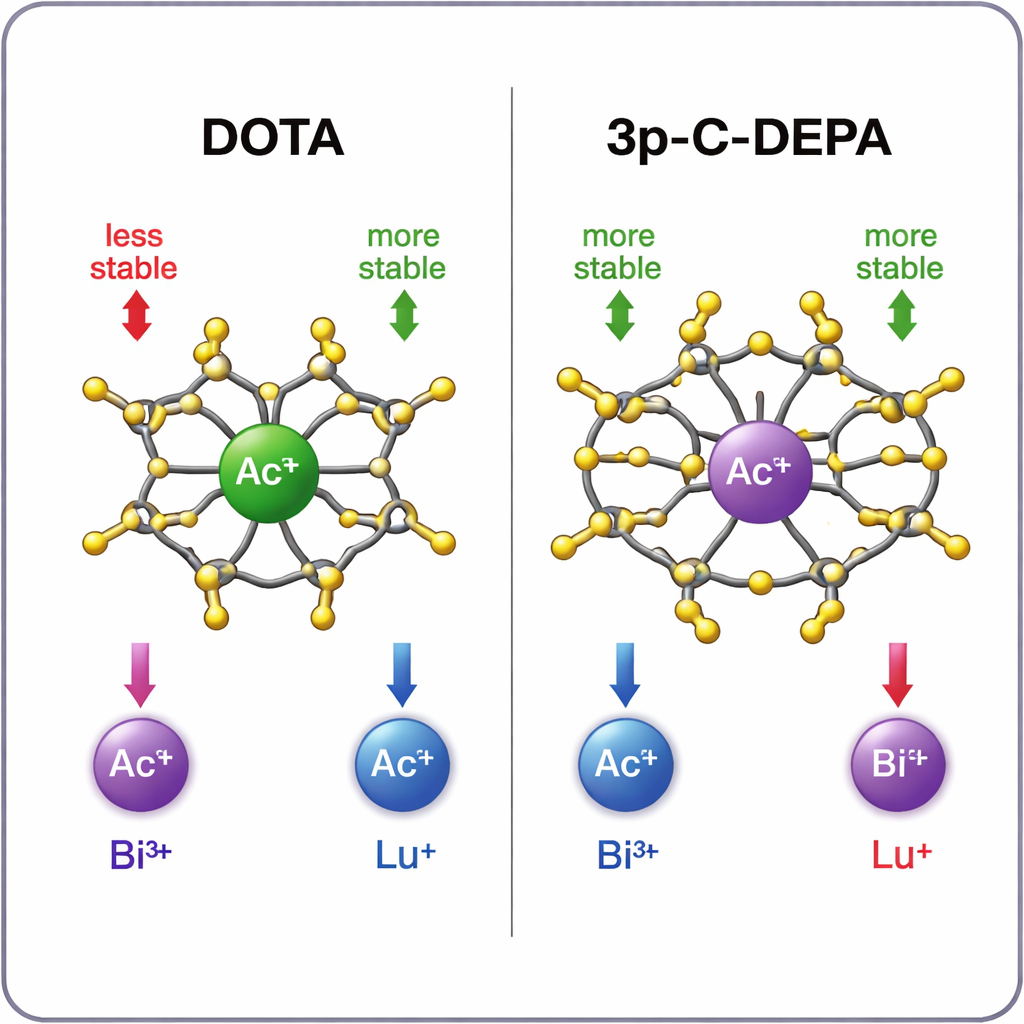
Która klatka trzyma który metal najlepiej?
Symulacje wykazują wyraźny wzorzec. Dla dużego jonu aktynu 3p‑C‑DEPA tworzy wyraźnie bardziej stabilny kompleks niż DOTA, dzięki swojej większej wnęce i większej liczbie donorów tlenu, które mogą chwycić metal. Bizmut‑213 także jest dobrze mieczony przez 3p‑C‑DEPA, korzystając z jego rozmiaru i charakteru akceptora elektronów, co dobrze współgra z grupami donorowymi chelatora. Natomiast mniejszy lutet‑177 lepiej pasuje do ciaśniejszego, ośmioramiennego środowiska DOTA. W 3p‑C‑DEPA nadmiar grup donorowych tłoczy się wokół małego jonu, generując oddziaływania odpychające, które zdają się spowalniać znakowanie i nieco osłabiać końcowy kompleks. Obliczone trendy stabilności dobrze zgadzają się z dostępnymi danymi eksperymentalnymi i wydajnością znakowania radiochemicznego, co dodaje wiarygodności przewidywaniom teoretycznym.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Mówiąc prościej, badanie sugeruje, że DOTA nie jest uniwersalną klatką: świetnie nadaje się do mniejszych metali, takich jak lutet, ale jest suboptymalna dla bardziej masywnych nadawców alfa, takich jak aktyn‑225. Natomiast 3p‑C‑DEPA zachowuje się jak specjalnie zaprojektowany uchwyt dla tych większych jonów — trzyma je mocniej i w łagodniejszych warunkach, które odpowiadają delikatnym molekułom celującym, takim jak przeciwciała. Choć potrzebne są dalsze prace eksperymentalne i kliniczne, obliczenia wskazują, że 3p‑C‑DEPA jest obiecującym szkieletem dla bezpieczniejszych i efektywniejszych celowanych terapii alfa — potencjalnie poszerzając dostęp do wysoce skutecznych terapii przeciwnowotworowych, które mogą wyniszczać guzy, oszczędzając otaczające tkanki zdrowe.
Cytowanie: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
Słowa kluczowe: celowana terapia alfa, leki radiofarmaceutyczne, projektowanie chelatorów, aktyn-225, teoria funkcjonału gęstości