Clear Sky Science · pl
Podejście proteomiczne i redoks-proteomiczne do zrozumienia heterogenności ARDS
Dlaczego to ma znaczenie dla osób na intensywnej terapii
Ostra niewydolność oddechowa (ARDS) to zagrażająca życiu postać niewydolności płuc, która może dotknąć osób z ciężkimi zakażeniami, urazami lub innymi poważnymi chorobami. Wielu pacjentów z ARDS wygląda podobnie przy łóżku chorego, a mimo to niektórzy wracają do zdrowia, podczas gdy inni umierają, i nie ma leku udowodnionego jako specyficznie odwracającego zespół. To badanie stawia proste, lecz istotne pytanie: czy dokładna analiza białek i reakcji chemicznych w płucach i krwi pacjentów z ARDS pozwoli ujawnić ukryte biologiczne „typy” choroby, które wyjaśniają, dlaczego los pacjentów tak się różni?
Patrzeć do wnętrza płuc, nie tylko do krwi
Aby to zbadać, naukowcy obserwowali 16 dorosłych pacjentów na oddziale intensywnej terapii z ARDS, będących na respiratorze. W ciągu pierwszych trzech dni od rozpoznania pobrali krew oraz specjalny materiał zwany płynem z płukania oskrzelowo‑pęcherzykowego (BAL), czyli delikatny „pranie” pęcherzyków płucnych. W miarę możliwości powtarzano pobrania przez kilka kolejnych dni. Za pomocą zaawansowanej spektrometrii mas zmierzono setki białek w każdym próbce (proteomika) i, co kluczowe, zbadano także stopień ich utlenienia (redoks‑proteomika), co odzwierciedla, jak bardzo zostały uszkodzone lub regulowane przez reaktywne formy tlenu — chemicznie agresywne produkty zapalenia.
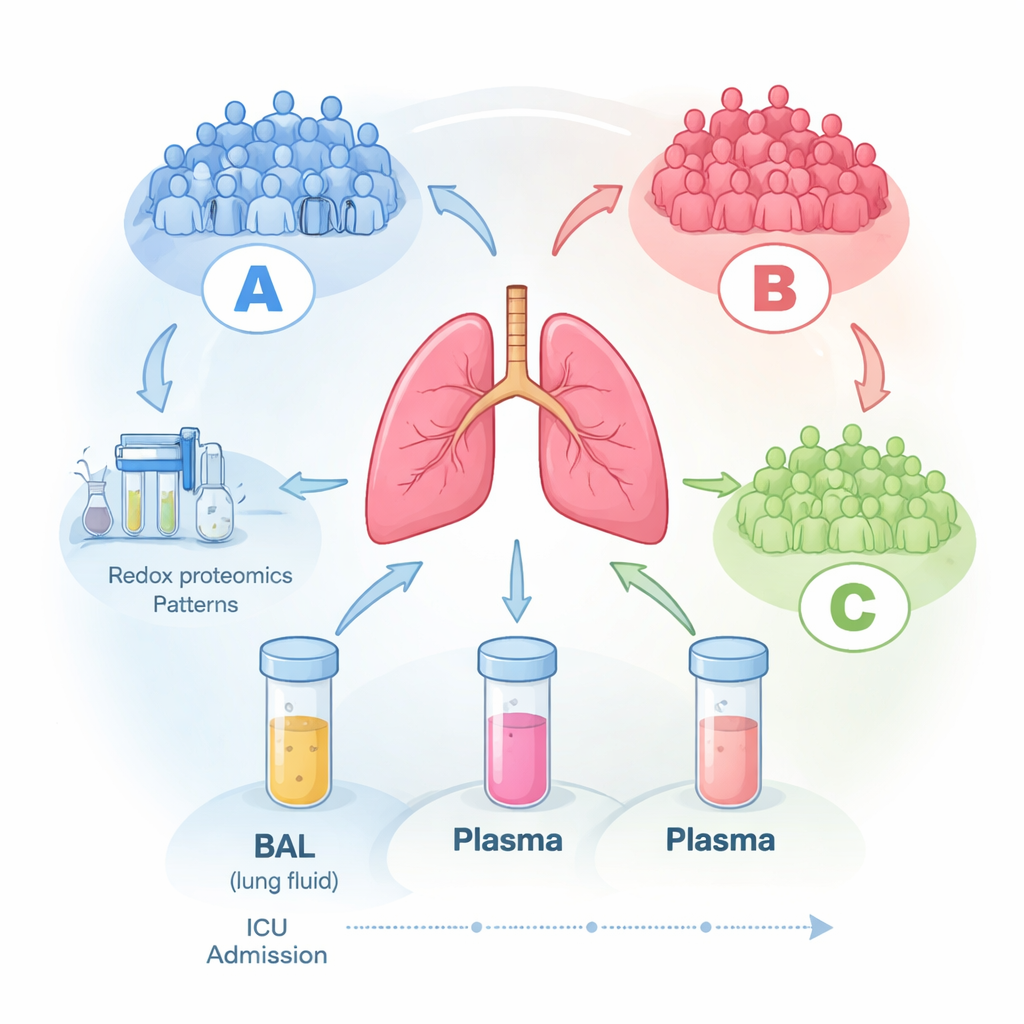
Pojawiają się trzy ukryte grupy pacjentów
Gdy pozwolono danym same się pogrupować bez podawania komputera informacji o pacjentach, w próbkach płynu z płuc ujawnił się wyraźny wzorzec: trzy odrębne grupy molekularne, oznaczone A, B i C. Pacjenci z grupy A mieli skłonność do cięższego przebiegu przy włączeniu do badania, podczas gdy grupy B i C miały łagodniejszą chorobę. Co istotne, te molekularne sygnatury pozostawały w dużej mierze stabilne przez okres do sześciu dni na OIT, sugerując, że każdy pacjent mieści się w stosunkowo stałym wzorcu biologicznym, zamiast przypadkowo zmieniać się z dnia na dzień. Standardowe miary przy łóżku — takie jak poziomy tlenu, długość pobytu czy ogólne skale ciężkości — nie korelowały dobrze z tymi molekularnymi podziałami, co sugeruje, że powszechne narzędzia kliniczne nie wychwytują kluczowej biologii zachodzącej w płucach.
Stres oksydacyjny i mechanizmy obronne organizmu
Głównym motywem przewijającym się przez dane była równowaga między szkodliwymi reaktywnymi formami tlenu a antyoksydacyjnymi mechanizmami obronnymi organizmu. W grupie A, najcięższej, wiele białek płucnych zaangażowanych w produkcję energii i utrzymanie komórkowego porządku występowało na niższych poziomach. Co jeszcze ważniejsze, istotne enzymy antyoksydacyjne, takie jak peroksiredoksyny, białka związane z glutationem, thioredoksyna i katalaza, były znacząco zredukowane. W przeciwieństwie do tego grupy B, a zwłaszcza C, miały wyższe poziomy tych ochronnych białek, co sugeruje, że ich płuca były lepiej przygotowane do detoksykacji szkodliwych utleniaczy i ograniczania szkód wtórnych zapalenia. Wzorce dotyczące stanu oksydacyjnego białek dodały kolejną warstwę informacji, pokazując różne podzbiory utlenionych białek wzbogacone w grupach o największej i najmniejszej ciężkości.
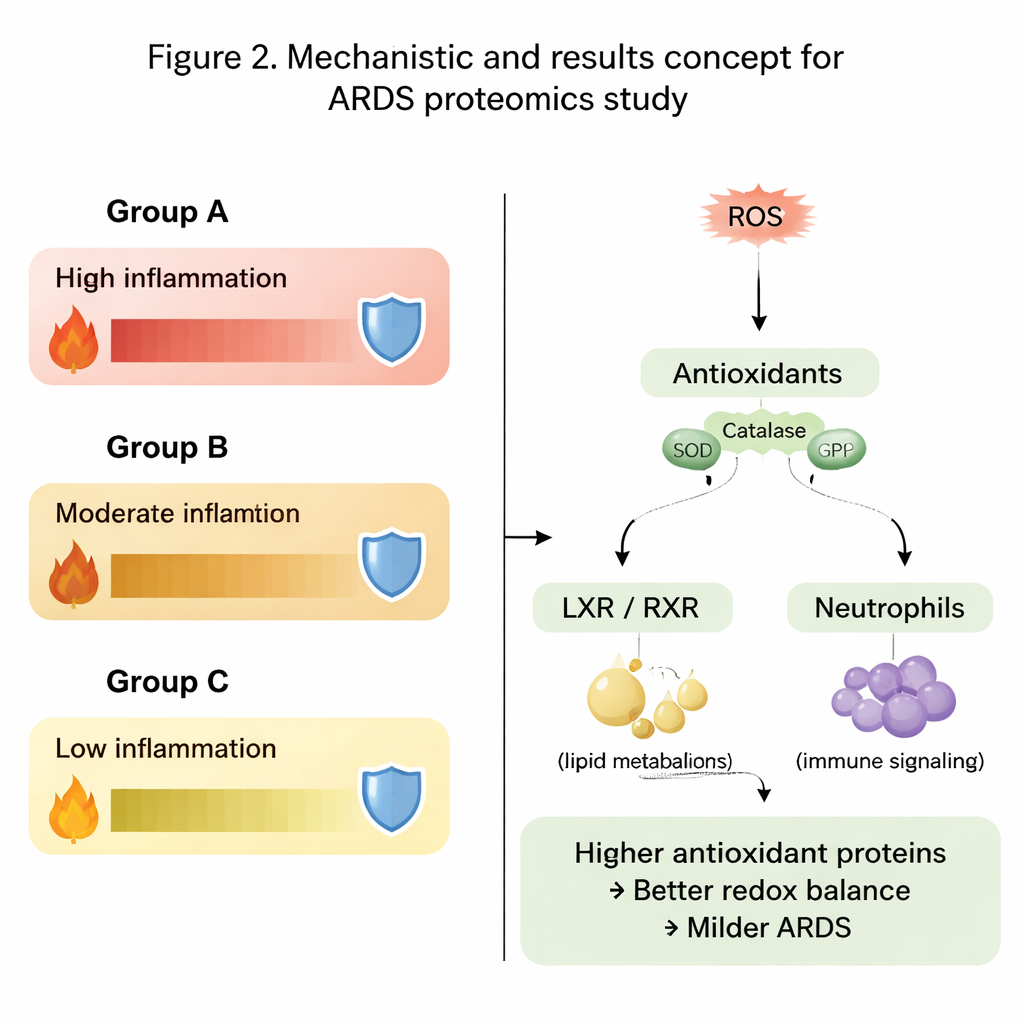
Szlaki sygnałowe kształtujące zapalenie
Ponad pojedynczymi białkami autorzy zbadali całe szlaki biologiczne. Stwierdzili, że ścieżki związane z zapaleniem, metabolizmem cholesterolu i lipidów oraz aktywnością komórek odpornościowych zachowywały się odmiennie w trzech grupach. Szczególnie wyróżniały się sygnały powiązane z receptorem LXR/RXR i enzymem DHCR24, które razem regulują zarówno metabolizm lipidów, jak i odpowiedzi immunologiczne. W najcięższej grupie te szlaki były przewidywane jako bardziej aktywne, w połączeniu z obniżonym sygnałem cytokinowym interleukiny‑12. Równocześnie szlaki związane z reaktywnymi formami tlenu, ich detoksykacją i aktywnością neutrofili wykazywały kontrastujące wzorce między płynem płucnym a krwią, podkreślając, że to, co dzieje się lokalnie w płucu, może różnić się od obserwowanego w krążeniu.
Co to może znaczyć dla przyszłej opieki
To niewielkie, eksploracyjne badanie nie zmienia dziś sposobu leczenia i jego ustalenia trzeba potwierdzić w znacznie większych grupach pacjentów. Pokazuje jednak, że dzięki dokładnemu profilowaniu białek i ich stanu redoks bezpośrednio w płynie z płuc — zamiast polegać wyłącznie na badaniach krwi czy wynikach przy łóżku chorego — można wyróżnić biologicznie istotne podtypy ARDS. Podtypy te różnią się nasileniem stresu oksydacyjnego, zdolnością antyoksydacyjną, metabolizmem i sygnalizacją immunologiczną oraz pozostają stosunkowo stabilne w ciągu pierwszych krytycznych dni choroby. W przyszłości takie molekularne odciski palców mogą pomóc lekarzom precyzyjniej klasyfikować pacjentów z ARDS, dobierać ukierunkowane terapie odpowiadające konkretnym wzorcom i projektować bardziej przemyślane badania kliniczne z większą szansą znalezienia naprawdę skutecznych terapii.
Cytowanie: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
Słowa kluczowe: ostra niewydolność oddechowa, proteomika, stres oksydacyjny, PŁUKANIE OSKRZELOWO‑PĘCHERZYKOWE, opieka krytyczna