Clear Sky Science · pl
Dysfunkcja mitochondriów i zaburzenia regulacji Ca2+ w ludzkich neuronach pochodzących z iPSC z mutacją preseniliny‑1 ujawniają się pod wpływem stresu przez mechanizm niezależny od MCU‑1
Dlaczego ma to znaczenie dla choroby Alzheimera
Choroba Alzheimera bywa zwykle opisywana przez pryzmat lepkich złogów białkowych w mózgu, ale na długo przed utratą pamięci mogą już nieprawidłowo funkcjonować malutkie „elektrownie” komórek nerwowych — mitochondria — oraz gospodarka jonami wapnia. Badanie to wykorzystuje ludzkie neurony wyhodowane z komórek skóry osoby noszącej znaną rodziną mutację Alzheimera, by zadać proste, lecz kluczowe pytanie: jak wcześnie i w jaki sposób zaczynają zawodzić produkcja energii i równowaga wapniowa?
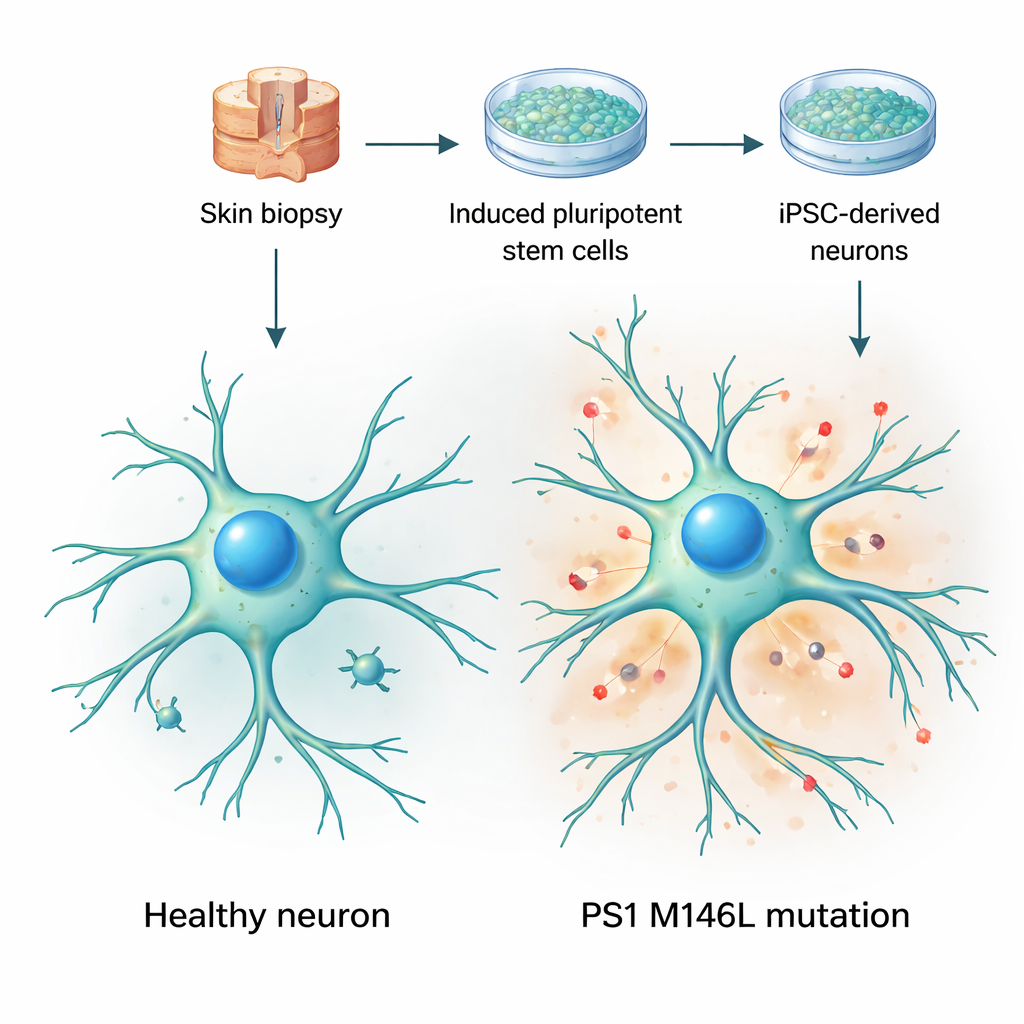
Przekształcanie komórek skóry w żywe modele mózgu
Naukowcy zaczęli od biopsji skóry pobranych od dwóch kobiet: jednej zdrowej ochotniczki oraz jednej bezobjawowej nosicielki mutacji preseniliny‑1 o nazwie M146L, występującej w argentyńskiej rodzinie z wczesnym początkiem choroby Alzheimera. Przeprogramowali komórki skóry do postaci indukowanych pluripotencjalnych komórek macierzystych — komórek zdolnych do przekształcenia się niemal w każdy rodzaj tkanki — a następnie nakierowali je na różnicowanie w neurony. W ciągu kilku tygodni hodowli komórki te przyjmowały typowe neuronalne kształty, wydłużały rozgałęzione wypustki i wyrażały standardowe markery neuronalne. Co ważne, zarówno komórki kontrolne, jak i mutacyjne dojrzewały w podobnym tempie i wyglądały ogólnie zdrowo, co pozwoliło badaczom skupić się na subtelnych zmianach funkcjonalnych, a nie na widocznej utracie lub uszkodzeniu komórek.
Sygnały elektryczne i wapń pod obciążeniem
Komórki nerwowe polegają na precyzyjnej kontroli wapnia — naładowanego atomu, który działa jak szybki włącznik i wyłącznik dla wielu procesów komórkowych. Używając barwników fluorescencyjnych, zespół śledził zmiany poziomów wapnia wewnątrz komórek podczas stymulacji elektrycznej potasem lub aktywacji za pomocą cząsteczek sygnałowych. Przy prostym depolaryzującym pobudzeniu neurony z mutacją M146L wykazywały słabsze wzrosty wapnia niż neurony kontrolne, co sugeruje problemy z utrzymaniem gradientów elektrycznych i jonowych, które normalnie napędzają napływ Ca2+. Jednak gdy badacze wywołali bardziej stresującą sytuację — wymusili wypływ wapnia z wewnętrznych magazynów w retikulum endoplazmatycznym — różnica stała się wyraźniejsza. W odpowiedzi na ten stres mitochondria w neuronach mutacyjnych pobierały znacząco mniej wapnia niż w komórkach kontrolnych, wskazując na zmniejszoną zdolność buforowania groźnych napływów Ca2+.
Oddzielenie wykorzystania energii od równowagi wapniowej
Aby zrozumieć, jak zmienione obchodzenie się z wapniem wpływa na metabolizm komórek, badacze mierzyli zużycie tlenu przez neurony — bezpośredni wskaźnik aktywności mitochondrialnej. Ku zaskoczeniu, neurony z mutacją M146L „oddychały” mocniej: ich podstawowe i maksymalne wskaźniki zużycia tlenu oraz ilość tlenu związana z produkcją ATP były wyższe niż w komórkach kontrolnych. Jednak efektywność sprzężenia wykorzystania tlenu z produkcją ATP wyglądała podobnie, i nie zaobserwowano wzrostu liczby mitochondriów ani kluczowych enzymów tworzących ATP. Zamiast tego mitochondria w neuronach mutacyjnych były dłuższe i bardziej rurkowate, z wyższymi poziomami białka fuzyjnego mitofusyny‑1 — wzorzec często obserwowany w komórkach poddanych przewlekłemu, niskopoziomowemu stresowi. Te nadaktywne, wydłużone mitochondria generowały również więcej reaktywnych form tlenu, niestabilnych cząsteczek, które mogą uszkadzać białka i DNA, jeśli nie zostaną odpowiednio zneutralizowane.
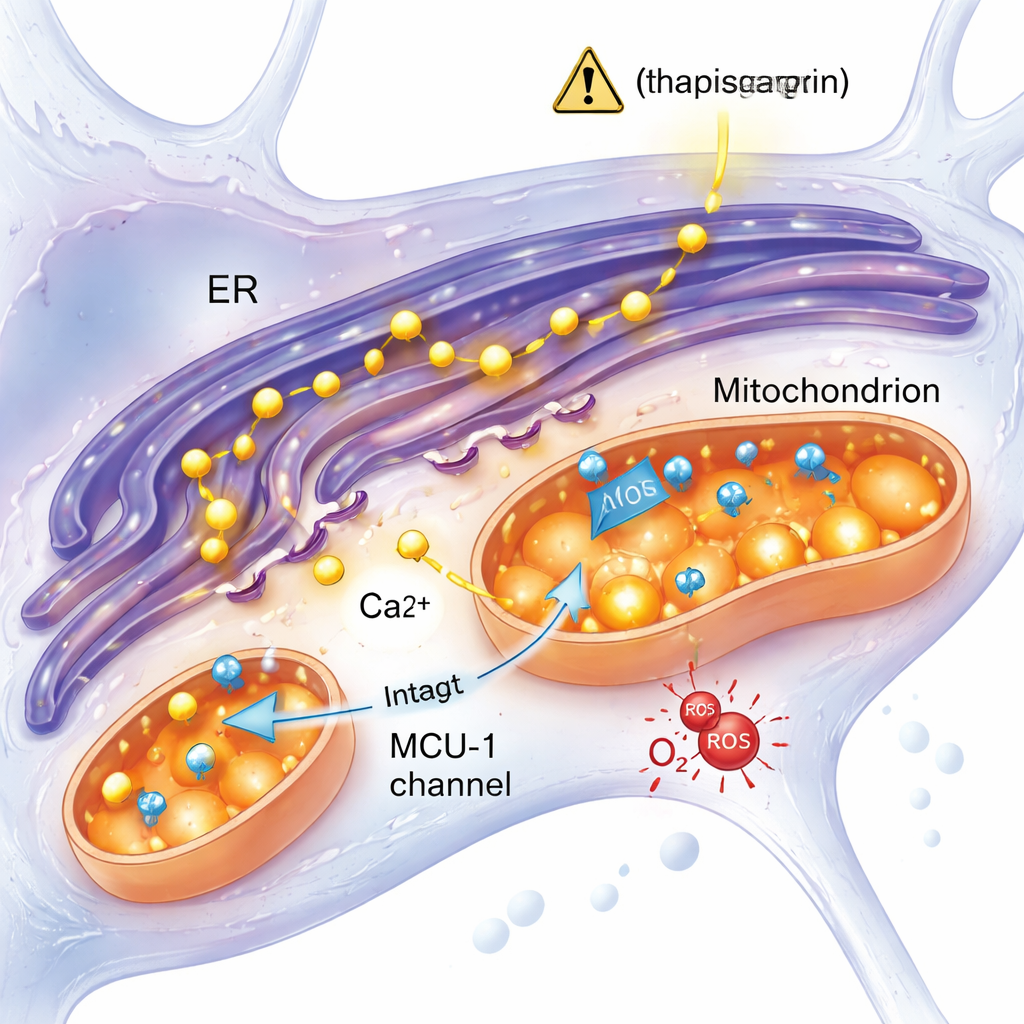
Odpowiedź na stres niezależna od kluczowego kanału wapniowego
Jedna z wiodących hipotez w badaniach nad Alzheimerem głosi, że nadmiar wapnia z retikulum endoplazmatycznego wlewa się do mitochondriów przez kanał zwany uniporterem wapniowym mitochondrium (MCU‑1), przeciążając je i powodując dysfunkcję. Badanie to przetestowało tę ideę bezpośrednio. Gdy zespół zablokował MCU‑1 przy użyciu specyficznego inhibitora, zarówno neurony kontrolne, jak i mutacyjne wykazały silne ograniczenie pobierania wapnia przez mitochondria, co potwierdza, że sam kanał funkcjonował w obu grupach. Co więcej, gdy uwolnienie wapnia zostało wywołane przez bardziej fizjologiczną ścieżkę z udziałem receptora IP3 — kolejnej istotnej bramy wapniowej — komórki mutacyjne i kontrolne reagowały podobnie. Wyniki te odciągają uwagę od uszkodzonego kanału MCU‑1 i sugerują raczej, że zmienione są fizyczne i funkcjonalne kontakty między retikulum endoplazmatycznym a mitochondriami, bądź inne aspekty ich interakcji, w neuronach mutacyjnych.
Co to znaczy dla zrozumienia i leczenia choroby
Podsumowując, wyniki kreślą obraz ludzkich neuronów niosących mutację PS1 M146L jako komórek, które w spoczynku wyglądają normalnie, ale reagują nieprawidłowo pod wpływem stresu. Ich mitochondria nie pobierają wystarczająco dużo wapnia przy nagłym uwolnieniu z magazynów wewnętrznych, a jednocześnie pracują intensywniej — zużywając więcej tlenu i generując więcej reaktywnych form tlenu — jakby utknęły w kosztownym trybie kompensacyjnym. Ponieważ dzieje się to w żywych neuronach pochodzących od ludzi, zanim pojawią się jakiekolwiek objawy kliniczne, badanie wspiera pogląd, że zaburzona sygnalizacja wapniowa i wczesne nadmierne obciążenie mitochondriów są zdarzeniami wyprzedzającymi w chorobie Alzheimera, a nie tylko późnymi produktami ubocznymi. Dla osób niebędących specjalistami kluczowy przekaz jest taki: utrzymanie równowagi między sygnałami wapniowymi a produkcją energii mitochondrialnej może być równie istotne w zapobieganiu chorobie, jak ukierunkowanie się na lepiej znane płytki amyloidowe.
Cytowanie: Wilson, C., Galeano, P., Remedi, M.M. et al. Mitochondrial dysfunction and Ca2+ dysregulation in human iPSC-derived neurons carrying presenilin-1 mutation arise under stress via an MCU-1-independent mechanism. Sci Rep 16, 6002 (2026). https://doi.org/10.1038/s41598-026-35597-0
Słowa kluczowe: choroba Alzheimera, mitochondria, sygnalizacja wapniowa, mutacja preseniliny‑1, neurony pochodzące z iPSC