Clear Sky Science · pl
Immunotesty do wykrywania i różnicowania Paenibacillus larvae, czynnika etiologicznego zgnilca amerykańskiego (AFB) u pszczół miodnych
Dlaczego choroba czerwiu pszczół ma znaczenie dla nas wszystkich
Pszczoły miodne robią znacznie więcej niż tylko produkują miód. Poprzez zapylanie upraw i roślin dziko rosnących pomagają zabezpieczyć nasze zaopatrzenie w żywność i utrzymać sprawne funkcjonowanie ekosystemów. Jednym z najbardziej niszczycielskich zagrożeń dla rodzin pszczelich jest bakteryjna choroba młodych, zwana zgnilcem amerykańskim. Gdy zadomowi się w ulu, może zniszczyć całą rodzinę i szybko szerzyć się na sąsiednie ule. W tym badaniu opisano nowe szybkie testy, które ułatwiają wczesne wykrycie choroby oraz określenie, która forma bakterii jest za nią odpowiedzialna, dając pszczelarzom i lekarzom weterynarii większe szanse na powstrzymanie ognisk, zanim wymkną się spod kontroli.
Śmiertelna choroba dziecięca pszczół
Zgnilec amerykański atakuje larwy pszczół miodnych, rozwijający się czerwi, który ma stać się robotnicami i matkami. Sprawcą jest przetrwalnikotwórcza bakteria Paenibacillus larvae. Jej przetrwalniki mogą przetrwać lata w starych plastrach i na wysuszonych pozostałościach larw, a do zakażenia wystarczy, że młoda larwa połknie zaledwie kilka przetrwalników. W miarę rozmnażania się bakterii larwa zapada się w lepką masę, która później wysycha do ciemnej łuski mocno przyklejonej do komórki. Te łuski zawierają miliony przetrwalników i stanowią długotrwałe rezerwuary zakażenia, które zbieraczki i pszczelarze mogą nieumyślnie przenosić między rodzinami i pasiekami.
Dwie odmiany tego samego zabójcy
Nie wszystkie szczepy P. larvae są jednakowo groźne w tym samym sensie. Na świecie dominują dwa główne typy genetyczne, znane jako ERIC I i ERIC II, które odpowiadają za niemal wszystkie obecne ogniska. Oba są śmiertelne, ale używają różnych narzędzi, by przejść przez przewód pokarmowy larwy i zaatakować ciało. Wszystkie zjadliwe szczepy wydzielają silny enzym degradujący chitynę, zwany PlCBP49, który pomaga im przegryzać ochronną wyściółkę jelit. Szczepy ERIC I wytwarzają także klasyczne toksyny bezpośrednio uszkadzające komórki jelit, podczas gdy szczepy ERIC II polegają na białku powierzchniowym zwanym SplA, które pomaga im przyczepiać się i następnie niszczyć barierę jelitową drogą, która wciąż nie jest do końca poznana. Ponieważ ERIC I i ERIC II różnią się tempem zabijania larw i przebiegiem ogniska, wiedza o tym, który typ występuje, może wpływać na decyzje dotyczące kontroli choroby.
Przekształcenie bakteryjnych „broni” w cele diagnostyczne
Autorzy zauważyli, że te czynniki zjadliwości — PlCBP49 i SplA — mogą zostać wykorzystane jako wysoce specyficzne markery. Jeśli test wykryje PlCBP49, wskaże zakażenie przez dowolny zjadliwy szczep P. larvae. Jeśli wykryje także SplA, zasygnalizuje konkretnie typ ERIC II. Aby to osiągnąć, zespół otrzymał oczyszczone wersje obu białek, a następnie wykorzystał je do wytworzenia zestawów przeciwciał monoklonalnych: laboratoryjnych białek wiążących się jedynie z pojedynczym celem molekularnym. Przeciwciała przetestowano starannie metodami dot blot i western blot przeciwko wielu szczepom ERIC I i ERIC II oraz przeciwko ponad 20 innym gatunkom bakterii powszechnie występującym w miodzie i plastrach czerwiu. Jedno przeciwciało przeciw PlCBP49 i jedno przeciw SplA okazały się szczególnie selektywne, rozpoznając wszystkie właściwe szczepy P. larvae i ignorując podobne bakterie ze środowiska ula.
Z laboratoryjnych płytek do testu przy ulu
Mając odpowiednie przeciwciała, badacze skonstruowali dwa laboratoryjne zestawy typu sandwich ELISA oraz jeden paskowy test strumieniowy (lateral flow), podobny w koncepcji do testu ciążowego lub testu na COVID-19 wykonywanego w domu. W ELISAch jedno przeciwciało wychwytuje docelowe białko z homogenizowanej larwy, a drugie znakowane przeciwciało ujawnia jego obecność poprzez zmianę barwy na plastikowej mikropłytce. Testy na eksperymentalnie zakażonych larwach wykazały, że ELISA dla PlCBP49 wykryła 89% zakażonych osobników bez fałszywych pozytywów, podczas gdy ELISA dla SplA wykryła 94% larw zakażonych ERIC II i poprawnie rozróżniła ERIC II od ERIC I z dokładnością 97%. W oparciu o te same pary przeciwciał zespół zaprojektował dwuliniowy pasek lateral flow z dwiema liniami testowymi: jedną dla PlCBP49 (wszystkie P. larvae) i jedną dla SplA (tylko ERIC II). Gdy próbki larw z infekcji laboratoryjnych i rzeczywistych ognisk przepuszczano przez paski, test poprawnie identyfikował P. larvae w 95–99% zakażonych larw i wykazywał specyficzność 96–100%, przy czym około 9 na 10 rozpoznań genotypu (ERIC I vs ERIC II) było sklasyfikowanych prawidłowo.
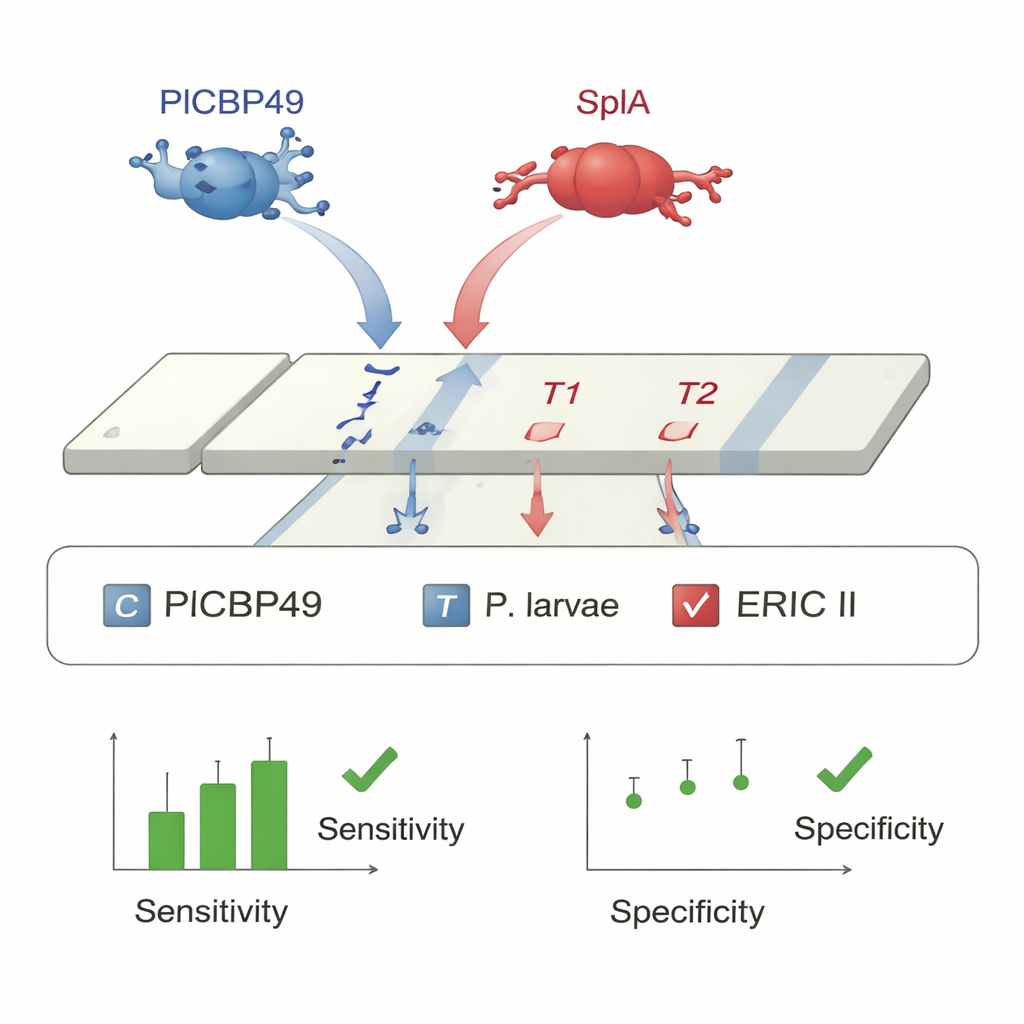
Co to oznacza dla pszczół i pszczelarzy
Obecnie potwierdzenie zgnilca amerykańskiego często wymaga wysyłki podejrzanych plastrów lub larw do wyspecjalizowanego laboratorium w celu hodowli lub testów DNA, co może trwać dniami lub tygodniami, podczas gdy choroba nadal się szerzy. Nowe zestawy ELISA dają laboratoriom szybszy, automatyzowalny sposób przesiewania wielu próbek, natomiast dwuliniowy pasek lateral flow może być używany bezpośrednio przy ulu jako test przyłóżkowy. Pszczelarz lub inspektor może pobrać kilka podejrzanych larw, wykonać test w ciągu kilku minut i dowiedzieć się nie tylko, czy P. larvae jest obecny, ale także, czy zaangażowany jest szybciej działający typ ERIC II. To połączenie szybkości, dokładności i możliwości użycia w terenie ma potencjał, by odmienić kontrolę zgnilca: wcześniejsze wykrycie oznacza wcześniejszą interwencję, mniej utraconych rodzin i lepszą ochronę usług zapylania, od których zależą rolnictwo i ekosystemy naturalne.
Cytowanie: Reinecke, A., Göbel, J. & Genersch, E. Immunoassays for the detection and differentiation of Paenibacillus larvae, the etiological agent of American foulbrood (AFB) in honey bees. Sci Rep 16, 2635 (2026). https://doi.org/10.1038/s41598-026-35590-7
Słowa kluczowe: choroba pszczół miodnych, zgnilec amerykański, Paenibacillus larvae, szybki test diagnostyczny, test strumieniowy (lateral flow)