Clear Sky Science · pl
Strukturalne i obliczeniowe wspomaganie rozwoju analogów 2,5-dodisubstytuowanych-1,3,4-oksadiazoli jako aktywnych inhibitorów LOX, ureazy i α-glukozydazy
Nowe narzędzia chemiczne do walki z powszechnymi chorobami
Wiele codziennych problemów zdrowotnych — od wrzodów i kamieni nerkowych po cukrzycę i przewlekłe zapalenia — jest napędzanych przez nadmiernie aktywne enzymy w organizmie. W tym badaniu zbadano rodzinę nowo zaprojektowanych małych cząsteczek, które działają jak drobne hamulce dla trzech takich enzymów. Poprzez dopracowanie ich struktury i testy w laboratorium oraz za pomocą symulacji komputerowych, badacze dążą do stworzenia podstaw pod skuteczniejsze i bezpieczniejsze leki w przyszłości. 
Dlaczego te enzymy są ważne
Zespół skupił się na trzech celach enzymatycznych, które odgrywają bardzo różne, lecz równie istotne role dla zdrowia. Ureaza pomaga rozkładać mocznik; gdy jest nadaktywowana w niektórych bakteriach lub tkankach, może przyczyniać się do wrzodów żołądka i dróg moczowych, tworzenia kamieni nerkowych, a także do podwyższonego ciśnienia krwi. Alfa-glukozydaza znajduje się na powierzchni komórek jelitowych i rozkłada złożone węglowodany do glukozy; jej hamowanie jest dobrze znaną metodą kontrolowania poziomu cukru we krwi w cukrzycy typu 2. Lipooksygenaza (LOX) przekształca tłuszcze w molekuły sygnalizacyjne, które napędzają zapalenie, astmę oraz niektóre procesy związane z rakiem. Dlatego poszukuje się leków obniżających aktywność tych enzymów bez szkody dla innych układów organizmu.
Budowanie biblioteki kandydatów
Aby poszukać takich leków, badacze zbudowali serię 15 powiązanych związków opartych na układzie pierścieniowym zwanym 1,3,4-oksadiazolem połączonym z jednostką piperydynową. Ten chemiczny szkielet występuje już w kilku nowoczesnych lekach i jest znany z dobrej interakcji z celami biologicznymi. Zespół zmieniał „ozdoby” przyczepione do rdzenia — małe grupy takie jak metyl, etyl, metoksy, benzyl i cykloheksyl — w różnych pozycjach, tworząc niewielką bibliotekę kandydatów oznaczonych 7a–7o. Każdą strukturę potwierdzono za pomocą standardowych narzędzi analitycznych, takich jak spektroskopia w podczerwieni i magnetycznego rezonansu jądrowego, upewniając się, że otrzymane związki odpowiadają projektom.
Testowanie zdolności cząsteczek do hamowania enzymów
Każdy związek następnie testowano przeciwko oczyszczonym LOX, ureazie i alfa-glukozydazie, aby ocenić, jak silnie potrafi spowolnić aktywność enzymu. Kilka molekuł wyróżniało się. W przypadku alfa-glukozydazy związki 7a i 7n były szczególnie efektywne, przewyższając w testach laboratoryjnych standardowy lek przeciwcukrzycowy akarbazę, osiągając duże procenty zahamowania przy niskich stężeniach mikromolowych. Dla LOX związki 7a, 7h i 7n wykazały bardzo silną aktywność, w niektórych przypadkach lepszą niż naturalny inhibitor referencyjny, kwercetyna. W testach ureazy związki 7a, a zwłaszcza 7l, dorównywały lub nieco przewyższały standardowy inhibitor tiomocznik, co sugeruje, że mogłyby w przyszłości posłużyć jako prowadzenia do terapii przeciwwrzodowych lub przeciwkamiennych. 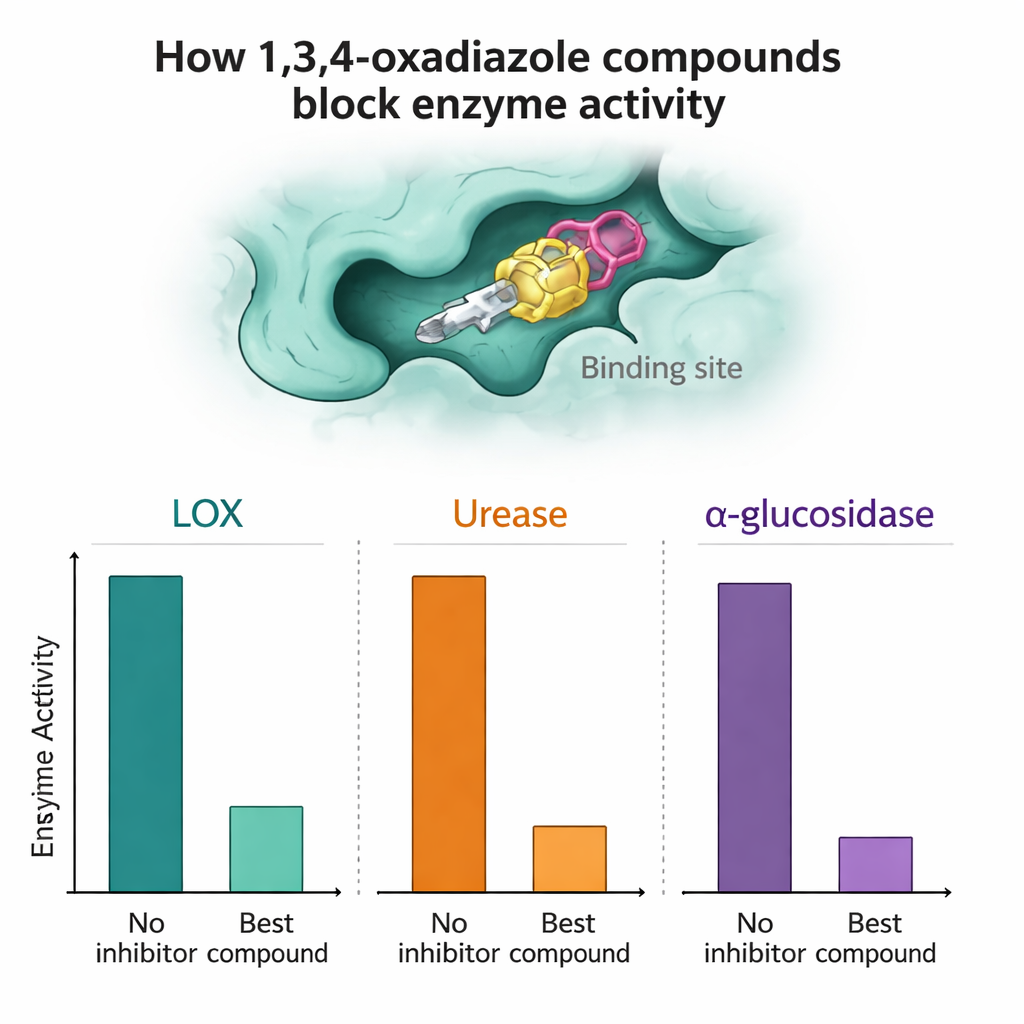
Łączenie struktury z aktywnością
Ponieważ jedynymi różnicami między związkami 7a–7o są niewielkie zmiany wokół rdzenia pierścienia, badacze mogli zacząć mapować proste relacje struktura–aktywność. Na przykład dodanie małych grup węglowodorowych w określonych pozycjach „orto” na przyłączonym pierścieniu często zwiększało zdolność do hamowania alfa-glukozydazy lub LOX. Inne podstawienia, takie jak niektóre grupy metoksy lub estry umieszczone mniej korzystnie, miały tendencję do osłabiania aktywności. Aby zrozumieć dlaczego, zespół zastosował symulacje komputerowe. Obliczenia kwantowo-chemiczne wykazały, że wszystkie molekuły były termodynamicznie stabilne i wystarczająco elastyczne, by dopasować się do kieszeni enzymów. Badania dokowania — wirtualne dopasowanie każdej cząsteczki do trójwymiarowych modeli enzymów — ujawniły, że najbardziej aktywne związki nawiązywały ciaśniejszy kontakt poprzez kombinację wiązań wodorowych i oddziaływań hydrofobowych (oleistych) w kluczowych miejscach w centrach aktywnych, podczas gdy słabsze kandydaty siedziały luźniej lub nie nawiązywały krytycznych punktów styku.
Co to oznacza dla przyszłych leków
Mówiąc obrazowo, badanie identyfikuje garść obiecujących „kluczy”, które dobrze pasują do trzech związanych z chorobami „zamków” i zaczyna wyjaśniać na poziomie atomowym, dlaczego jedne klucze działają lepiej od innych. Żadne z tych molekuł nie jest jeszcze gotowe na lek — wciąż wymagają testów bezpieczeństwa, optymalizacji zachowania w organizmie oraz prób na zwierzętach i ludziach. Jednak praca pokazuje, że rama 1,3,4-oksadiazol–piperidyna jest żyznym punktem wyjścia dla przyszłych terapii ukierunkowanych na cukrzycę, stany zapalne i zaburzenia związane z ureazą. Połączenie starannych pomiarów laboratoryjnych z szczegółowym modelowaniem komputerowym dostarcza drogowskazu do dopracowania tych kandydatów w bardziej precyzyjne i skuteczne leki.
Cytowanie: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Słowa kluczowe: inhibitory enzymów, odkrywanie leków, związki oksadiazolowe, cukrzyca i zapalenie, ureaza i lipooksygenaza