Clear Sky Science · pl
SHP2 promuje osteosarcomę poprzez regulację sygnalizacji STAT3/TET3/HOXB2
Dlaczego to badanie o raku kości ma znaczenie
Osteosarcoma jest najczęstszym pierwotnym nowotworem kości u dzieci i nastolatków, a mimo współczesnej chemioterapii i chirurgii przeżycie pacjentów z zaawansowaną lub nawrotową chorobą od dekad ulegało niewielkiej poprawie. To badanie analizuje wewnętrzne okablowanie komórek osteosarcomy, aby ustalić, które cząsteczki działają jak „główne wyłączniki”, pomagające guzom rosnąć, rozsiewać się i opierać leczeniu. Odkrycie kluczowej ścieżki kontrolnej skupionej wokół białka SHP2 wskazuje na nowe cele lekowe, które w przyszłości mogą uczynić terapie osteosarcomy skuteczniejszymi i bardziej precyzyjnymi.
Idąc za wskazówkami aktywności genów guza
Naukowcy zaczęli od potraktowania osteosarcomy jako problemu danych. Przeanalizowali publiczne zestawy danych ekspresji genów porównujące próbki nowotworowe z normalną tkanką kostną, a następnie zastosowali narzędzia statystyczne, by wychwycić geny, które konsekwentnie były nasilone lub osłabione w nowotworze. Setki genów różniły się, a wiele z nich skupiało się w znanych szlakach nowotworowych napędzających wzrost, przeżycie i migrację komórek. Wśród nich jedno białko, SHP2, wyróżniało się jako węzeł silnie powiązany z kilkoma innymi: czynnikiem sygnałowym STAT3, enzymem modyfikującym DNA TET3 oraz regulatorem rozwoju HOXB2. Sugerowało to, że te molekuły mogą tworzyć powiązany łańcuch pomagający komórkom osteosarcomy zachowywać się agresywnie. 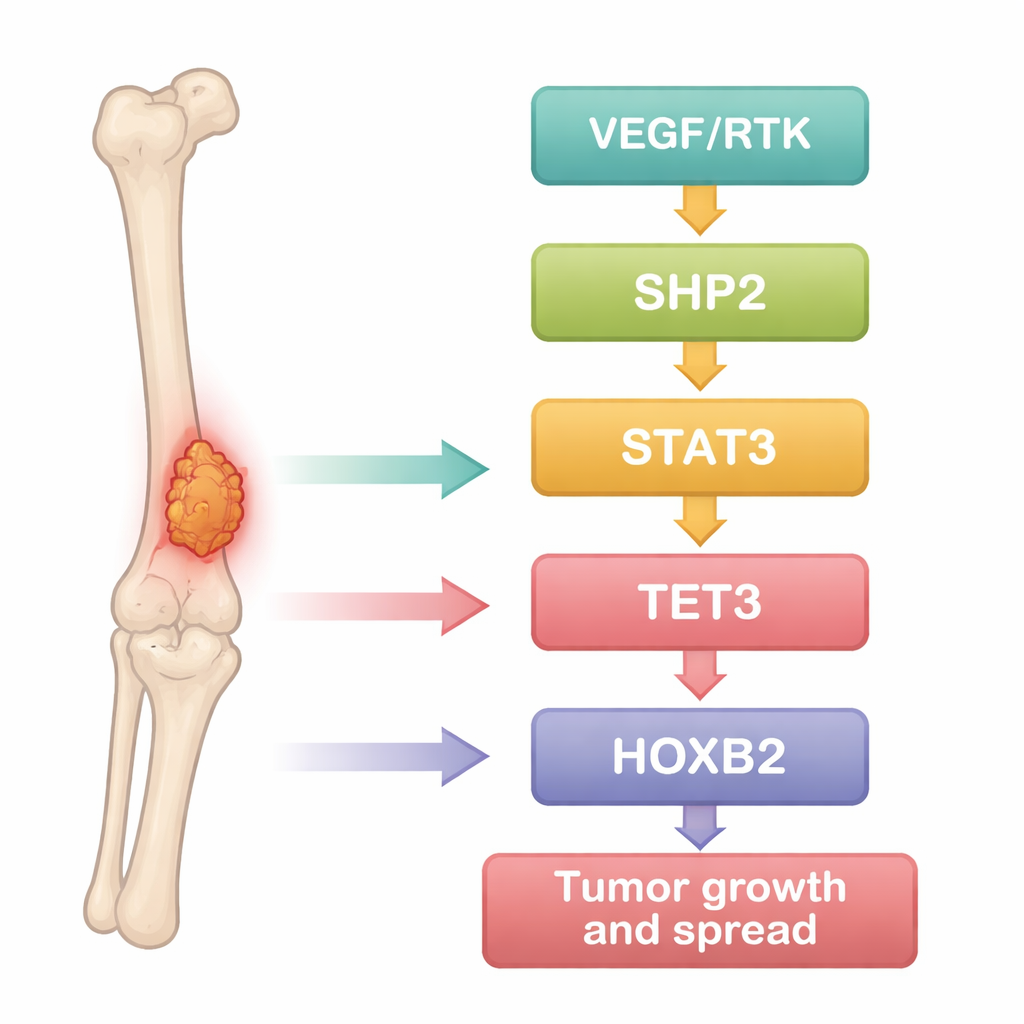
Testowanie roli SHP2 w komórkach nowotworowych
Aby wyjść poza korelacje, zespół zmodyfikował ludzkie linie komórkowe osteosarcomy (143B i MG63), tak by zmniejszać lub zwiększać poziom SHP2. Po obniżeniu SHP2 zdolność komórek do proliferacji, migracji po powierzchni i inwazji przez membranę wyraźnie spadła. Poziomy białek STAT3, TET3 i HOXB2 oraz markerów związanych z nowotworem, takich jak c-Myc, NANOG i NUSAP1, również się obniżyły. Ponowne aktywowanie STAT3 lub nadekspresja HOXB2 odwracały wiele z tych efektów, co wskazuje, że SHP2 działa powyżej łańcucha, który ostatecznie wpływa na geny kontrolujące podział komórek, cechy podobne do komórek macierzystych i aparat mitotyczny.
Budowanie krok po kroku ścieżki nowotworowej
Sklejając razem wyniki eksperymentów, autorzy przedstawiają model krok po kroku. W mikrośrodowisku guza wysokie poziomy naczyniowo‑śródbłonkowego czynnika wzrostu (VEGF) stymulują receptory tyrozynowe kinazy (RTK) na powierzchni komórki. Te z kolei aktywują SHP2 wewnątrz komórki. Aktywne SHP2 uruchamia STAT3, czynnik transkrypcyjny, który przemieszcza się do jądra i pomaga zwiększyć produkcję TET3. TET3 następnie edytuje chemiczne znaczniki na DNA, specyficznie usuwając grupy metylowe z regionu genu HOXB2. Ta demetylacja działa jak zdjęcie hamulca, pozwalając na silniejszą ekspresję HOXB2. HOXB2, gen zwykle uczestniczący w kierowaniu rozwojem, teraz zwiększa aktywność c‑Myc, NANOG i NUSAP1, które razem napędzają niepohamowany wzrost komórek guza, nasilają zachowania inwazyjne i wspierają cechy związane z przerzutami.
Od szalki Petriego do żywych zwierząt
Aby sprawdzić, czy ta ścieżka ma znaczenie w całych guzach, naukowcy wszczepili zmodyfikowane komórki osteosarcomy pod skórę myszy. Guzy powstałe z komórek nadprodukujących SHP2 rosły większe i cięższe niż guzy kontrolne. Gdy TET3 został wyciszony w tych komórkach bogatych w SHP2, wzrost guza spowolnił, a poziomy HOXB2 spadły, mimo że SHP2 i STAT3 pozostały aktywne. Ponowne wprowadzenie HOXB2 przywróciło witalność guza. Pomiary poziomów białek w tkance guza odzwierciedlały wcześniejsze wyniki z hodowli komórek, wzmacniając koncepcję, że SHP2, STAT3, TET3 i HOXB2 działają jako połączona oś napędzająca bardziej złośliwe zachowanie osteosarcomy. 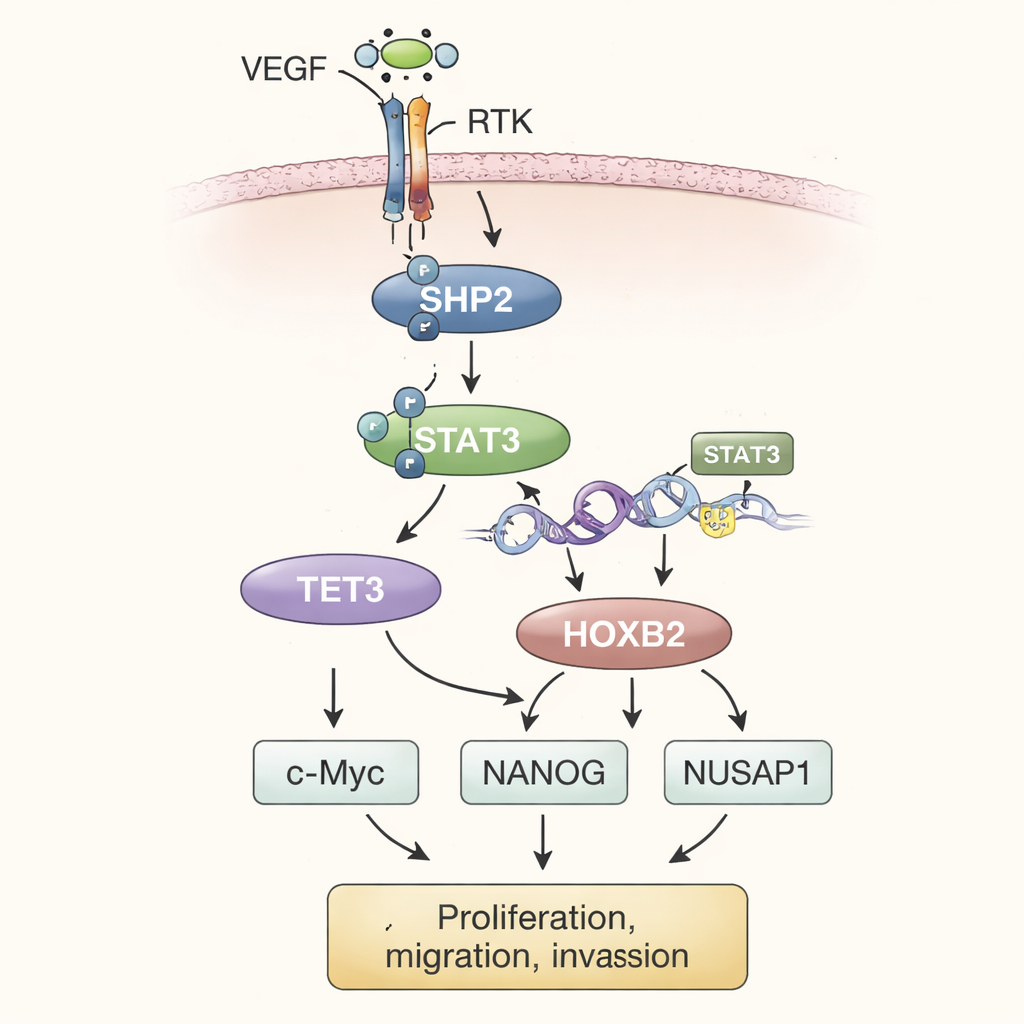
Co to oznacza dla przyszłych terapii
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że badacze zarysowali jasny łańcuch sygnałowy — od VEGF i jego receptorów powierzchniowych, przez SHP2 i STAT3, aż do TET3, HOXB2 i kilku silnych genów wzrostu — który pomaga wyjaśnić, dlaczego osteosarcoma może rosnąć szybko i wcześnie dawać przerzuty. Ponieważ SHP2 i STAT3 są enzymami, które w zasadzie można zablokować małocząsteczkowymi lekami, a TET3 i HOXB2 oznaczają późniejsze etapy tej samej drogi, ścieżka ta oferuje wiele punktów, w których przyszłe terapie mogłyby interweniować. Choć badanie przeprowadzono na liniach komórkowych i myszach, dostarcza szczegółowej mapy, z której producenci leków mogą korzystać, projektując terapie kombinowane mające na celu wyłączenie centralnych przełączników kontrolnych guza zamiast jedynie atakowania jego efektów końcowych.
Cytowanie: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Słowa kluczowe: osteosarcoma, SHP2, szlak STAT3, sygnalizacja nowotworowa, terapia celowana