Clear Sky Science · pl
Nieinwazyjne obrazowanie PET stresu oksydacyjnego wywołanego LPS w mięśniach szkieletowych przy użyciu radiotracera celującego w ROS
Dlaczego zestresowane mięśnie mają znaczenie
W miarę starzenia się, w przebiegu infekcji lub po długim unieruchomieniu w łóżku szpitalnym nasze mięśnie mogą się kurczyć i słabnąć. Duża część tego ukrytego uszkodzenia zaczyna się na długo przed widoczną utratą masy mięśniowej i jest napędzana przez niestabilne cząsteczki zwane reaktywnymi formami tlenu (ROS). W tym badaniu badacze opisują nowy sposób „widzenia” tego niewidocznego chemicznego stresu w mięśniach za pomocą badania PET, co potencjalnie pozwoli lekarzom wykrywać problemy wcześnie — zanim utrata mięśni stanie się trudna do odwrócenia. 
Bliższe spojrzenie na niewidoczny stres mięśniowy
Atrofia mięśni szkieletowych to stopniowa utrata masy i siły mięśniowej, która może wystąpić wraz ze starzeniem się, ciężką chorobą, brakiem aktywności lub w wyniku terapii, takich jak chemioterapia. Tradycyjnie lekarze korzystali z narzędzi takich jak biopsje, MRI czy CT, aby ocenić kondycję mięśni. Te metody pokazują zmiany wielkości i struktury, ale nie ujawniają wczesnych sygnałów chemicznych, które uruchamiają proces uszkodzenia. Jednym z najwcześniejszych i najważniejszych sygnałów jest stres oksydacyjny — nadmiar ROS, który zaburza równowagę chemiczną komórki i aktywuje szlaki prowadzące do rozkładu białek mięśniowych. Możliwość bezpośredniego pomiaru tego stresu w żywym mięśniu mogłaby pomóc zidentyfikować osoby zagrożone i monitorować efekty terapii chroniących mięśnie.
Tracer, który uwidacznia szkodliwe cząsteczki
Badacze skupili się na specjalistycznym tracerze do obrazowania PET o nazwie [18F]ROStrace, zaprojektowanym tak, aby lokalizować nadtlenek, jeden z głównych rodzajów ROS. Po potwierdzeniu, że tracer można wytwarzać w sposób powtarzalny i że pozostaje stabilny przez kilka godzin, przetestowali, czy rzeczywiście reaguje na stres oksydacyjny w komórkach mięśniowych hodowanych w laboratorium. Komórki mięśni myszy (myotuby C2C12) narażone na toksynę bakteryjną LPS, która wywołuje zapalenie i ROS, akumulowały więcej [18F]ROStrace w czasie niż komórki nieleczone. Gdy komórki chroniono lekiem antyoksydacyjnym, pobieranie tracera spadało; gdy ROS zwiększano innym związkiem, pobieranie wzrastało. Te wzorce wykazały, że sygnał tracera rósł i malał zgodnie z poziomem ROS, a nie z ogólnymi zmianami kształtu komórek czy metabolizmu. 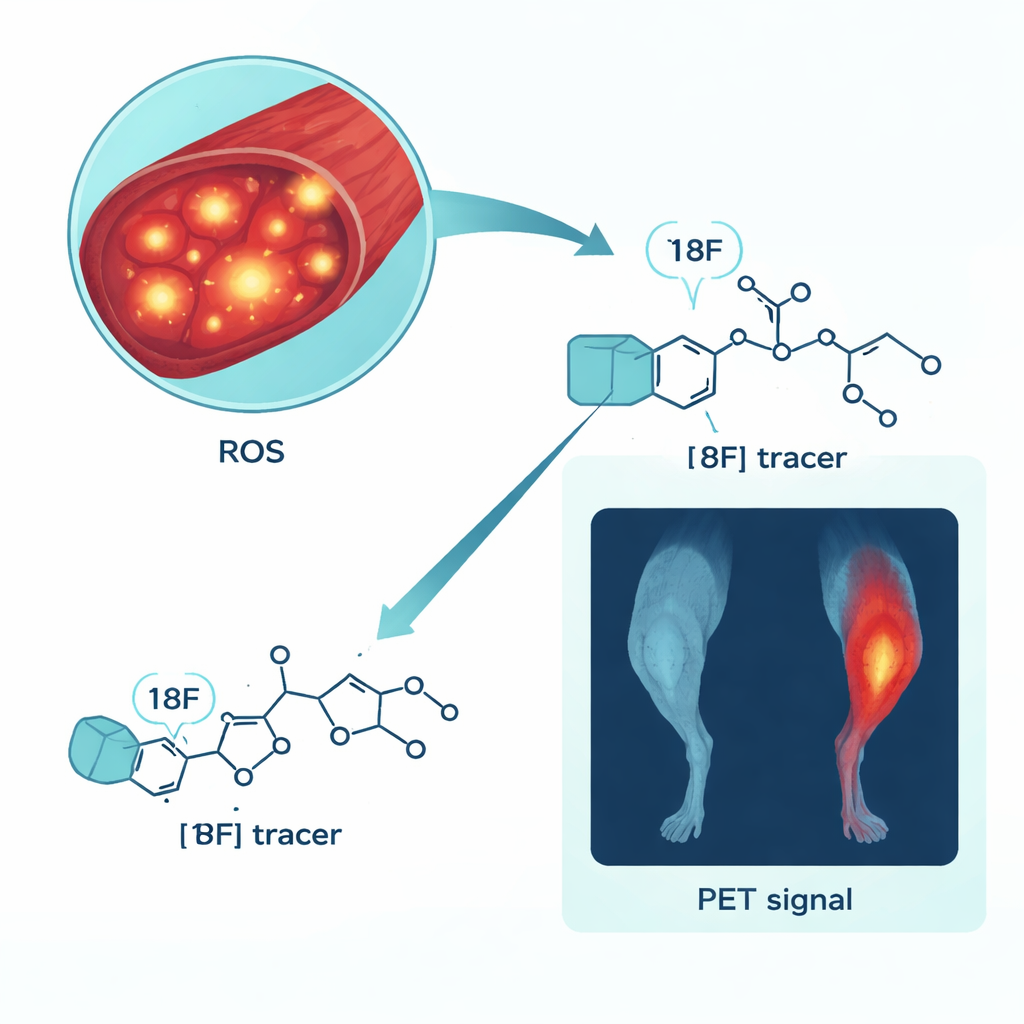
Od hodowli do żywych mięśni
Następnie zespół przeszedł do badań na myszach, aby sprawdzić, czy [18F]ROStrace potrafi ujawnić stres oksydacyjny w rzeczywistej tkance mięśniowej. Myszy otrzymały wstrzyknięcie LPS, aby wywołać ogólnoustrojowy stan zapalny powodujący wczesne oznaki wyniszczenia mięśni. Za pomocą PET/CT naukowcy zeskanowali zwierzęta około dobę później i zmierzyli pobieranie tracera w mięśniach kończyn tylnych. W porównaniu ze zdrowymi myszami kontrolnymi, grupa traktowana LPS miała w tych mięśniach w przybliżeniu dwukrotnie wyższy sygnał PET, co wskazuje na znacznie większe obciążenie oksydacyjne. Skanowanie w różnych punktach czasowych wykazało, że poziomy tracera w mięśniach osiągały stabilne plateau około godziny po podaniu, wyznaczając praktyczne okno obrazowania do przyszłych badań i możliwej translacji klinicznej.
Biologiczne wskazówki stojące za jasnym sygnałem
Aby potwierdzić, że obrazy PET rzeczywiście odzwierciedlają szkodliwą chemię, a nie przepływ krwi czy inne nieswoiste efekty, badacze przeanalizowali te same mięśnie za pomocą kilku standardowych metod laboratoryjnych. W mikroskopie mięśnie i hodowane myotuby poddane LPS wyglądały cieńsze, a poszczególne włókna miały mniejszy przekrój poprzeczny — cechy zgodne z wczesnymi etapami atrofii. Mitochondria, elektrownie komórkowe, wykazywały obniżone potencjały błonowe, co jest oznaką zaburzonej wewnętrznej równowagi pod wpływem stresu oksydacyjnego. Kluczowe geny napędzające rozkład mięśni, MuRF-1 i Atrogin-1, były wyraźnie podwyższone w komórkach i tkankach traktowanych LPS. Wreszcie barwienie barwnikiem fluorescencyjnym chemicznie powiązanym z [18F]ROStrace potwierdziło, że poziomy ROS były rzeczywiście wyższe w mięśniach wykazujących silniejsze sygnały PET, zarówno w hodowlach komórkowych, jak i u żywych myszy.
Co to może oznaczać dla pacjentów
Podsumowując, wyniki pokazują, że PET z [18F]ROStrace może nieinwazyjnie uwidocznić obszary stresu oksydacyjnego w mięśniach szkieletowych, a jasność sygnału koreluje z innymi cechami wczesnego uszkodzenia mięśni. Dla pacjentów może to w przyszłości oznaczać możliwość wykrywania stresu mięśniowego zanim wystąpi znaczące wyniszczenie, monitorowania, czy nowe leki lub programy ćwiczeń łagodzą szkodliwą chemię, oraz lepszego zrozumienia stanów od osłabienia związanego z sepsą po starcze kruchości. Choć potrzeba dalszych badań długoterminowych i badań u ludzi, to narzędzie obrazowania ukierunkowane na ROS otwiera nowe okno na to, jak i kiedy mięśnie zaczynają zawodzić — i jak możemy interweniować wcześniej.
Cytowanie: Park, J.Y., Park, S.M., Lee, T.S. et al. Noninvasive PET imaging of LPS-induced oxidative stress in skeletal muscle using a ROS-targeting radiotracer. Sci Rep 16, 4917 (2026). https://doi.org/10.1038/s41598-026-35489-3
Słowa kluczowe: atrofia mięśni, stres oksydacyjny, obrazowanie PET, reaktywne formy tlenu, [18F]ROStrace