Clear Sky Science · pl
Globalna analiza ekspresji RNA w próbkach pacjentek wskazała potencjalne biomarkery diagnostyczne specyficzne dla endometriozy otrzewnowej, jajnikowej i głębokiej
Dlaczego ta choroba ma znaczenie w codziennym życiu
Endometrioza dotyka szacunkowo 190 milionów kobiet na całym świecie, często powodując silny ból miednicy, zmęczenie oraz problemy z płodnością. Mimo to wiele osób czeka niemal dekadę na jednoznaczną diagnozę, zazwyczaj potwierdzaną dopiero podczas zabiegu chirurgicznego. W tym badaniu postawiono proste, ale istotne pytanie: czy zamiast tego można odczytać molekularne „odciski palców” organizmu, aby wykryć endometriozę wcześniej, a nawet rozróżnić jej różne postaci przy pomocy prostego testu w przyszłości?
Różne oblicza tej samej choroby
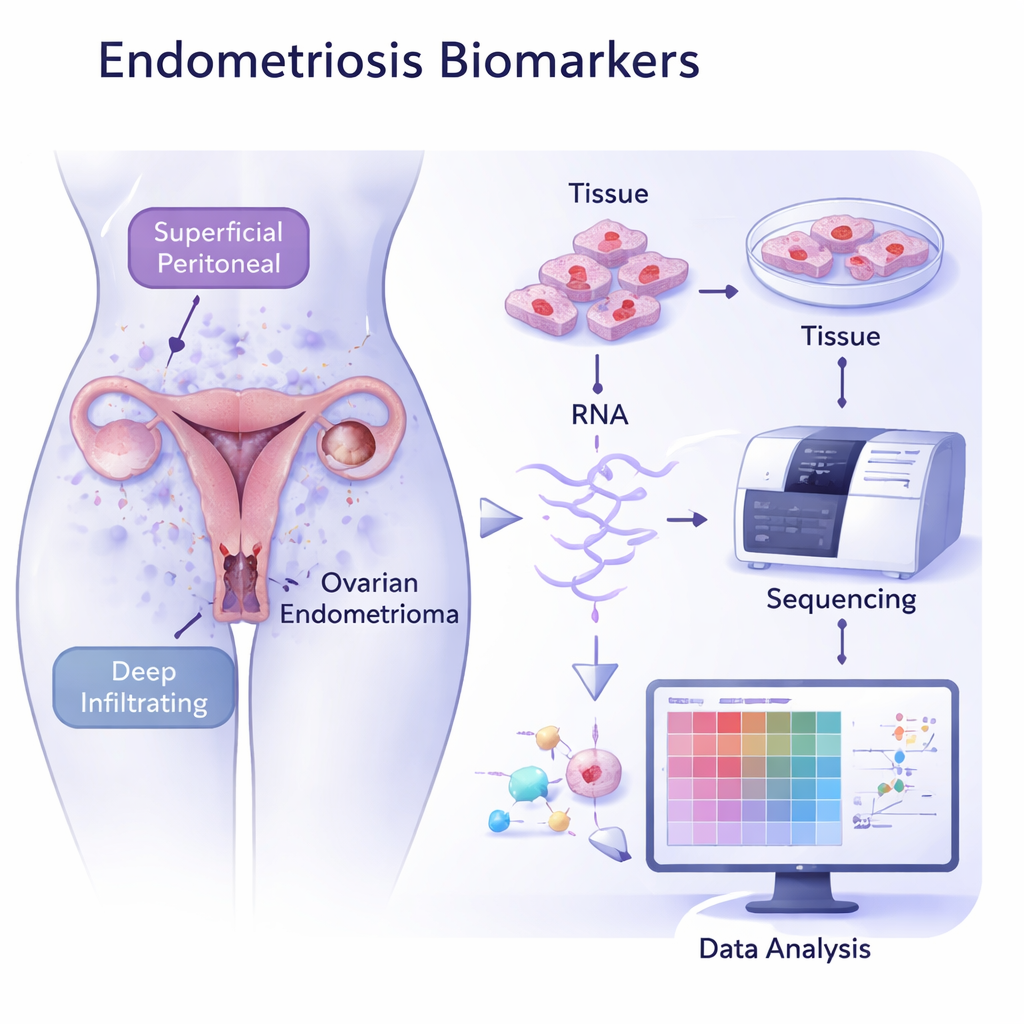
Endometrioza występuje, gdy tkanka podobna do błony śluzowej macicy rozwija się tam, gdzie jej nie powinno być — na przykład na jajniku, cienkiej wyściółce jamy brzusznej (otrzewnej) lub głęboko w narządach miednicy. Te lokalizacje określają trzy główne podtypy: jajnikowy, otrzewnowy i głęboki. Każdy z nich może powodować odmienne wzorce bólu, problemy z płodnością i uszkodzenia narządów. Obecnie lekarze opierają się na objawach, badaniach obrazowych i często laparoskopii — zabiegu w znieczuleniu — aby potwierdzić rozpoznanie i ustalić podtyp. Nieinwazyjna metoda rozróżniania tych form oszczędziłaby wielu kobietom lat niepewności i operacji.
Odczytywanie „kodu kreskowego” RNA w zmienionej chorobowo tkance
Naukowcy zebrali próbki tkanek od 26 kobiet z endometriozą — obejmujących wszystkie trzy podtypy — oraz od 15 kobiet bez choroby. Następnie zastosowali sekwencjonowanie RNA, metodę mierzącą, które geny są włączone lub wyłączone, aby zbudować globalny obraz aktywności w tych tkankach. Porównując tkanki chorobowe z zdrową wyściółką macicy, próbki ułożyły się w wyraźne klastry, ukazując odrębne wzorce aktywności genów. Zmiany na jajnikach utworzyły zwartą grupę, podczas gdy zmiany otrzewnowe i głębokie grupowały się razem, co wspiera ideę, że te podtypy podążają różnymi szlakami biologicznymi, mimo wspólnych cech.
Wspólne szlaki bliznowacenia i stanu zapalnego
We wszystkich trzech podtypach zespół wykrył zwiększoną aktywność genów związanych z budową i przebudową rusztowania tkankowego (macierz pozakomórkowa), wzrost skurczliwości komórek typowy dla bliznowacenia i silne sygnalizowanie zapalne. Zmiany te odpowiadają obserwacjom klinicznym: sztywne, włókniste zmiany powodujące ból i zrosty. Badanie wykazało także zmieniony krajobraz immunologiczny w obrębie zmian. Tak zwane makrofagi M2, typ komórek odpornościowych związany z gojeniem ran i fibrozą, były szczególnie liczne, podczas gdy komórki NK (natural killers) — ważne w usuwaniu nieprawidłowych komórek — były wyraźnie zmniejszone. Ta nierównowaga może pomagać tkance endometrialnej przetrwać i się rozprzestrzeniać, mimo że znajduje się w niewłaściwym miejscu.
Cząsteczkowe wskazówki specyficzne dla podtypów
Ponad te wspólne wzorce każdy podtyp miał własny sygnaturowy profil molekularny. W endometriozie głębokiej i otrzewnowej silnie wzrosła aktywność genów zaangażowanych w sygnalizację fosfodiesteraz — szlaki już powiązane z innymi chorobami włóknieniowymi. W endometriozie jajnikowej wyróżniały się geny związane z prezentacją antygenów i produkcją hormonów, co sugeruje, że jajnik tworzy odrębne środowisko biochemiczne. Badacze przeanalizowali także RNA niekodujące — cząsteczki, które nie tworzą białek, ale mogą regulować aktywność genów. Zidentyfikowali kilka takich RNA, które były znacznie zwiększone ogólnie lub specyficznie w niektórych podtypach, co wskazuje na nowe regulatorowe elementy i możliwe biomarkery wykrywalne we krwi lub innych płynach ustrojowych.
Obiecujące markery białkowe dla przyszłych testów
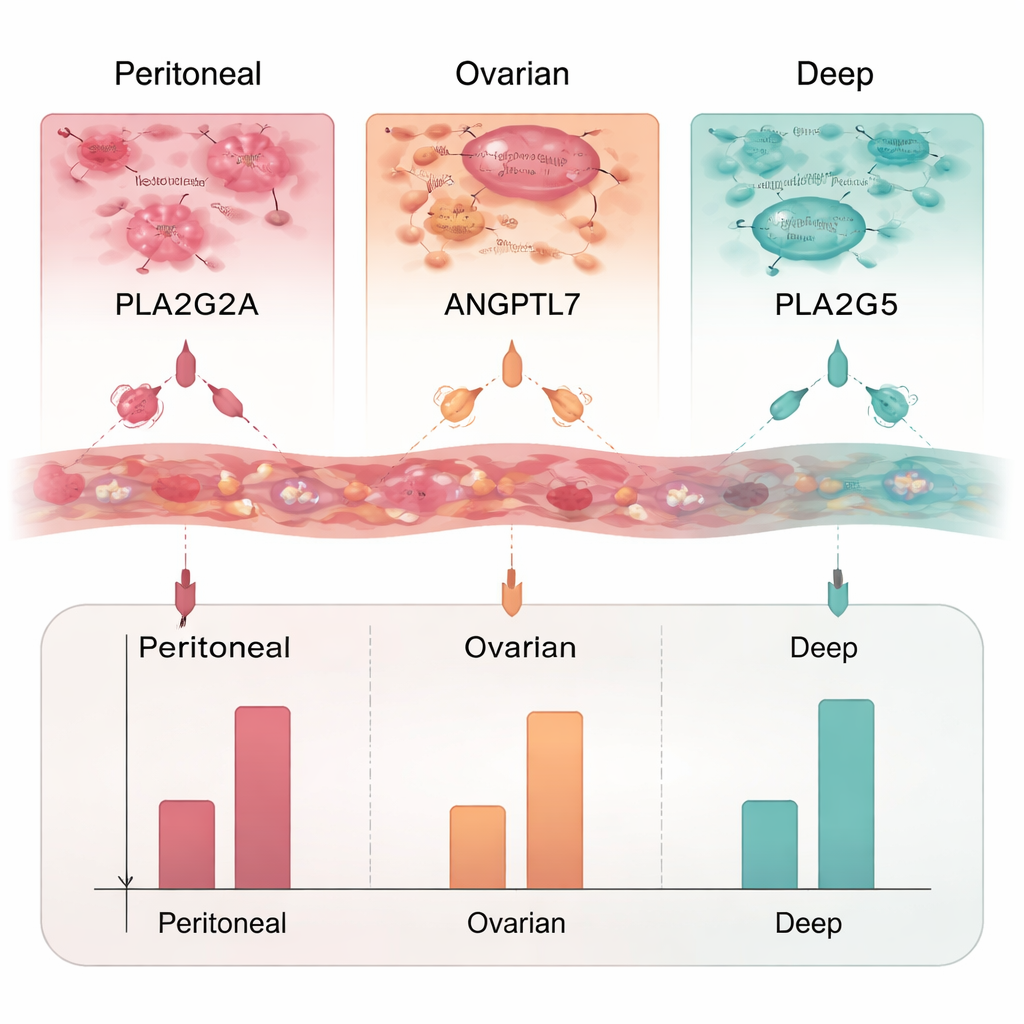
Z długiej listy zmienionych genów zespół skupił się na tych kodujących białka wydzielane — idealne kandydatury do przyszłego testu krwi. Wybrali trzy białka do bliższych badań: PLA2G2A, ANGPTL7 i PLA2G5. Przy użyciu ELISA, laboratoryjnej metody mierzenia poziomów białek, stwierdzili, że PLA2G2A była podwyższona we wszystkich trzech typach endometriozy, szczególnie w zmianach jajnikowych. ANGPTL7 była zwiększona głównie w zmianach głębokich i otrzewnowych, natomiast PLA2G5 podwyższono jedynie w endometriozie głębokiej. Razem te białka tworzą potencjalny panel, który mógłby nie tylko wskazywać na obecność endometriozy, ale także sugerować lokalizację zmian.
Co to oznacza dla pacjentek
To badanie nie dostarcza jeszcze gotowego testu krwi, ale kładzie ważne fundamenty. Mapując zachowanie tysięcy genów i komórek odpornościowych w różnych podtypach endometriozy, praca identyfikuje konkretne białka — PLA2G2A, ANGPTL7 i PLA2G5 — które mogłyby być w przyszłości mierzone nieinwazyjnie. Jeśli zostaną zweryfikowane w większych, niezależnych grupach pacjentek, kombinacje takich markerów mogłyby skrócić długą drogę do rozpoznania, zmniejszyć potrzebę operacji jedynie w celu potwierdzenia choroby i umożliwić bardziej dopasowane leczenie w zależności od dokładnego podtypu, z którym ma do czynienia kobieta.
Cytowanie: Lisá, Z., Fanta, M., Kokavec, J. et al. Global RNA expression analysis of patient samples identified potential diagnostic biomarkers specific for peritoneal, ovarian and deep endometriosis. Sci Rep 16, 5070 (2026). https://doi.org/10.1038/s41598-026-35467-9
Słowa kluczowe: endometrioza, biomarkery, sekwencjonowanie RNA, komórki odpornościowe, zdrowie kobiet