Clear Sky Science · pl
Opracowanie globalnego systemu przesiewowego do wykrywania interakcji białko–białko za pomocą uzupełniania luminescencji w drożdżach rozdzielających
Rozświetlając ukryte życie białek
Każde uderzenie serca, myśl i oddech w naszych ciałach zależy od współdziałania białek wewnątrz komórek. Te drobne partnerstwa, zwane interakcjami białko–białko, kontrolują wszystko, od sposobu odczytu genów po reakcje komórek na stres. Wiele z tych powiązań jest jednak krótkotrwałych lub delikatnych, co utrudnia ich wykrycie dostępnymi narzędziami. W pracy opisano nowy, wysoce czuły system „oparty na świetle” zbudowany w prostym organizmie modelowym — drożdżu rozdzielającym — który pozwala jednocześnie ujawnić tysiące ukrytych połączeń między białkami.
Dlaczego partnerstwa białek są tak trudne do zaobserwowania
Białka rzadko działają solo. Wiążą się z różnymi partnerami w różnych momentach, czasem zaledwie na chwilę, a ich zachowanie może zmieniać się pod wpływem modyfikacji chemicznych lub miejsca w komórce. Tradycyjne metody badania tych interakcji albo wyjmują białka z ich naturalnego środowiska, albo polegają na sztucznych sztuczkach genetycznych, które nie wychwytują wszystkich parowań. W rezultacie istniejące mapy interakcji w komórce są niekompletne. Autorzy postanowili ulepszyć ten obraz, tworząc bardziej elastyczny i czuły system, który mógłby przebadać niemal każde białko w drożdżach rozdzielających w żywych komórkach.
Zmiana dotyku w światło
Rdzeniem nowego podejścia jest rozdzielony enzym emitujący światło. Jedna część, nazwana LgBiT, jest przyczepiona do „przynęty” — białka, które badacze chcą analizować. Druga część, SmBiT, jest przyłączona do wielu potencjalnych „zdobywców”, po jednym w każdym szczepie drożdży. Same w sobie te dwie części enzymu niemal się nie łączą. Ale gdy białko-przynęta i białko-zdobywca wiążą się wewnątrz komórki, części te łączą się ponownie, odtwarzając aktywny enzym, który świeci w obecności chemicznego substratu. Mierząc natężenie światła wytwarzanego przez każdy szczep drożdży, zespół może określić, które białka faktycznie spotykają się w komórce i jak silna jest ich interakcja. Aby nie przegapić partnerów z powodu blokowania funkcji przez znacznik, białko-przynęta jest tworzone w dwóch wersjach, z LgBiT przyłączonym do jednego lub drugiego końca, co znacznie zwiększa szanse, że przynajmniej jedna orientacja zadziała. 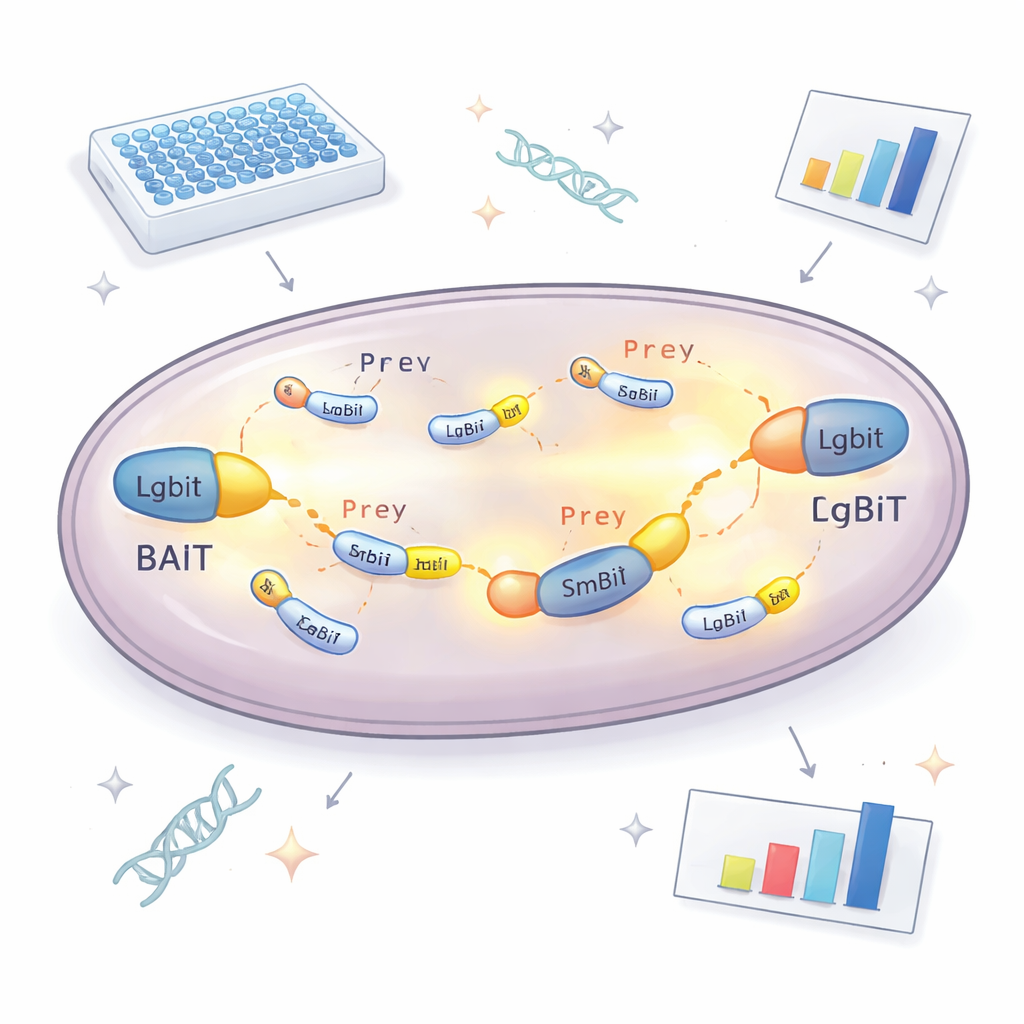
Projektowanie biblioteki i systemu szczepów drożdżowych
Budowa tej platformy wymagała czegoś więcej niż sprytnego enzymu. Badacze musieli również wprowadzić tysiące białek-zdobywców do drożdży w kontrolowany, jednorazowy sposób. Zaprojektowali specjalny wektor DNA dla białek-zdobywców, który wstawia się w określone miejsce genomu drożdżowego i przenosi czerwony znacznik fluorescencyjny. Jasność tego czerwonego sygnału odzwierciedla liczbę wstawionych kopii, co pozwala zespołowi łatwo wybrać kolonie z dokładnie jedną kopią — kluczowe dla wiarygodnych porównań. Stworzono także dedykowane wektory przynęty, które umieszczają LgBiT na początku lub końcu białka-przynęty, oddzielone elastycznymi łącznikami, aby białko mogło prawidłowo się składać i poruszać. Ostrożnie zaprojektowane szczepy drożdży zostały następnie zbudowane tak, by mogły jednocześnie gościć dwa konstrukty przynęty i jeden konstruktn białka-zdobywcy, wykorzystując markery odżywcze, aby zapewnić przeżycie tylko poprawnie złożonych komórek.
Sprawdzanie systemu w praktyce
Aby sprawdzić, czy ich projekt rzeczywiście poprawia wykrywalność, naukowcy najpierw przeanalizowali białka z dobrze znanymi partnerami. Potwierdzili, że siła sygnału silnie zależała od tego, gdzie przyczepiono świetlny znacznik: niektóre interakcje ujawniały się tylko wtedy, gdy LgBiT znajdował się na jednym końcu przynęty, a nie na drugim. Ekspresja obu wersji jednocześnie zwiększała emisję światła, dowodząc, że strategia z dwiema przynętami ułatwia wychwycenie słabych lub zależnych od orientacji interakcji. System wykrywał także kontakty z udziałem białek błonowych — klasy, która jest notorycznie trudna dla tradycyjnych metod typu yeast two-hybrid. Po tej walidacji zespół rozszerzył badanie do skali genomowej, używając jako przynęty białka związanego z transkrypcją, nazwanego Tfs1. Przesiewając ponad 4 600 białek-zdobywców, znaleźli 31 silnych kandydatów, w tym kilka już znanych partnerstw i wiele nowych, niektóre znajdujące się poza jądrem, w obszarach takich jak mitochondria czy powierzchnia komórki. 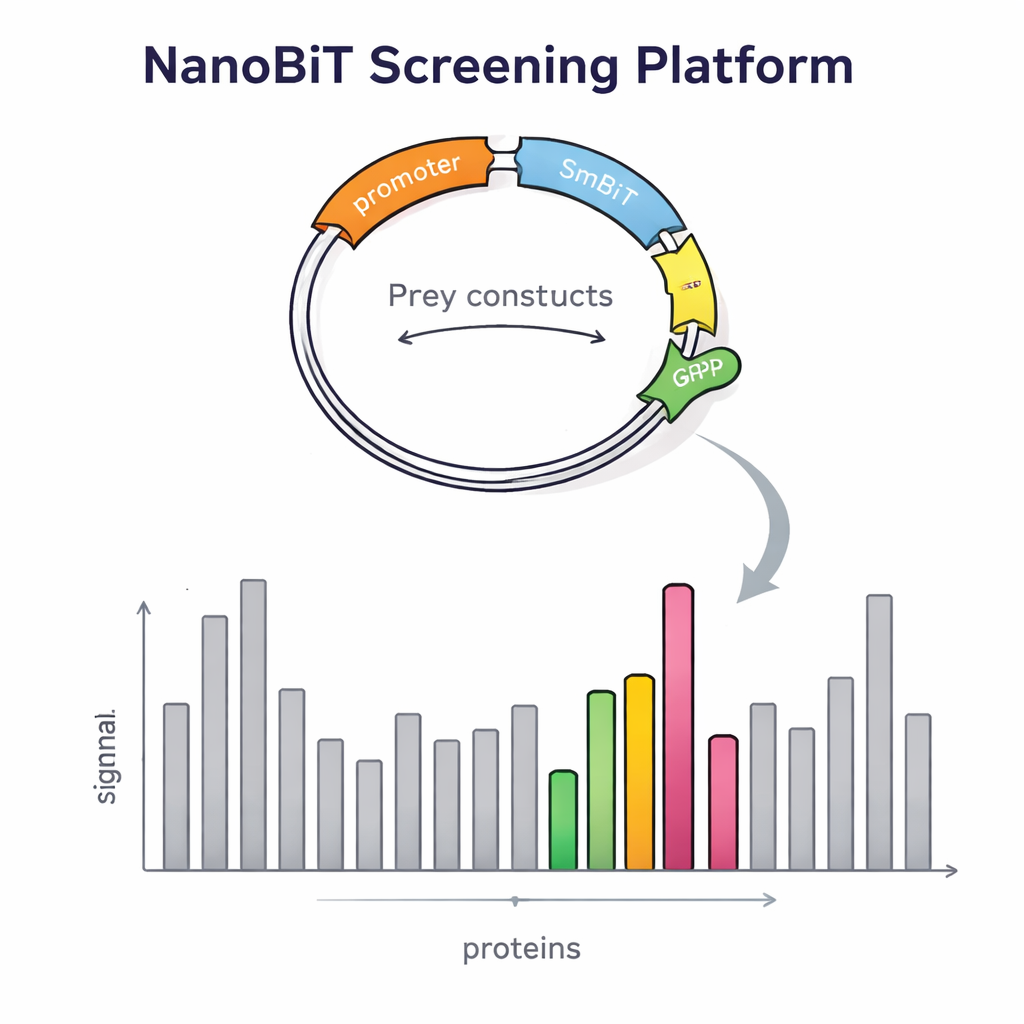
Co to oznacza dla biologii i odkrywania leków
Dla osoby niezajmującej się specjalistycznie kluczowy wniosek jest taki, że autorzy zbudowali bardziej czuły „radar interakcji” wewnątrz komórek drożdżowych. Przekształcając krótkie uściski dłoni białek w mierzalne błyski światła i sprytnie organizując genetykę tak, by trzy znakowane białka mogły być wyrażone razem, ich system ujawnia zarówno znane, jak i dotąd niewidoczne partnerstwa białkowe. Chociaż dalsze weryfikacje innymi technikami będą nadal konieczne, aby potwierdzić każde nowe parowanie, ta platforma wypełnia ważne luki w naszych mapach sieci komórkowych. Ponieważ szczepy zostały również zaprojektowane tak, by były bardziej wrażliwe na małe cząsteczki, ten sam układ można dostosować do poszukiwania leków, które albo rozrywają szkodliwe partnerstwa białkowe, albo stabilizują korzystne, oferując potężne nowe narzędzie zarówno dla biologii podstawowej, jak i wczesnych etapów odkrywania leków.
Cytowanie: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Słowa kluczowe: interakcje białek, drożdże rozdzielające, test luminescencyjny, przesiewy wysokoprzepustowe, narzędzia odkrywania leków