Clear Sky Science · pl
Sekretom zależny od cząsteczki rozpoznającej sygnał u człowieka
Jak komórki decydują, które białka opuszczają komórkę
Nasze komórki nieustannie wysyłają białka, które tworzą hormony, przeciwciała i struktury międzytkankowe. Nie każde jednak powinno podążać w świat. To badanie stawia podstawowe, wciąż nierozwiązane pytanie: jak komórki ludzkie decydują, które białka polegają na kluczowym pomocniku zwanym cząsteczką rozpoznającą sygnał (SRP), aby trafić do wewnętrznego centrum wysyłkowego komórki, a które potrafią to zrobić bez niej? Mapując tę decyzję równocześnie dla tysięcy białek, autorzy ujawniają, kto zależy od SRP, kto nie, i co się dzieje, gdy ten system zawodzi — temat istotny dla wielu chorób związanych z nieprawidłowym kierowaniem lub brakiem białek wydzielanych.
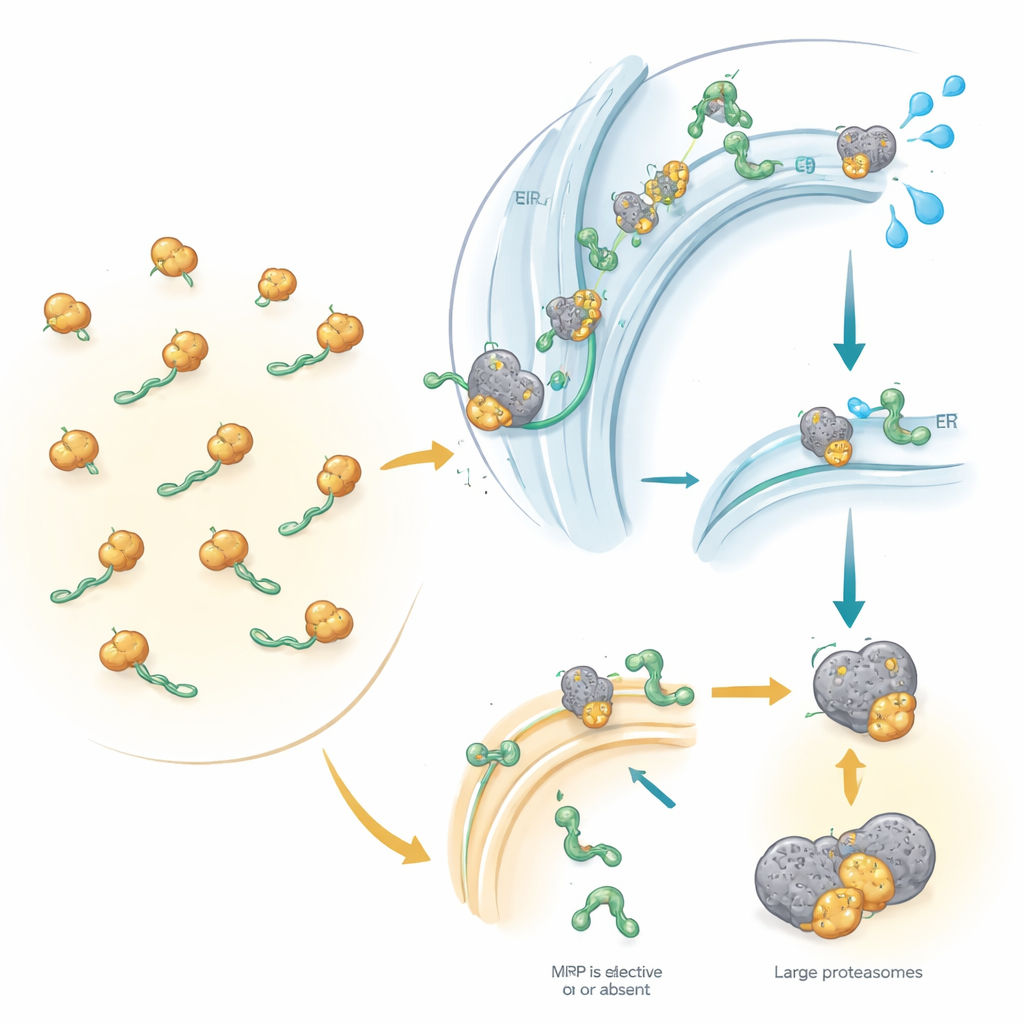
Dock wysyłkowy komórki i jego główny przewodnik
Około jedna na trzy ludzkie białka przeznaczona jest na powierzchnię komórki, do błon komórkowych lub do wydzielania na zewnątrz. Aby trafić we właściwe miejsce, większość z nich musi najpierw wejść do sieci wewnętrznych błon zwanej retikulum endoplazmatycznym — wysyłkowego doku komórki. SRP działa jak przewodnik: rozpoznaje małą „etykietę adresową” na początku nowo syntetyzowanych białek i tymczasowo wstrzymuje ich produkcję. To zatrzymanie daje rybosomowi — maszynie wytwarzającej białka — czas na zadokowanie przy retikulum endoplazmatycznym, gdzie synteza jest wznawiana, a rosnące białko wciągane do lub przez błonę. Niektóre białka jednak znane są z używania alternatywnych dróg, które nie wymagają SRP, zwłaszcza bardzo małe białka lub te zakotwiczone za pomocą końca ogonowego. Dotąd naukowcy nie wiedzieli, w skali globalnej, które białka ludzkie rzeczywiście potrzebują SRP, a które potrafią je ominąć.
Wyłączanie SRP, żeby zobaczyć, co się psuje
Aby to sprawdzić, badacze selektywnie zmniejszyli poziom jednego niezbędnego składnika SRP, SRP54, w ludzkich komórkach HeLa. Następnie zastosowali wrażliwą technikę zwaną spektrometrią mas, aby zmierzyć ponad 6000 białek wewnątrz komórek i prawie 2000 białek obecnych w otaczającym płynie, zwanym medium warunkowym. Porównanie komórek z normalnym SRP54 i z jego redukcją pozwoliło zobaczyć, które białka stały się mniej obfite, które wzrosły, a które pozostały niezmienione. Wyraźny spadek poziomu białka — zwłaszcza zarówno we wnętrzu komórki, jak i w medium — uznano za oznakę, że dane białko zależy od SRP, by być poprawnie zsyntetyzowane i skierowane.
Kto zależy od SRP, a kto radzi sobie bez niego
Analiza wykazała, że większość białek normalnie wydzielanych do medium wyraźnie polega na SRP. Gdy SRP54 został zmniejszony, większość tych białek wydzielanych, szczególnie tych niosących klasyczną sygnałową „etykietę adresową”, gwałtownie spadła. Wiele białek błonowych wewnątrz komórki również się zmniejszyło, ujawniając je jako klientów SRP. Mniejszy zestaw białek z podobnymi etykietami adresowymi pozostał w dużej mierze niezmieniony, oznaczając je jako niezależne od SRP; prawdopodobnie korzystają z alternatywnych dróg trafiania do retikulum endoplazmatycznego. Badacze odkryli też, że specyficzne cechy etykiety — na przykład dodatnio naładowany region na jej początku — były częstsze wśród białek zależnych od SRP, co sugeruje subtelne reguły pomagające SRP wybierać ładunek. Jednocześnie niektóre białka zaangażowane w znakowanie uszkodzonych białek do degradacji oraz funkcje mitochondrialne wzrosły, co sugeruje, że komórki uruchamiają systemy awaryjne i zwiększają produkcję energii, gdy główny przewodnik wysyłki zawodzi.
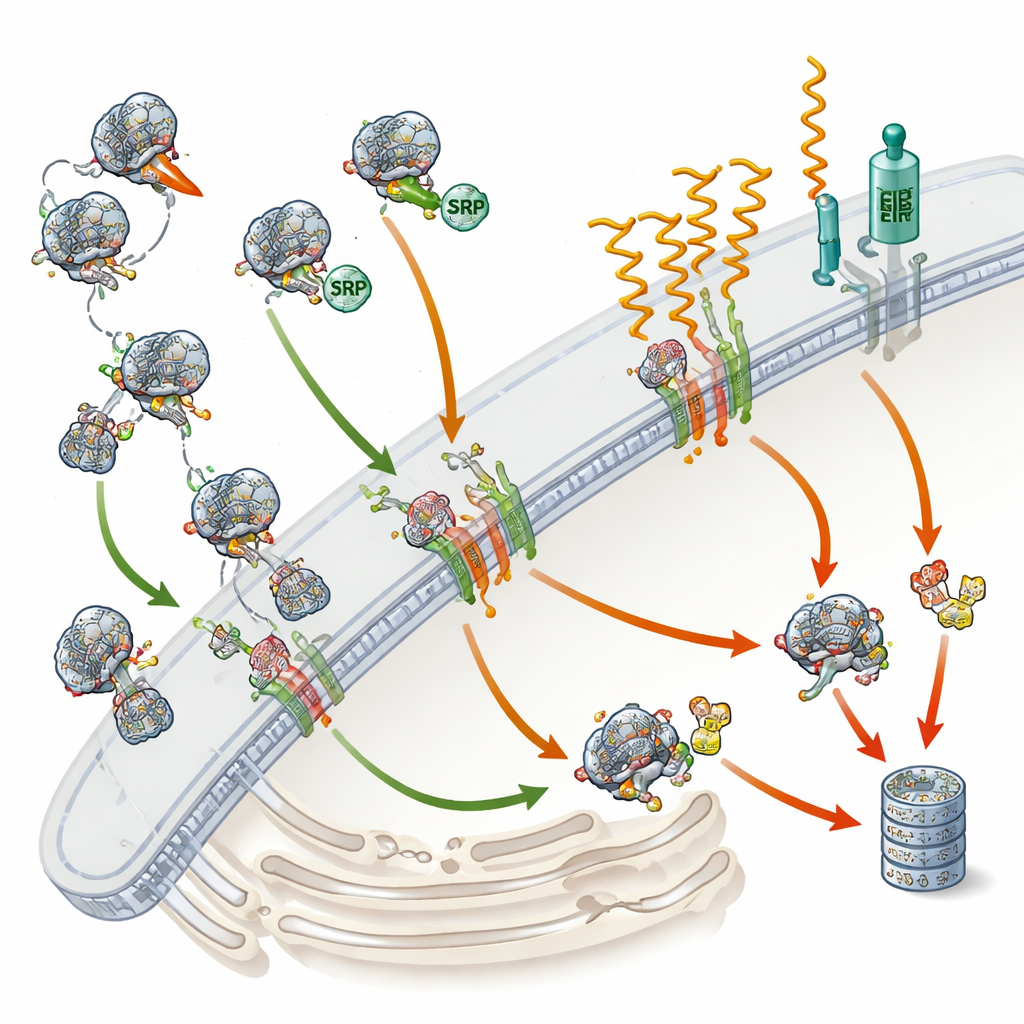
Kontrola jakości, gdy kierowanie zawodzi
Badanie poszło dalej niż samo liczenie białek: porównano zmiany z przesunięciami w mRNA, planach używanych do syntezy białek. Wiele białek zależnych od SRP straciło nie tylko samą cząsteczkę, ale i ich RNA — wskazując na udział ścieżki kontroli jakości znanej jako RAPP. Gdy SRP nie może prawidłowo zaangażować powstającego białka sekretornego lub błonowego, ta ścieżka zdaje się uruchamiać rozkład odpowiadającego mRNA, zapobiegając dalszej produkcji źle skierowanego białka. Równocześnie niepełnowartościowe białka, które nie osiągają retikulum endoplazmatycznego, prawdopodobnie otrzymują małe molekularne „flagi” i trafiają do komórkowych „niszczarek” zwanych proteasomami. Co ciekawe, klasyczne szlaki stresowe retikulum endoplazmatycznego nie były silnie aktywowane, co sugeruje, że defekt SRP wywołuje odmienny typ odpowiedzi stresowej komórki.
Co to znaczy dla zdrowia i chorób
Mapując po raz pierwszy w komórkach ludzkich, które białka wydzielane i błonowe są zależne od SRP, a które niezależne, praca ta dostarcza wzorcowej mapy zasad wysyłki komórkowej. Wyniki pokazują, że większość eksportowanych białek rzeczywiście polega na SRP i że, gdy SRP zawodzą, komórki reagują przez degradację zarówno białek, jak i ich planów RNA, jednocześnie uruchamiając alternatywne mechanizmy radzenia sobie. Ponieważ wiele mutacji powodujących choroby dotyczy sygnałowych „etykiet adresowych” białek wydzielanych, zrozumienie, jak SRP rozpoznaje swoje ładunki i jak RAPP usuwa wadliwe produkty, może pomóc wyjaśnić, dlaczego określone mutacje prowadzą do niedoborów hormonalnych, zaburzeń odporności czy neurodegeneracji — i w końcu wskazać nowe sposoby dostrajania kierowania białek w kontekście zdrowia człowieka.
Cytowanie: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
Słowa kluczowe: wydzielanie białek, cząsteczka rozpoznająca sygnał, sekretom, kontrola jakości białek