Clear Sky Science · pl
Sekwencyjna inhibicja platyną i PARP zwiększa skuteczność immunoterapii PD1 w mysiej rakowej gruczołu trzustkowego z mutacją Brca2
Dlaczego to badanie ma znaczenie dla pacjentów
Rak trzustki jest jednym z najgroźniejszych nowotworów, a nawet jeśli lekarze wiedzą, że guz ma podatność — na przykład mutację w genie BRCA2 — obecne terapie rzadko utrzymują chorobę pod kontrolą przez długi czas. To badanie wykorzystuje realistyczny model myszy, aby odpowiedzieć na praktyczne pytanie, z którym mierzy się wielu pacjentów i onkologów: czy po silnej chemioterapii i inhibitorze PARP dodanie nowoczesnej immunoterapii może znacząco wydłużyć przeżycie i dlaczego guzy tak często nawracają?
Uparty rak z genetyczną słabością
Gruczołowy rak przewodowy trzustki jest wyjątkowo trudny do leczenia — pięcioletnie przeżycie nadal wynosi kilka procent. Niewielka część pacjentów ma odziedziczone lub nowotworowe defekty w BRCA2, genie niezbędnym do naprawy uszkodzonego DNA. Takie guzy są wyjątkowo wrażliwe na leki uszkadzające DNA, jak chemioterapia na bazie platyny, oraz na inhibitory PARP, które dodatkowo upośledzają zdolność komórek nowotworowych do naprawy DNA. Standardowe postępowanie w zaawansowanym raku trzustki z mutacją BRCA to miesiące chemioterapii platynowej, a następnie leczenie podtrzymujące inhibitorem PARP. Jednak w kluczowym badaniu POLO ta strategia nie przedłużyła całkowitego przeżycia, co podkreśla konieczność zrozumienia mechanizmów oporności i opracowania lepszych podejść podtrzymujących.
Budowanie bardziej realistycznego modelu mysiego
Wiele istniejących modeli laboratoryjnych pozbawia nowotwór elementów odpornościowych i zrębu, które otaczają guzy u pacjentów. Aby temu sprostać, autorzy zaprojektowali myszy rozwijające guzy trzustki z niedoborem BRCA2 w kontekście w pełni funkcjonującego układu odpornościowego. Z tych spontanicznych guzów otrzymano klonalne linie komórkowe, które można było wszczepić do genetycznie dopasowanych myszy. Guzy z mutacją Brca2 przypominały ludzkie nowotwory trzustki: były silnie włókniste, w dużej mierze wykluczały limfocyty T i wykazywały wysokie poziomy spontanicznego uszkodzenia DNA. Co istotne, guzy były bardzo wrażliwe na powszechnie stosowaną kombinację platynową (gemcytabina plus cisplatyna), podczas gdy sam inhibitor PARP dawał jedynie skromne i krótkotrwałe efekty u zwierząt, mimo silnej aktywności wobec tych samych komórek w hodowli. 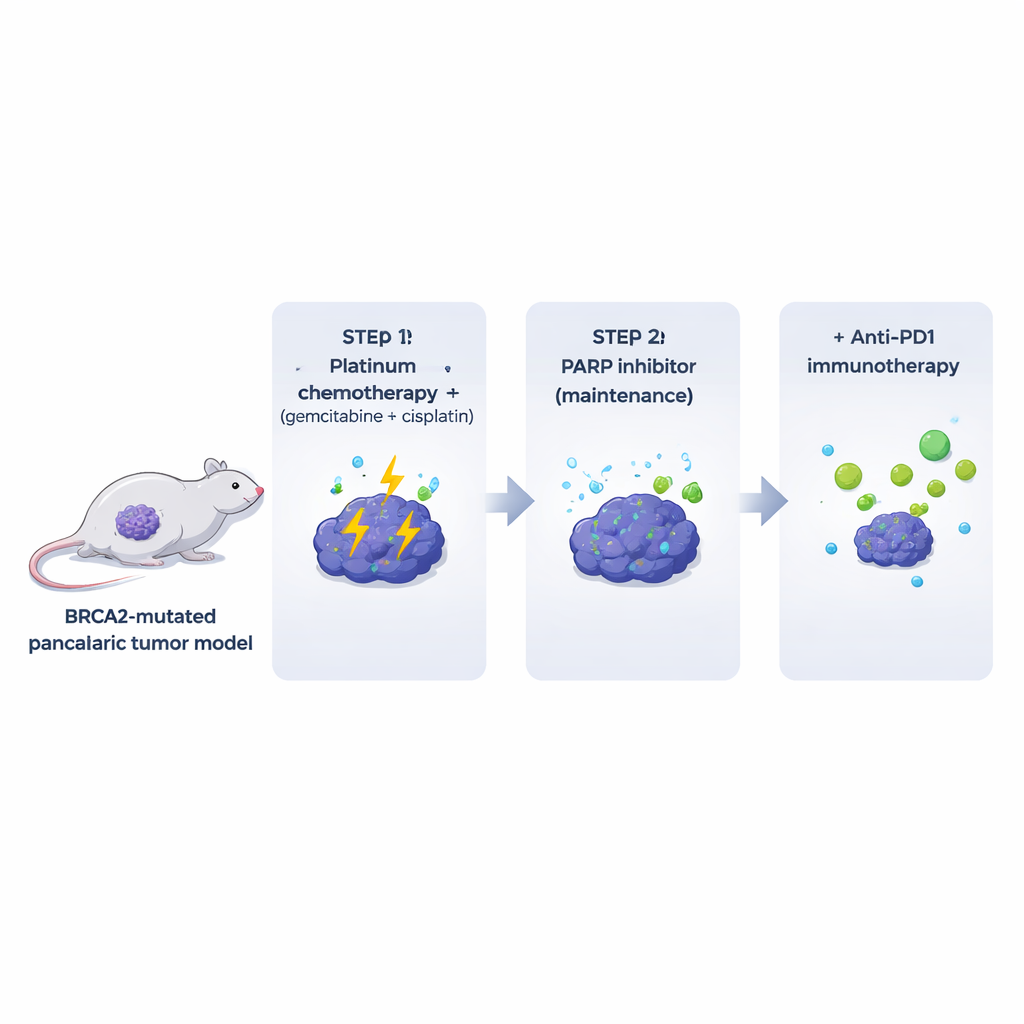
Chemioterapia przekształca mikrośrodowisko guza
Zespół zapytał następnie, co dzieje się wewnątrz guza po chemioterapii platynowej. Dziesięć dni po leczeniu guzy zmniejszyły się, ale nie zostały całkowicie zniszczone. Analizy ekspresji genów ujawniły wyraźne przesunięcie w kierunku aktywności związanej z odpornością: włączone zostały szlaki powiązane z aktywacją limfocytów T i odpornością adaptacyjną. W leczonych guzach znaleziono więcej limfocytów T, z których wiele nosiło markery wyczerpania — oznaki, że zostały aktywowane, ale stają się mniej efektywne. Podobne wzorce zwiększonej obecności komórek T obserwowano u ludzkich nowotworów trzustki z mutacjami BRCA lub pokrewnym PALB2 po tym, jak pacjenci otrzymali chemioterapię platynową przed operacją. Równocześnie komórki nowotworowe zwiększały poziomy PD-L1, białka powierzchniowego, które może wyłączać limfocyty T przez zaangażowanie receptora PD-1, co sugeruje, że guzy broniły się przed tym nowym naciskiem immunologicznym.
Dlaczego sam PARP nie wystarcza — i skąd bierze się oporność
Naśladując opiekę nad pacjentem, badacze zastosowali u myszy początkowy cykl gemcytabiny i cisplatyny, a następnie leczenie podtrzymujące inhibitorem PARP, olaparibem. Ten schemat poprawił kontrolę guza i przeżycie w porównaniu z samą chemioterapią, potwierdzając, że uprzednie leczenie platyną może uczynić guzy bardziej wrażliwymi na inhibicję PARP. Jednak żadna mysz nie została wyleczona: guzy ostatecznie odrastały podczas leczenia podtrzymującego PARP. Guzy oporne wykazywały bardziej zróżnicowany wygląd i silnie podwyższone poziomy regulatora rozwoju CDX2. Sugeruje to, że przynajmniej w tym modelu oporność nie wynika wyłącznie z naprawy pierwotnego defektu naprawy DNA, lecz może obejmować zmianę tożsamości komórkowej guza. CDX2 może potencjalnie służyć jako biomarker wczesnej oporności u pacjentów.
Odblokowanie immunoterapii odpowiednią sekwencją
Leki przeciwko punktom kontrolnym immunologicznym, takie jak przeciwciała anty‑PD1, zrewolucjonizowały leczenie niektórych nowotworów, ale rak trzustki pozostaje w dużej mierze niewrażliwy. Zgodnie z tym, anty‑PD1 (z lub bez drugiego leku checkpoint, anty‑CTLA4) nie pomagał, gdy był podawany guzakom BRCA2-mutantym bez uprzedniego leczenia, i niewiele dawał, gdy był po prostu dodany do terapii inhibitorem PARP. Obraz zmienił się przy pełnej sekwencji: najpierw chemioterapia platynowa, a następnie leczenie podtrzymujące — PARP z dodatkiem anty‑PD1. W tym ustawieniu guzy kurczyły się mocniej, a myszy żyły dłużej niż po chemioterapii z PARP lub samym anty‑PD1. Dodanie anty‑CTLA4 do leczenia podtrzymującego PARP nie przyniosło podobnych korzyści, co sugeruje, że środowisko guza uprzednio przygotowane przez chemioterapię jest szczególnie predysponowane do odpowiedzi na zablokowanie PD‑1. 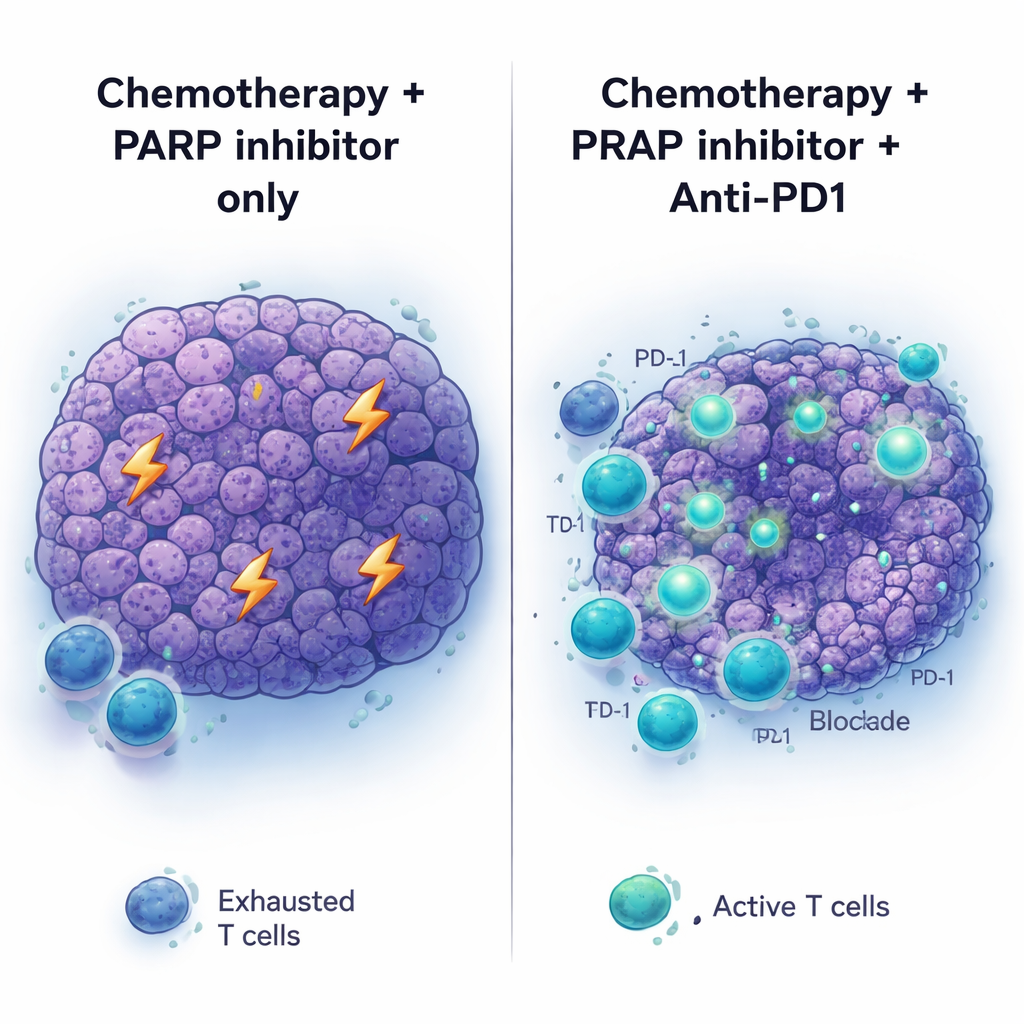
Co to może znaczyć dla przyszłej opieki
Podsumowując, badanie wskazuje, że w raku trzustki z mutacją BRCA kolejność i kombinacja terapii mają ogromne znaczenie. Silna chemioterapia uszkadzająca DNA nie tylko bezpośrednio atakuje komórki nowotworowe, lecz także wywołuje odpowiedź immunologiczną, nawet jeśli ta odpowiedź jest początkowo stłumiona przez wyczerpanie i obronę PD‑L1. Inhibitory PARP mogą wydłużyć korzyść, ale same rzadko bywają lecznicze i mogą popychać guzy w stronę opornego stanu z wysokim poziomem CDX2. Nakładanie immunoterapii anty‑PD1 na leczenie podtrzymujące PARP po chemioterapii platynowej może przekształcić tę krótkotrwale zapalną, wyczerpaną odpowiedź immunologiczną w bardziej skuteczną i trwałą reakcję przeciwnowotworową. Trwające badania kliniczne łączące inhibitory PARP z immunoterapią w raku trzustki związanym z BRCA będą kluczowe, by sprawdzić, czy ta starannie wyznaczona sekwencja da się przełożyć na dłuższe i lepsze życie pacjentów.
Cytowanie: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Słowa kluczowe: rak trzustki, mutacja BRCA2, chemioterapia platynowa, inhibitor PARP, immunoterapia PD-1