Clear Sky Science · pl
Wydajna synteza amidów bez rozpuszczalnika przez reakcję Rittera katalizowaną przez wielokrotnego użytku nanokompozyt Fe3O4/g-C3N4/NTMPA
Dlaczego czystsza chemia ma znaczenie
Wiele leków, tworzyw sztucznych i nawet włókien wysokowydajnych opiera się na prostym typie wiązania chemicznego zwanego wiązaniem amidowym. Wytwarzanie tych wiązań na skalę przemysłową zwykle wymaga silnych, żrących kwasów i dużych ilości rozpuszczalników, co generuje odpady i problemy z bezpieczeństwem. Artykuł opisuje nowy, magnetycznie reagujący katalizator stały, który potrafi tworzyć amidy w wysokich wydajnościach bez użycia rozpuszczalnika, wskazując drogę do bezpieczniejszej i bardziej zrównoważonej produkcji leków i materiałów.
Kluczowe ogniwo w lekach i materiałach
Amidy łączą łańcuchy białek i występują w niezliczonych farmaceutykach, agrochemikaliach oraz polimerach takich jak nylon. Chemicy dysponują wieloma metodami tworzenia wiązań amidowych, ale większość wymaga materiałów wyjściowych aktywowanych lub ostrych warunków reakcji. Reakcja Rittera wyróżnia się tym, że łączy prosty alkohol (lub alken) bezpośrednio z nitrilem w jednym etapie. W klasycznej postaci wymaga jednak stężonych kwasów mineralnych, takich jak kwas siarkowy czy solny. Te ciekłe kwasy są żrące, trudne do oddzielenia od produktów i trudne do ponownego wykorzystania, co czyni je mało odpowiednimi dla zielonej chemii.
Mały magnes, którym można mieszać
Naukowcy zaprojektowali stały katalizator możliwy do oddzielenia magnetycznie, który może zastąpić te ciekłe kwasy. Materiał łączy trzy składniki: nanocząstki tlenku żelaza (Fe3O4) nadające własności magnetyczne; warstwowy, bogaty w węgiel i azot materiał (grafitowy azotek węgla, g‑C3N4) pełniący rolę ochronnego nośnika; oraz silnie kwasową cząsteczkę nitrilotri(metylofosfonową) (NTMPA), dostarczającą kwasowość napędzającą reakcję. Elementy te są złożone tak, że NTMPA jest zakotwiczony na powierzchni g‑C3N4, a drobne cząstki Fe3O4 są wtopione w cały kompozyt. Ponieważ cały materiał reaguje na magnes, można go wyciągnąć z mieszaniny reakcyjnej po prostu przykładając magnes do zewnętrznej ścianki kolby.
Ustalenie struktury katalizatora
Aby potwierdzić, że zbudowano zamierzony materiał, autorzy użyli szeregu narzędzi z dziedziny nauki o materiałach. Spektroskopia w podczerwieni wykazała sygnały pochodzące od grup fosfonowych, struktury węglowo‑azotowej oraz wiązań żelazo–tlen, wszystkie obecne w ostatecznym kompozycje. Dyfrakcja rentgenowska wskazała, że magnetyczny tlenek żelaza zachował formę krystaliczną, podczas gdy azotek węgla pozostał warstwowym, częściowo nieuporządkowanym ciałem stałym. Mikroskopia elektronowa ujawniła cząstki o kształcie arkuszy ozdobione równomiernie rozmieszczonymi sferami w zakresie 10–20 nanometrów, a mapowanie pierwiastkowe pokazało równomierne rozproszenie żelaza, węgla, azotu, tlenu i fosforu. Pomiary powierzchni właściwej i rozmiaru porów potwierdziły mezoporowatą strukturę — pełną nanoskalowych kanałów umożliwiających dostęp reagentów do miejsc aktywnych — natomiast analiza termiczna wykazała stabilność materiału do kilkuset stopni Celsjusza.
Szybkie reakcje bez rozpuszczalnika
Po ustaleniu struktury zespół przetestował katalizator w reakcji Rittera między różnymi alkoholami i nitrylami. Okazało się, że najlepsze warunki były zaskakująco proste: równe ilości alkoholu i nitrylu, niewielka dawka stałego katalizatora, ogrzewanie do 80 °C i brak dodatkowego rozpuszczalnika. W tych warunkach wiele różnych substratów przekształciło się w odpowiadające amidy w wysokich do doskonałych wydajnościach, często powyżej 90%. Alkohole tercjarne i benzyliczne (które łatwiej tworzą reaktywny intermediat wymagany w reakcji Rittera) reagowały w ciągu zaledwie 1–4 godzin, podczas gdy trudniejsze substraty wymagały nieco dłuższego czasu. Zarówno aromatyczne, jak i alifatyczne nitryle działały dobrze; silnie odciągające grupy na aromatycznych nitrylach zwiększały wydajność reakcji. Ogólnie badanie wykazało, że stały katalizator może dorównać lub przewyższyć wiele ciekłych kwasów, unikając przy tym żrących mediów i dodatkowych rozpuszczalników.
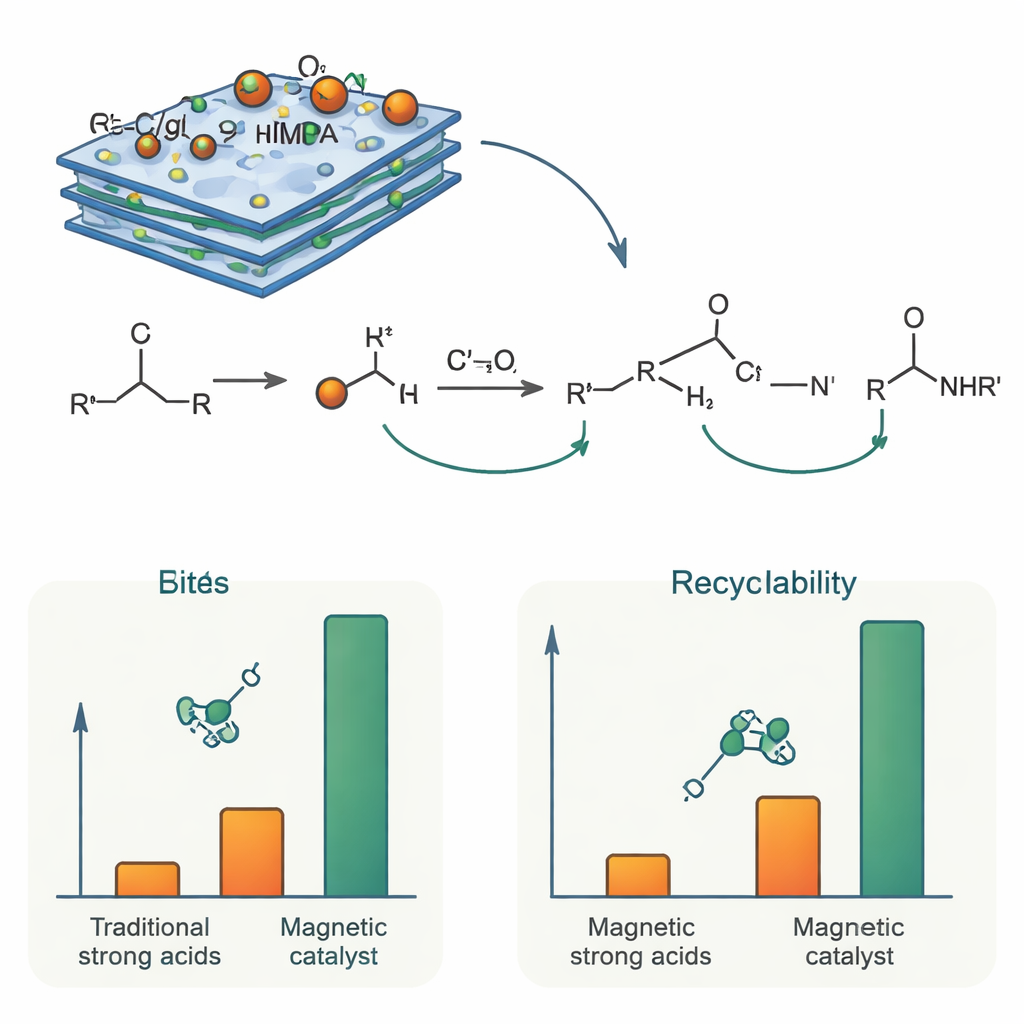
Jak to działa i dlaczego się utrzymuje
Chemicznie rola katalizatora polega na krótkotrwałym protonowaniu alkoholu i ułatwieniu utraty wody, tworząc nietrwały naładowany dodatnio międzyprodukt. Molekuła nitrylu atakuje następnie ten międzyprodukt tworząc nowe wiązanie węgiel–azot, które ostatecznie przekształca się w amid przez reakcję z wodą powstającą w trakcie procesu. Grupy fosfonowe w NTMPA dostarczają kontrolowanej kwasowości — na tyle silnej, by napędzać te kroki, ale złagodzonej przez powierzchnię azotku węgla, co minimalizuje niepożądane reakcje uboczne. Ponieważ aktywne jednostki NTMPA są chemicznie związane z nośnikiem stałym, nie wypłukują się podczas reakcji. Pomiary magnesowalności potwierdziły, że cząstki pozostają silnie magnetyczne, co pozwala szybko usunąć zużyty katalizator za pomocą magnesu. W testach powtórnego użycia ta sama porcja katalizatora została zastosowana co najmniej sześć razy przy jedynie niewielkim spadku aktywności, a analizy strukturalne po użyciu wykazały, że jego skład i morfologia pozostały w dużej mierze niezmienione.
Co to oznacza dla bardziej zielonej produkcji
Dla czytelnika nienależącego do specjalistów kluczowy wniosek jest taki, że autorzy opracowali wielokrotnego użytku, reagujący na magnes proszek, który może pomóc chemikom w tworzeniu ważnych wiązań amidowych bez polegania na ostrych ciekłych kwasach i dodatkowych rozpuszczalnikach zwykle wymaganych. Podejście to zmniejsza ilość odpadów, upraszcza oczyszczanie produktów i ułatwia recykling katalizatora — wszystko to ma znaczenie dla bardziej zielonej chemii przemysłowej. Chociaż praca koncentruje się na jednym typie reakcji, te same zasady projektowe — kotwiczenie silnych grup kwasowych na trwałym, magnetycznym nośniku — mogą być zastosowane w wielu innych przekształceniach istotnych dla produkcji leków i zaawansowanych materiałów.
Cytowanie: Karimitabar, H., Sardarian, A.R. Efficient solvent-free amide synthesis via Ritter reaction catalyzed by a reusable Fe3O4/g-C3N4/ NTMPA nanocomposite. Sci Rep 16, 6494 (2026). https://doi.org/10.1038/s41598-026-35371-2
Słowa kluczowe: synteza amidów, reakcja Rittera, magnetyczny nanokatalizator, chemia bez rozpuszczalnika, zielona kataliza