Clear Sky Science · pl
Rubiadin-1-methyl ether łagodzi włóknienie płuc wywołane bleomycyną
Dlaczego związek roślinny w chorobie z bliznowaceniem płuc ma znaczenie
Idiopatyczne włóknienie płuc to śmiertelna choroba, w której normalna, gąbczasta tkanka płucna stopniowo zostaje zastąpiona sztywną tkanką bliznowatą, utrudniając każde wdechy. Dostępne leki mogą spowalniać to bliznowacenie, ale rzadko je zatrzymują, a często wywołują skutki uboczne. W tym badaniu sprawdzono, czy rubiadin‑1‑methyl ether (RBM) — związek naturalny występujący w korzeniach kilku powszechnych roślin — może złagodzić włóknienie płuc w dobrze ugruntowanym modelu myszy. Praca bada także, jak RBM wpływa na komórki układu odpornościowego, które przyczyniają się do tego uszkodzenia.
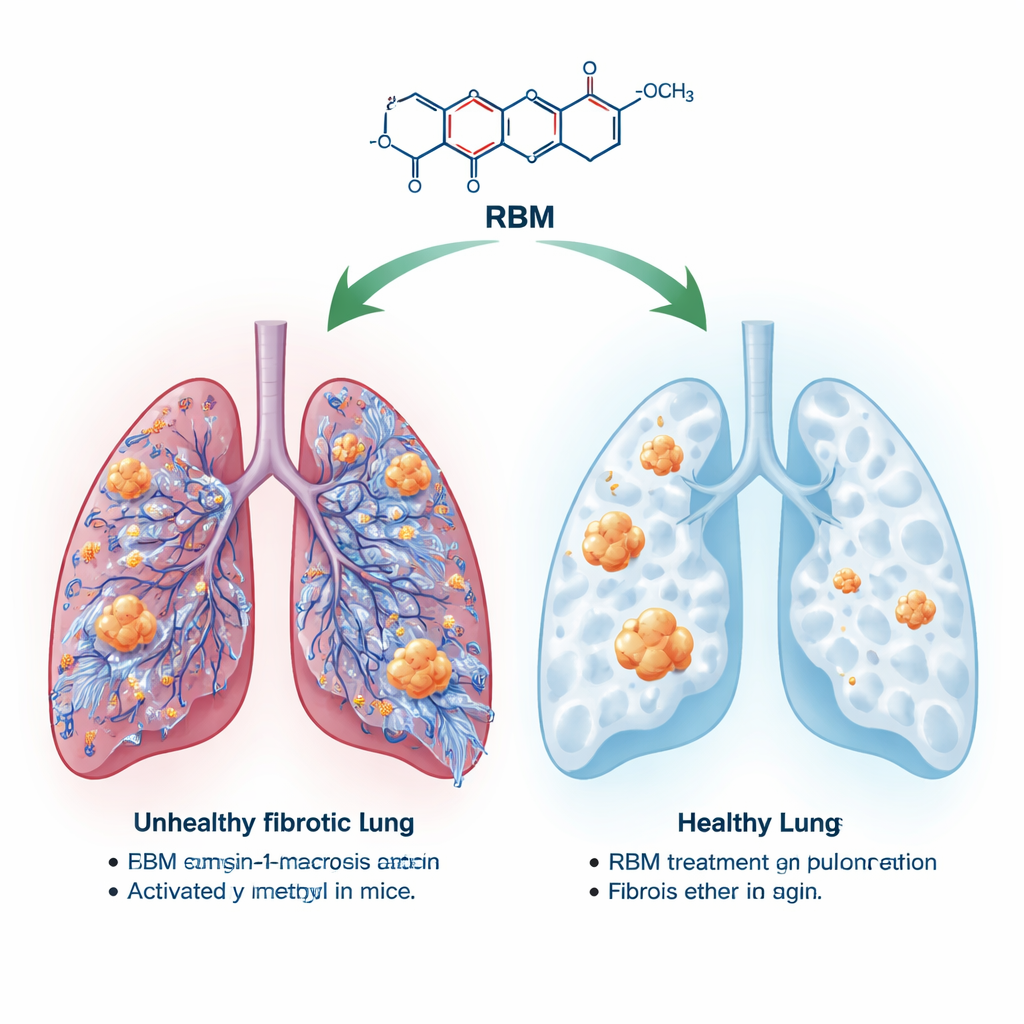
Bliższe spojrzenie na bliznowacenie w płucach
W włóknieniu płuc nadmiar tkanki łącznej, zwanej macierzą pozakomórkową, wypełnia płuca i zaburza ich delikatną architekturę. Pacjenci często żyją zaledwie trzy do pięciu lat po rozpoznaniu, a opcje terapeutyczne ograniczają się do leków spowalniających pogorszenie, zamiast naprawdę naprawiać płuca. Naukowcy wiedzą, że cząsteczka sygnałowa zwana TGF‑β1 oraz proces przejścia nabłonkowo‑mezenchymalnego odgrywają kluczową rolę w tym bliznowaceniu. Wiele szczegółów — zwłaszcza jak komórki odpornościowe i związki pochodzenia roślinnego modulują te szlaki — wciąż jest odkrywanych.
Związek roślinny z medyczną przeszłością
RBM należy do rodziny związków naturalnych zwanych antrachinonami, które występują w roślinach z rodziny marzanowatych (Rubiaceae), takich jak Rubia cordifolia i gatunki Morinda. Związki z tej grupy badano pod kątem działania od przeczyszczającego po przeciwnowotworowe i przeciwmalaryczne. Wcześniejsze prace wykazały, że RBM może tłumić sygnały zapalne, takie jak tlenek azotu i niektóre interleukiny, oraz wpływać na rozwój komórek tłuszczowych. Ekstrakty bogate w RBM i pokrewne molekuły wykazały ostatnio zdolność łagodzenia włóknienia płuc u zwierząt, co sugeruje, że sam RBM może być istotnym składnikiem aktywnym. Do tej pory jednak jego bezpośredni wpływ na bliznowacenie płuc i szczegółowy mechanizm działania pozostawały niejasne.
Testowanie RBM w modelu myszy z urazem płuc
Aby naśladować ludzkie włóknienie płuc, badacze podali myszom jednorazową dawkę leku chemioterapeutycznego bleomycyny do tchawicy, co wiarygodnie wywołuje zapalenie i bliznowacenie płuc. Po tym urazie zwierzęta otrzymywały różne dawki RBM doustnie (3, 10 lub 30 mg na kilogram masy ciała). Przez trzy tygodnie zespół monitorował masę ciała, masę płuc w stosunku do masy ciała oraz mikroskopowe zmiany w tkance płucnej przy użyciu standardowych barwień uwidaczniających uszkodzenia i depozyty kolagenu. Badano także próbki płukania płuc w celu policzenia komórek zapalnych i zmierzenia kluczowych mediatorów sygnalizacyjnych, oraz użyto metod molekularnych do oceny genów powiązanych z bliznowaceniem i ze specyficznym stanem komórek odpornościowych znanym jako makrofag M2.
Mniej zapalenia, mniej markerów bliznowacenia i spokojniejsze komórki odpornościowe
Dawka 10 mg/kg RBM okazała się optymalna. Myszy otrzymujące jedynie bleomycynę traciły na wadze, rozwijały ciężkie, wypełnione kolagenem płuca i wykazywały poważne zniekształcenia pęcherzyków płucnych. RBM w dawce 10 mg/kg częściowo odwrócił te zmiany: utrata masy ciała była mniejsza, struktura płuc wyglądała bliżej normalnej, a ilość tkanki bliznowatej bogatej w kolagen zmalała. W płynie z płukania płuc RBM zmniejszył całkowitą liczbę komórek zapalnych niemal o połowę, ze szczególnie silnym spadkiem neutrofili — rodzaju białych krwinek powiązanych z ostrym uszkodzeniem. Geny kodujące główne białka budujące blizny — fibrynę, kolagen typu I i alfa‑aktynę mięśni gładkich — były znacząco obniżone po leczeniu RBM. Co ważne, RBM także zmniejszył poziomy mediatorów zapalnych i pro‑fibrotycznych, takich jak TGF‑β1, IL‑6, IL‑1β i TNF‑α, oraz przesunął populację makrofagów z dala od stanu M2, który jest znany z promowania włóknienia. Markery M2 na powierzchni komórek i wewnątrz komórek obniżyły się istotnie.
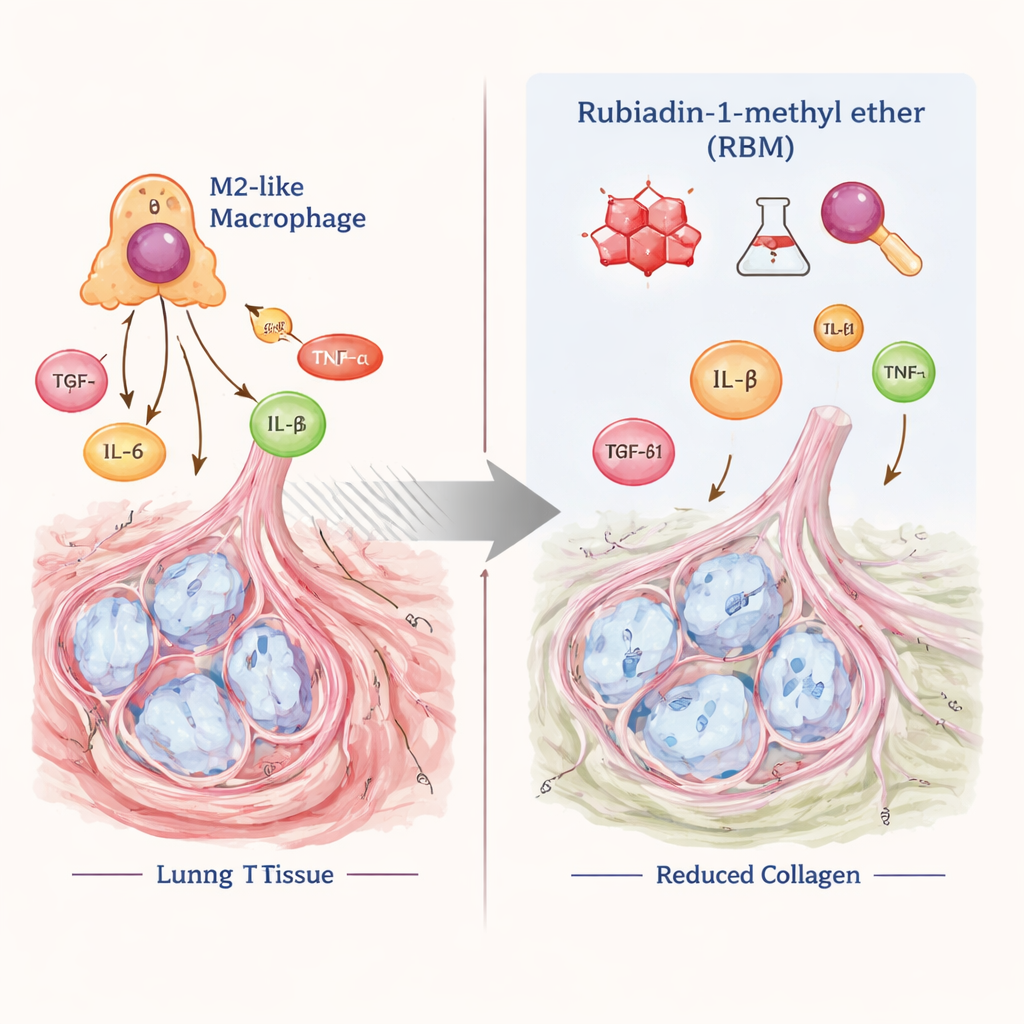
Jak RBM może przebudowywać środowisko płuc
Makrofagi to komórki odpornościowe, które mogą pomagać w gojeniu tkanek, ale w chorobach przewlekłych mogą też nakłaniać narządy do włóknienia. Typ M2 makrofagów, choć w niektórych sytuacjach przeciwzapalny, jest coraz częściej uznawany za czynnik napędzający bliznowacenie płuc, ponieważ wydziela TGF‑β1 i inne czynniki wzrostu stymulujące komórki produkujące kolagen. W tym badaniu RBM wydaje się działać jak hamulec dla tej szkodliwej pętli: ograniczając polaryzację w kierunku M2 i obniżając wydzielanie TGF‑β1, związek prawdopodobnie osłabia sygnały nakazujące komórkom płucnym odkładać więcej tkanki bliznowatej. Autorzy sugerują, że RBM interferuje z szlakiem sygnalizacyjnym TGF‑β1/Smad — centralnym węzłem we włóknieniu — chociaż zauważają, że potrzebne są dalsze badania mechanistyczne, aby potwierdzić dokładne cele molekularne.
Co to może oznaczać dla przyszłych terapii
Dla czytelników niebędących specjalistami najważniejsze jest to, że naturalnie występujący związek roślinny zmniejszył u myszy stan zapalny, ograniczył bliznowacenie i zmniejszył liczbę komórek odpornościowych sprzyjających włóknieniu. RBM nie wyleczył włóknienia całkowicie, a najwyższa dawka nie działała lepiej — być może dlatego, że nadmiar może wprowadzać nowe obciążenia dla tkanki płucnej. Mimo to wyniki stawiają RBM jako obiecującego kandydata do dalszego rozwoju jako łagodniejsza, pochodzenia roślinnego terapia dla idiopatycznego włóknienia płuc, schorzenia o ograniczonych możliwościach leczenia. Zanim będzie można go przetestować u ludzi, badacze będą musieli wyjaśnić, jak związek jest wchłaniany i metabolizowany w organizmie, sprawdzić go w większych i bardziej przypominających ludzkie modelach zwierzęcych oraz zbadać, czy może bezpiecznie wzmocnić działanie istniejących leków spowalniających bliznowacenie płuc.
Cytowanie: Zhen, X., Xinpeng, L., Jing, S. et al. Rubiadin-1-methyl ether alleviates bleomycin induced pulmonary fibrosis. Sci Rep 16, 4864 (2026). https://doi.org/10.1038/s41598-026-35352-5
Słowa kluczowe: idiopatyczne włóknienie płuc, polaryzacja makrofagów, terapia produktami naturalnymi, sygnalizacja TGF-beta, włóknienie płuc