Clear Sky Science · pl
System znacznika REC pozbawiony lizyny do zastosowań w biotynylacji w bliskości
Dlaczego małe znaczniki na białkach mają znaczenie
W każdej komórce białka rzadko działają samotnie — tworzą zmienne partnerstwa, które napędzają zdrowie i chorobę. Aby zbadać te partnerstwa, naukowcy często przyczepiają do białek małe „identyfikatory”, dzięki którym można je śledzić, wyizolować z mieszaniny lub zobaczyć pod mikroskopem. Popularna metoda nazwana biotynylacją w bliskości pozwala odwzorować, kto stoi obok kogo wewnątrz komórki, ale ma ukryty problem: wiele z tych identyfikatorów ulega chemicznej modyfikacji i efektywnie „znika” właśnie wtedy, gdy są najbardziej potrzebne. W tym badaniu przedstawiono nowy rodzaj znacznika, nazwany REC, zaprojektowany tak, by pozostać wykrywalnym w tych wymagających warunkach.
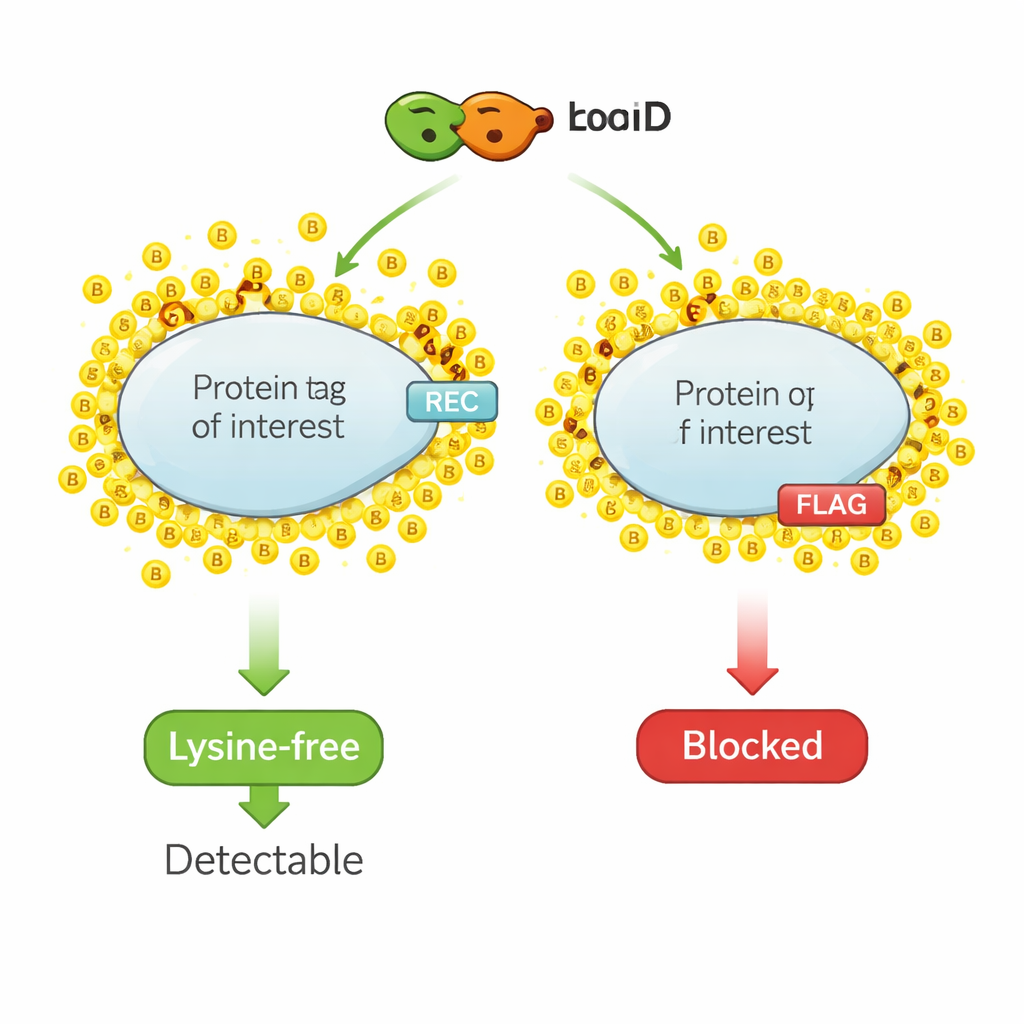
Chemiczny marker dla sąsiadów białkowych
Biotynylacja w bliskości działa jak molekularny zakreślacz. Zmodyfikowany enzym, taki jak TurboID, łączy się z białkiem zainteresowania. Po dodaniu biotyny — małej witaminy — TurboID szybko przyłącza cząsteczki biotyny do pobliskich białek. Naukowcy potem wyławiają wszystkie biotynylowane białka i identyfikują je, uzyskując migawkę lokalnego sąsiedztwa białka. Jednak ta sama chemia, która znakuję pobliskie białka, również atakuje małe epitopowe znaczniki powszechnie używane do detekcji, ponieważ te znaczniki zwykle zawierają lizynę — aminokwas będący głównym miejscem przyłączania biotyny. Gdy lizyny w znaczniku zostaną pokryte biotyną, przeciwciała przestają rozpoznawać znacznik, a sygnał w standardowych metodach detekcji maleje lub znika.
Projekt znacznika, który odmawia modyfikacji
Aby rozwiązać ten problem, autorzy postawili sobie za cel stworzenie nowego znacznika całkowicie pozbawionego lizyny. Rozpoczęli od fragmentu białka pasożyta malarii nazwanego PfRipr5, które ma niewielkie podobieństwo do białek ludzkich, co zmniejsza ryzyko niepożądanych reakcji krzyżowych. Przy użyciu metody przesiewowej opartej na mikrochipie w królikach wygenerowali 22 przeciwciała monoklonalne przeciw PfRipr5 i zidentyfikowali jedno, oznaczone klonem nr 6, wykazujące szczególnie silne i specyficzne wiązanie. Poprzez systematyczne przycinanie i mutacje fragmentu PfRipr5 zawęzili cel przeciwciała do 11–aminokwasowego odcinka. Ta minimalna sekwencja zawierała tylko jedną lizynę, którą zastąpili podobnym aminokwasem — argininą. Co ciekawe, przeciwciało nadal wiązało się równie dobrze. Ta zoptymalizowana, pozbawiona lizyny sekwencja została nazwana znacznikiem REC, a dopasowane przeciwciało — przeciwciałem REC.
Testowanie znacznika REC w praktyce
Zespół następnie sprawdził, czy znacznik REC może zastąpić powszechnie używane znaczniki, takie jak FLAG, w standardowych technikach laboratoryjnych. Po zespoleniu z białkami fluorescencyjnymi lub sygnalizacyjnymi i wytworzeniu w systemach bezkomórkowych oraz komórkach ssaczych, białka z znacznikiem REC były łatwo wykrywalne przez immunoblotting, czuły test płytkowy oparty na świetle zwany AlphaScreen oraz przez immunobarwienie w komórkach. Siła detekcji była podobna do znacznika FLAG i innego systemu pozbawionego lizyny (AGIA), a przeciwciało REC wykazywało bardzo niewielkie tło w różnych liniach komórkowych człowieka i małpy. Co ważne, znacznik działał zarówno umieszczony na początku, jak i na końcu białka, oraz na białkach zlokalizowanych w różnych regionach komórkowych, w tym w jądrze, mitochondriach, retikulum endoplazmatycznym i błonie komórkowej.
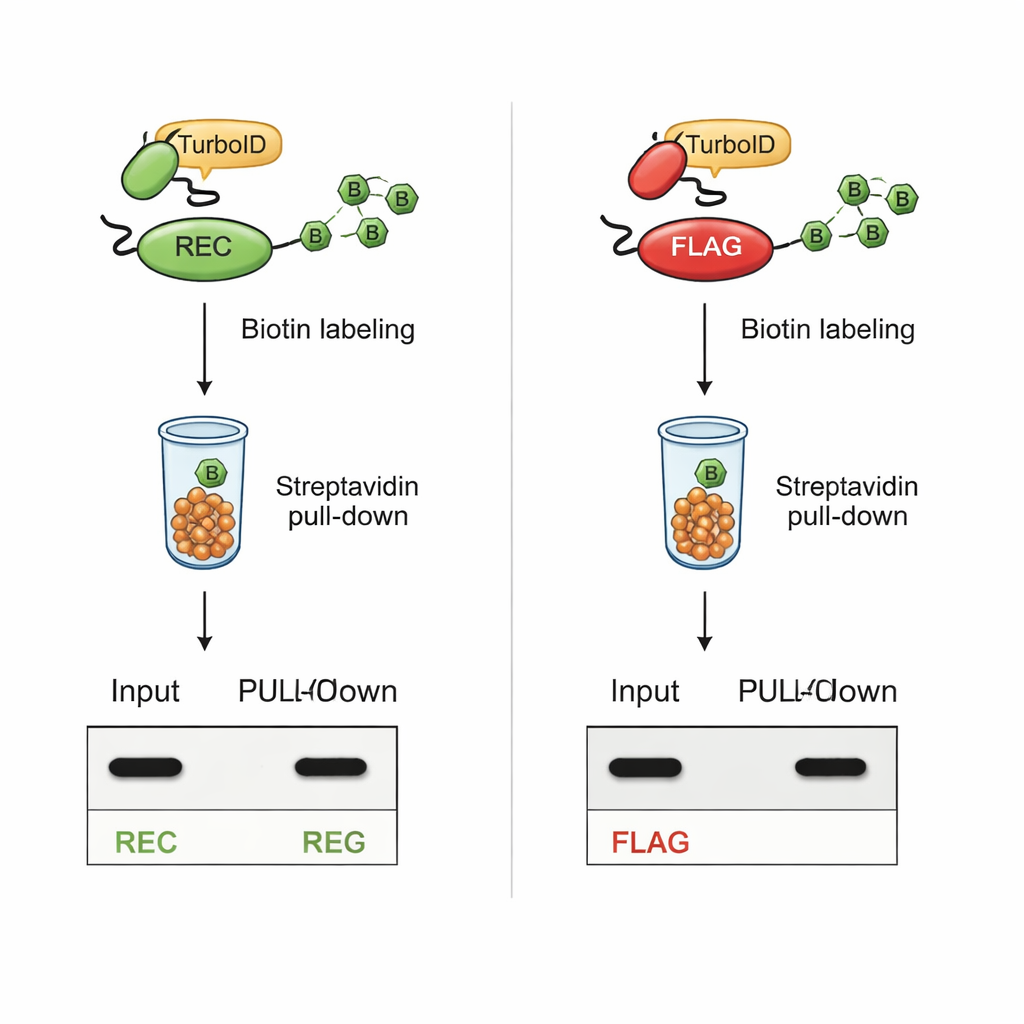
Pozostawanie widocznym podczas intensywnego znakowania
Krytyczny test polegał na sprawdzeniu, czy REC pozostanie wykrywalny po biotynylacji opartej na TurboID. W komórkach, gdzie TurboID było zespolone ze znanymi partnerami interakcji, białka niosące znacznik REC pozostały wyraźnie widoczne zarówno w ekstraktach całokomórkowych, jak i w oczyszczonej, biotynylowanej frakcji. W przeciwieństwie do tego, białka z klasycznym znacznikiem FLAG utraciły sygnał FLAG po aktywacji TurboID, mimo że same białka były nadal obecne. Dodatkowe eksperymenty z syntetycznymi peptydami wykazały, że TurboID bezpośrednio biotynyluje lizyny w sekwencji FLAG, fizycznie blokując dostęp przeciwciała. Znacznik REC, nieposiadający w ogóle lizyny, pozostał nienaruszony przez TurboID i nadal był łatwy do wykrycia.
Co to oznacza dla przyszłych eksperymentów
Dla badaczy badających sieci białkowe w żywych komórkach, znacznik REC oferuje praktyczne nowe narzędzie: zachowuje się jak znane znaczniki w codziennych testach, ale nadal działa, gdy aktywne są silne enzymy znakowania w bliskości. Oznacza to, że naukowcy mogą bardziej wiarygodnie potwierdzić obecność i prawidłowe wychwycenie znakowanych białek oraz badać inne modyfikacje oparte na lizynie — takie jak ubikwitynacja i acetylacja — bez zakłóceń ze strony samego znacznika. Krótko mówiąc, REC to niewielka zmiana konstrukcyjna o dużym znaczeniu, pomagająca uczynić skomplikowane eksperymenty mapowania białek bardziej przejrzystymi i godnymi zaufania.
Cytowanie: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Słowa kluczowe: znakowanie białek, biotynylacja w bliskości, TurboID, interakcje białek, epitopowe znaczniki