Clear Sky Science · pl
Interakcja między metylacją DNA ELMO1 a Med31 sprzyja EMT i metaplazji jelitowej indukowanej przez H. pylori poprzez polaryzację M2
Dlaczego bakterie żołądkowe mają znaczenie dla ryzyka raka
Większość z nas nosi miliardy bakterii w przewodzie pokarmowym, a jedna z nich — Helicobacter pylori — może cicho bytować w żołądku przez dziesięciolecia. U niektórych osób ta infekcja jest bezobjawowa, ale u innych staje się pierwszym krokiem w kierunku raka żołądka, jednego z najgroźniejszych nowotworów na świecie. Badanie to analizuje, jak drobna chemiczna zmiana w DNA komórek żołądka pomaga przemienić długotrwałą infekcję w uszkodzenie przedrakowe, a w końcu w środowisko sprzyjające rozwojowi nowotworu.
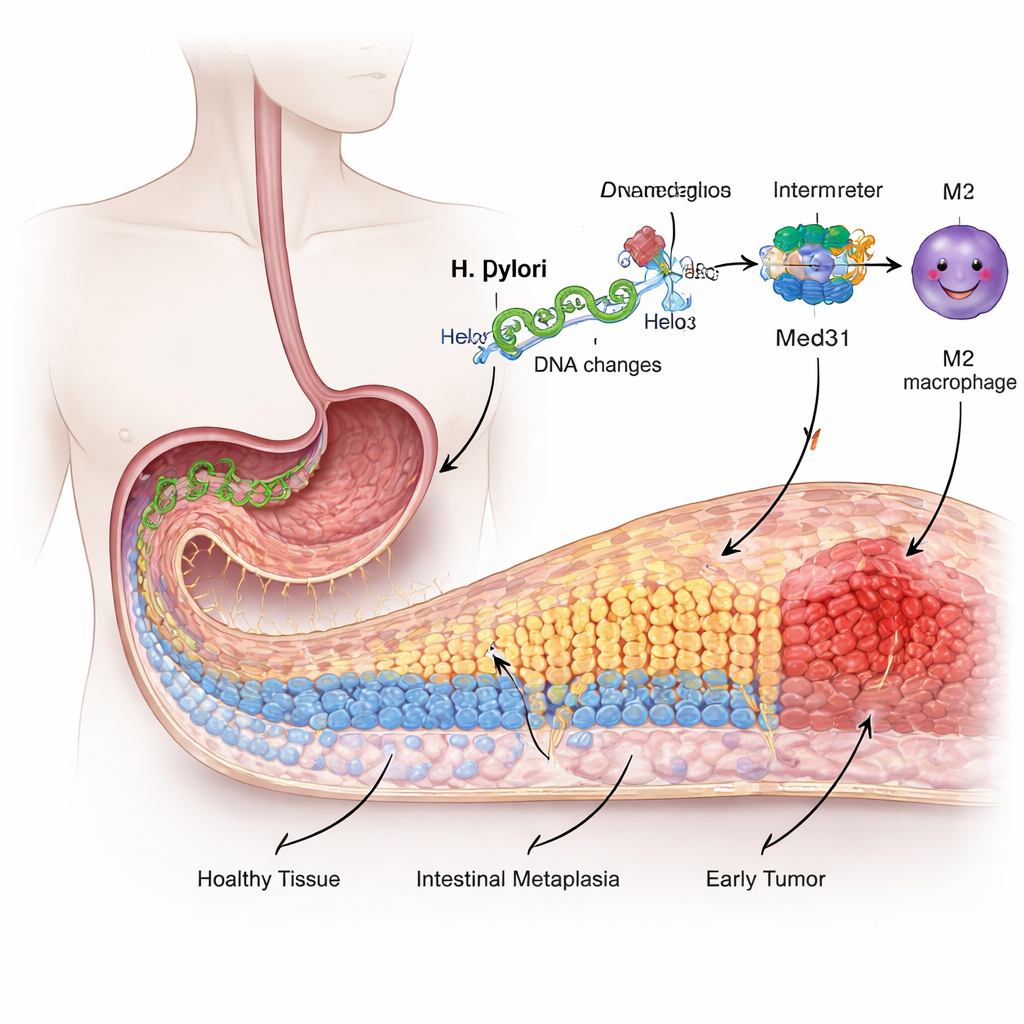
Z przyjaznej wyściółki do ryzykownej przemiany
Wewnętrzna powierzchnia żołądka pokryta jest wyspecjalizowanymi komórkami przystosowanymi do radzenia sobie z silnym kwasem, a nie do trawienia pokarmu jak w jelicie. Pod wpływem wieloletniego drażnienia i stanu zapalnego wywołanego przez H. pylori część tych komórek żołądka zaczyna się „przebudowywać”, przejmując cechy komórek jelitowych w procesie zwanym metaplazją jelitową. Ta zmiana jest uważana za etap przedrakowy. Badacze użyli ludzkiej linii komórek żołądkowych, aby naśladować infekcję, i stwierdzili, że ekspozycja na H. pylori powodowała, iż komórki te szybciej się dzieliły, łatwiej się poruszały i włączały markery typu jelitowego — wszystkie to sygnały, że wyściółka odchodzi od swojej normalnej tożsamości.
Małe chemiczne znaczniki o dużych konsekwencjach
Nasze DNA może być oznaczane drobnymi grupami chemicznymi zwanymi grupami metylowymi, które działają jak przełączniki włącz/wyłącz dla genów, nie zmieniając przy tym samego kodu genetycznego. Zespół skupił się na genie ELMO1, już znanym z udziału w ruchliwości komórek i przerzutowaniu nowotworów. Wykazali, że infekcja H. pylori zwiększa metylację genu ELMO1 i, co paradoksalne, podnosi jego aktywność oraz poziom białka w komórkach żołądka. Gdy zastosowano lek usuwający te metylowe znaczniki, komórki traciły wiele zmian wywołanych przez infekcję: dzieliły się rzadziej, mniej się przemieszczały i wykazywały mniej sygnałów metaplazji jelitowej. Wskazuje to na metylację ELMO1 jako kluczowy przełącznik włączany przez bakterię.
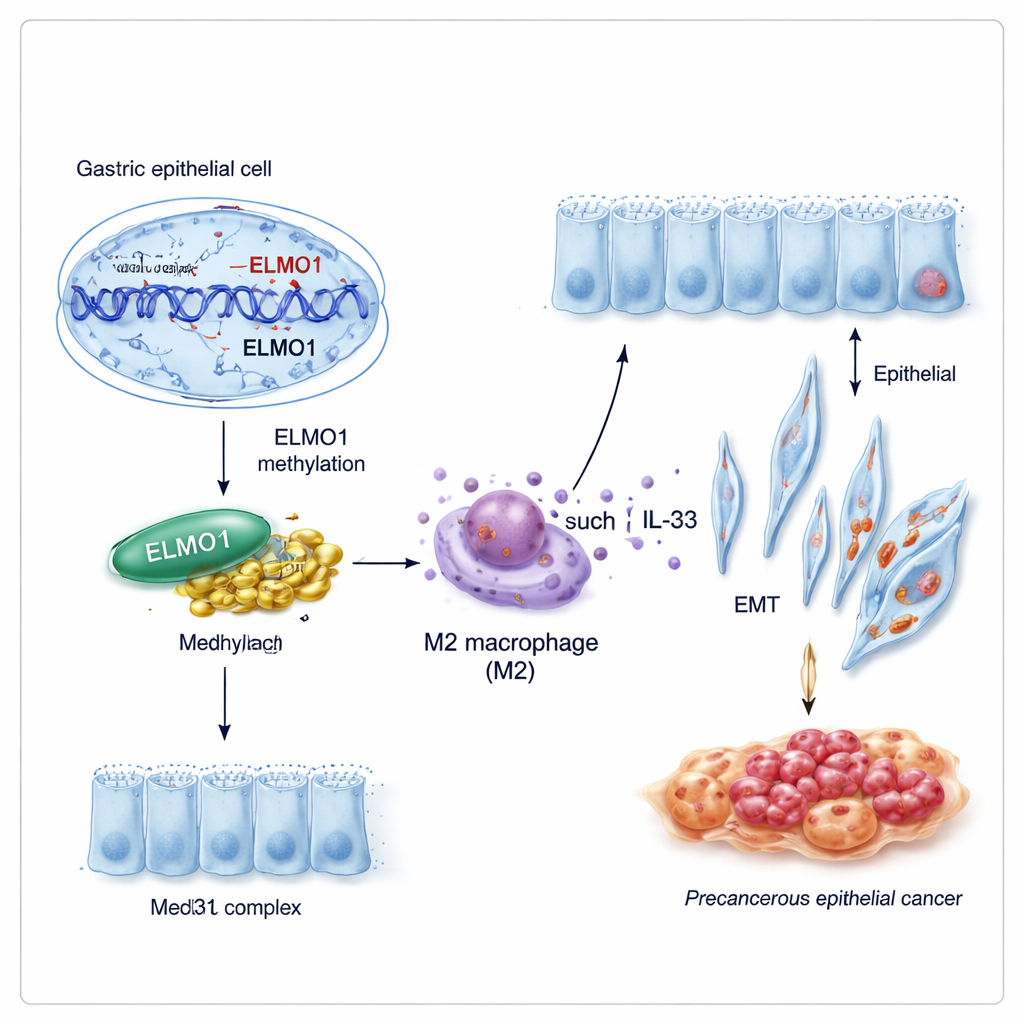
Nowe partnerstwo, które przebudowuje zachowanie komórek
Geny rzadko działają samodzielnie. Badacze odkryli, że metylowany ELMO1 sprzyja współpracy z innym białkiem, Med31, będącym częścią dużej „płyty sterującej”, która pomaga decydować, które geny komórka włącza. W warunkach sprzyjających metylacji DNA poziomy ELMO1 rosły, Med31 zwiększał swoją obecność i obydwa białka fizycznie się wiązały, podczas gdy wcześniej znany partner ELMO1, DOCK10, został odsunięty na boczny tor. Nowy duet ELMO1–Med31 wydaje się zmieniać program ekspresji genów w komórkach żołądka w sposób zachęcający je do przyjmowania cech jelitowych i bardziej agresywnego zachowania.
Jak komórki odpornościowe są nakierowywane, by pomagać guzowi
Nowotwór nie rozwija się w izolacji; rośnie w złożonym sąsiedztwie komórek odpornościowych i podporowych. Badanie pokazuje, że zakażone komórki żołądkowe z metylowanym ELMO1 wydzielają wyższe poziomy IL‑33, sygnału, który skłania pobliskie komórki odpornościowe zwane makrofagami do przyjęcia sprzyjającego guzowi stanu „M2”. W systemie ko‑hodowli autorzy stwierdzili, że makrofagi wystawione na te sygnały silnie przesuwały się w stronę fenotypu M2 i z kolei wydzielały czynniki, które skłaniały świeże komórki żołądka do większej ruchliwości, inwazyjności i przyjmowania cech jelitowych. Markery przejścia nabłonkowo‑mezenchymalnego — gdy stacjonarne komórki wyściółki przekształcają się w wędrujące, zdolne do inwazji komórki — wzrastały gwałtownie pod wpływem tych makrofagów M2.
Co to oznacza dla zapobiegania rakowi żołądka
Podsumowując, praca ta kreśli łańcuch zdarzeń: infekcja H. pylori zmienia metylację DNA ELMO1, zmodyfikowany ELMO1 łączy się z Med31, zakażone komórki wysyłają sygnały przekształcające pobliskie komórki odpornościowe w pomocników M2, a ci pomocnicy napędzają zarówno metaplazję jelitową, jak i bardziej inwazyjny stan komórek. Dla osób niezajmujących się tą dziedziną kluczowa idea jest taka, że powszechna bakteria żołądkowa może przekształcić zarówno wyściółkę żołądka, jak i lokalną odpowiedź immunologiczną za pomocą odwracalnych chemicznych znaczników na DNA. Zrozumienie tej ścieżki może otworzyć drogę do nowych badań krwi wykrywających wczesne wzorce ryzykownej metylacji, a także leków zakłócających oś ELMO1–Med31–M2 zanim przewlekła infekcja przejdzie w raka żołądka.
Cytowanie: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Słowa kluczowe: rak żołądka, Helicobacter pylori, metylacja DNA, metaplazja jelitowa, mikrośrodowisko guza