Clear Sky Science · pl
Modelowanie i eksperymentalna weryfikacja precypitacji nanocząstek polikaprolaktonu
Dlaczego małe plastikowe kulki mają znaczenie dla medycyny
Wyobraź sobie umieszczenie silnego leku w punkcie tak małym, że może przesunąć się przez naczynia krwionośne i uwolnić ładunek dokładnie tam, gdzie jest potrzebny. Takie cząstki, nazywane nanocząstkami polimerowymi, stanowią trzon wielu nowych terapii i narzędzi obrazowania. Jednak wytworzenie ich o odpowiednim i powtarzalnym rozmiarze bywa zaskakująco trudne. W tym badaniu pokazano, jak prosty, oparty na fizyce model komputerowy może przewidywać i regulować rozmiar powszechnie stosowanej biodegradowalnej nanocząstki, co potencjalnie skraca o lata proces prób i błędów w opracowywaniu nowych nanoleków.
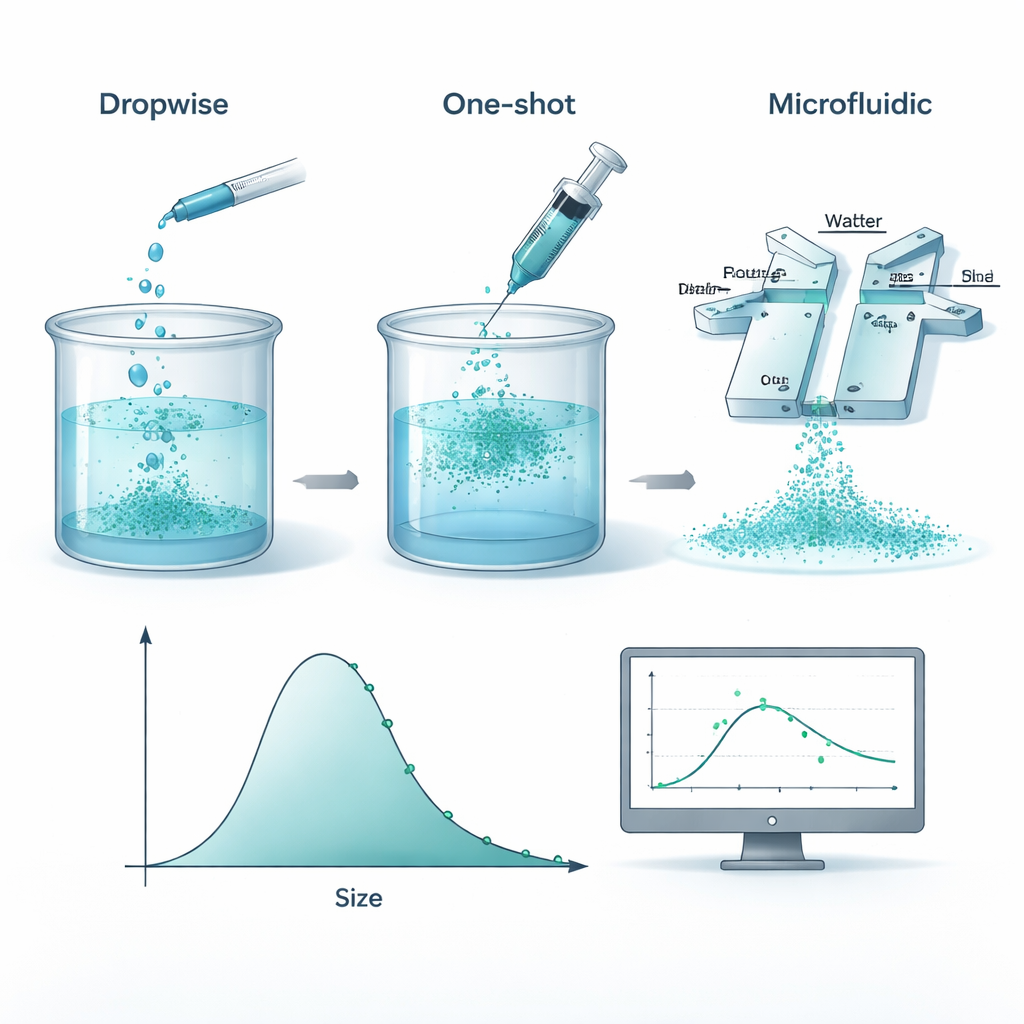
Od kuchennego mieszania po laboratoryjną precyzję
Aby stworzyć te nanocząstki, badacze rozpuszczają biodegradowalny plastik zwany polikaprolaktonem (PCL) w rozpuszczalniku organicznym, a następnie mieszają go z wodą, tak że polimer „wytrąca się” z roztworu i formuje drobne kuleczki. Zespół porównał trzy praktyczne metody: powolne dodawanie roztworu polimeru kropla po kropli, wlaniem go jednorazowo oraz wtłaczanie obu cieczy przez mały chip mikrofluidyczny, gdzie spotykają się w wąskich kanałach. Przy dokładnie kontrolowanych warunkach wszystkie trzy podejścia dały cząstki o bardzo podobnych średnich rozmiarach i rozkładach wielkości. Oznacza to, że przynajmniej w badanych zakresach ważniejsze niż dokładne narzędzie mieszające są składniki—ilość polimeru i stabilizatora—a nie sposób mieszania.
Jak lepkość i molekuły pomocnicze kształtują cząstki
Następnie badacze zbadali, jak skład przepisu kontroluje końcowy rozmiar cząstek. Zwiększenie ilości PCL w fazie organicznej sprawia, że ta ciecz staje się gęstsza, czyli bardziej lepka. Pomyśl o mieszaniu syropu z wodą zamiast soku: gęstszy syrop rozbija się na większe krople. W tym przypadku gęstsze roztwory polimeru prowadziły do większych nanocząstek i nieco szerszych rozkładów wielkości. Dodanie drugiego rozpuszczalnika, etanolu, pomogło utrzymać stabilność procesu nawet przy bardzo wysokich poziomach polimeru, ale kosztem powiększenia cząstek w górnym zakresie stężeń. Drugi składnik, surfaktant zwany Pluronic F‑127, działa jak molekularny środek przeciwzbrylający. Przy niskich stężeniach surfaktantu cząstki mają tendencję do zderzania się i zlepiania, rosnąc i stając się mniej jednorodnymi. Wraz ze wzrostem stężenia surfaktantu pokrywa on powierzchnie cząstek, zapobiega ich łączeniu i daje mniejsze, bardziej stabilne nanocząstki—do pewnego punktu, po którym dalsze zwiększanie daje skromne korzyści, a rozkład wielkości może stać się bardziej zróżnicowany.
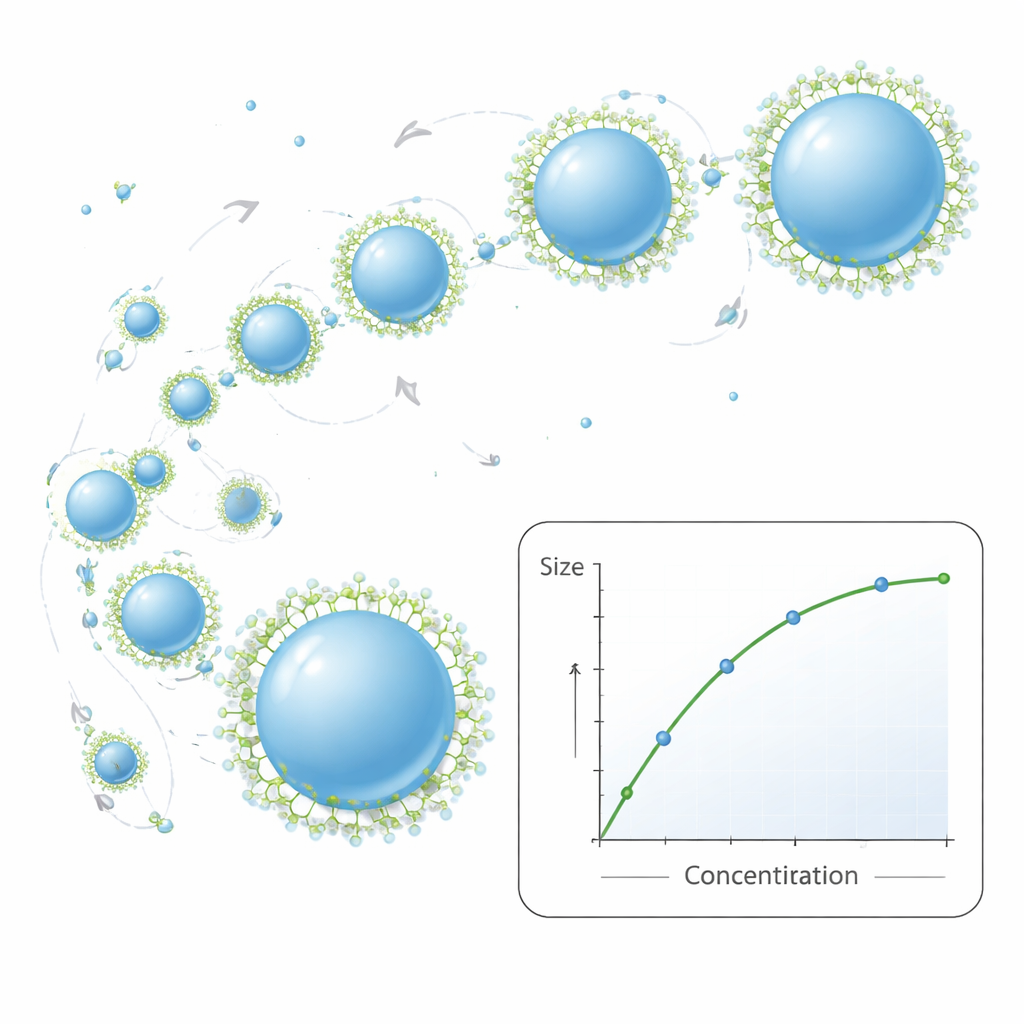
Prosta zasada wzrostu zgodna z rzeczywistością
U podstaw pracy leży zwarty model matematyczny opisujący, jak nanocząstki rosną po ich początkowym powstaniu. Traktuje się ich ruch jako przypadkowe drgania w cieczy, gdzie zderzenia czasami prowadzą do połączenia dwóch cząstek w większą. Wcześniejsze modele zakładały, że gdy cząstki się spotkają, natychmiast się scalają i stają się idealnymi kulami. Nowy model dodaje dwa realistyczne elementy: po pierwsze pozwala na skończony czas, w którym dwie stykające się cząstki relaksują się z wydłużonego kształtu do pojedynczej kuli; po drugie umożliwia surfaktantom stopniowe „blokowanie” powierzchni, spowalniając lub zatrzymując dalsze łączenie. Mając jedynie kilka mierzalnych wejść—takich jak temperatura, lepkość cieczy i początkowe stężenie polimeru—model przewiduje, jak średni rozmiar cząstek powinien zmieniać się przy różnych warunkach recepturowych. W wielu eksperymentach przewidywane rozmiary ściśle odpowiadały tym zmierzonym metodą rozpraszania światła, a jednocześnie model uchwycił ogólne tendencje dotyczące szerokości rozkładu wielkości.
Wykorzystanie modelu jako narzędzia projektowego
Aby sprawdzić, czy podejście jest naprawdę użyteczne, zespół odwrócił zadanie: zamiast prosić model o wyjaśnienie danych z przeszłości, poprosił go o zaproponowanie receptur, które powinny dać trzy konkretne rozmiary nanocząstek i stopnie jednorodności. Następnie przygotowali te „zaprojektowane” formulacje w laboratorium. Zmierzane średnice cząstek różniły się od założeń tylko o 1–7 procent—w granicach typowej zmienności eksperymentalnej—co pokazuje, że model może niezawodnie ukierunkować wybór składu. Prognozy dotyczące tego, jak wąski lub szeroki będzie rozkład wielkości, były mniej dokładne, ale nadal wystarczające do rozróżnienia stosunkowo jednorodnych i bardziej rozstrzelonych populacji. W porównaniu z zaawansowanymi metodami symulacyjnymi, które śledzą każdą cząsteczkę lub każdy wir przepływu, uproszczony model działa szybko na skromnych komputerach i łatwo go dostosować do innych polimerów i układów przetwarzania.
Co to oznacza dla przyszłości nanomedycyny
Dla osób niezajmujących się specjalistycznie kluczowy przekaz jest taki, że wytwarzanie użytecznych nanocząstek nie musi już opierać się wyłącznie na mozolnych próbach i błędach w laboratorium. Poprzez uchwycenie istotnej fizyki dotyczącej tego, jak małe plastikowe krople poruszają się, zderzają i są chronione przez surfaktanty, praca ta dostarcza praktycznej „mapy” łączącej wybory formulacyjne—ile polimeru, jaki miks rozpuszczalników, ile stabilizatora—z końcowym rozmiarem cząstek. Ponieważ PCL jest powszechnie stosowanym biodegradowalnym materiałem w dostarczaniu leków, implantach i środkach obrazowania, model ten może pomóc badaczom szybciej projektować bezpieczniejsze i skuteczniejsze nanoleki, zużywając mniej materiałów. Te same zasady można rozszerzyć na inne polimery, przynosząc większą przewidywalność i efektywność do świata terapii na poziomie nano.
Cytowanie: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Słowa kluczowe: nanocząstki polimerowe, nanoprecypitacja, dostarczanie leków, modelowanie numeryczne, polikaprolakton