Clear Sky Science · pl
Nicorandil łagodzi ból neuropatyczny i zapalny poprzez sygnalizację TNF-α, IL6/MAPKERK1/2 oraz NO/cGMP
Dlaczego łagodzenie bólu nerwowego ma znaczenie
Miliony ludzi żyją z piekącym, przeszywającym lub mrowiącym bólem, który utrzymuje się długo po wygojeniu urazu. Ten „ból neuropatyczny” może być oporny na powszechne środki przeciwbólowe i często wiąże się z działaniami niepożądanymi przy długotrwałym stosowaniu leków. Badanie podsumowane tutaj bada, czy nikorandyl — lek sercowy już podawany pacjentom z dusznicą — mógłby także uspokoić nadaktywne szlaki bólowe w układzie nerwowym oraz w jaki sposób dzieje się to na poziomie komórkowym.
Lek sercowy wkracza do badań nad bólem
Nikorandyl rutynowo przepisywany jest w leczeniu dusznicy, ponieważ rozszerza naczynia krwionośne. Dokonuje tego poprzez dwa główne mechanizmy: dostarczanie niewielkich ilości tlenku azotu, który jest cząsteczką sygnałową, oraz otwieranie określonych kanałów potasowych w komórkach. Wcześniejsze badania na zwierzętach sugerowały, że nikorandyl może także zmniejszać ból, działając na receptory nerwowe związane z odczuwaniem ciepła i ostrości (jak po ostrej papryce) oraz angażując własny system opioidowy organizmu. W niniejszym badaniu badacze dążyli do odwzorowania, co dzieje się w dalszych etapach po tych początkowych efektach, koncentrując się na zapaleniu, stresie oksydacyjnym (rodzaj chemicznego „rdzewienia”) i konkretnych szlakach sygnałowych wewnątrz neuronów.
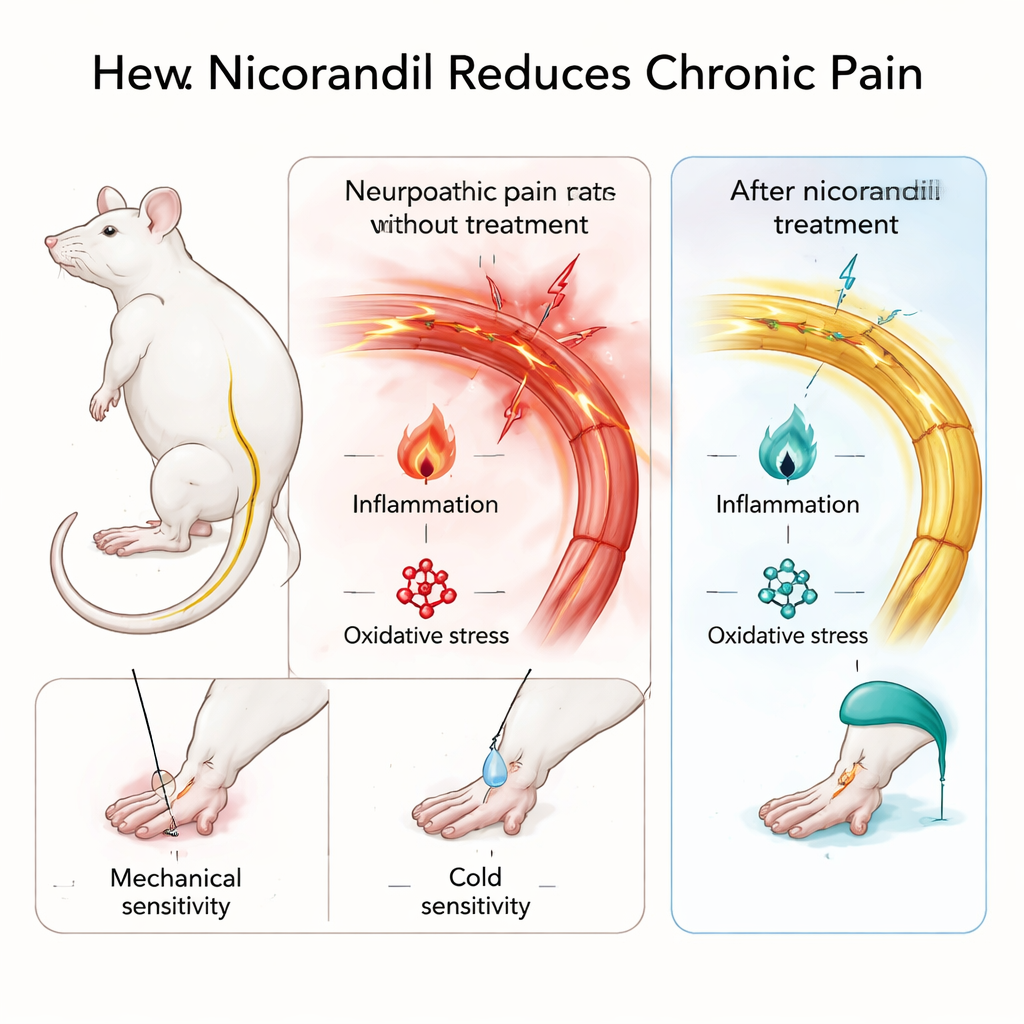
Testowanie nikorandyla w modelach przewlekłego bólu
Aby naśladować długotrwały ból nerwowy, zespół luźno związł nerw kulszowy u szczurów — klasyczny zabieg wywołujący nadwrażliwość na dotyk i zimno podobną do ludzkiego bólu neuropatycznego. Wykorzystano także test formalinowy, w którym łagodny środek drażniący jest wstrzykiwany do łapy, co wywołuje dobrze określony, dłużej trwający ból zapalny. Szczury otrzymywały nikorandyl doustnie w dwóch dawkach, a naukowcy mierzyli, jak silnie reagowały na lekkie dotknięcie i zimno na uszkodzonej łapie oraz ile lizów lub skurczów wykazywały po podaniu formaliny. Co ważne, nikorandyl nie powodował senności ani utraty równowagi w teście na otwartym polu, co sugeruje, że zmniejszenie zachowań związanych z bólem nie wynikało jedynie z sedacji.
Zmniejszanie chemicznych „sygnałów alarmowych”
Nikorandyl wyraźnie zmniejszył zarówno ból wywołany uszkodzeniem nerwu, jak i ból po formalinie. Leczone szczury lepiej znosiły dotyk i zimno oraz wykazywały mniej skurczów i krótszy czas lizania. Badania krwi wykazały, że nikorandyl obniżał poziomy silnych mediatorów zapalenia — czynnika martwicy nowotworu alfa (TNF-α) i interleukiny-6 (IL‑6) — oraz cyklooksygenazy‑2, enzymu wspomagającego produkcję prostaglandyn związanych z bólem. Obniżył także poziom malonodialdehydu, markera stresu oksydacyjnego, co wskazuje na mniejsze uszkodzenie chemiczne błon komórkowych. Pod mikroskopem nerwy od zwierząt leczonych nikorandylem wyglądały zdrowiej: odnotowano mniejsze uszkodzenia strukturalne i obrzęk w nerwie kulszowym oraz w zgrupowaniu komórek czuciowych zwanym zwojem rdzeniowym grzbietowym.
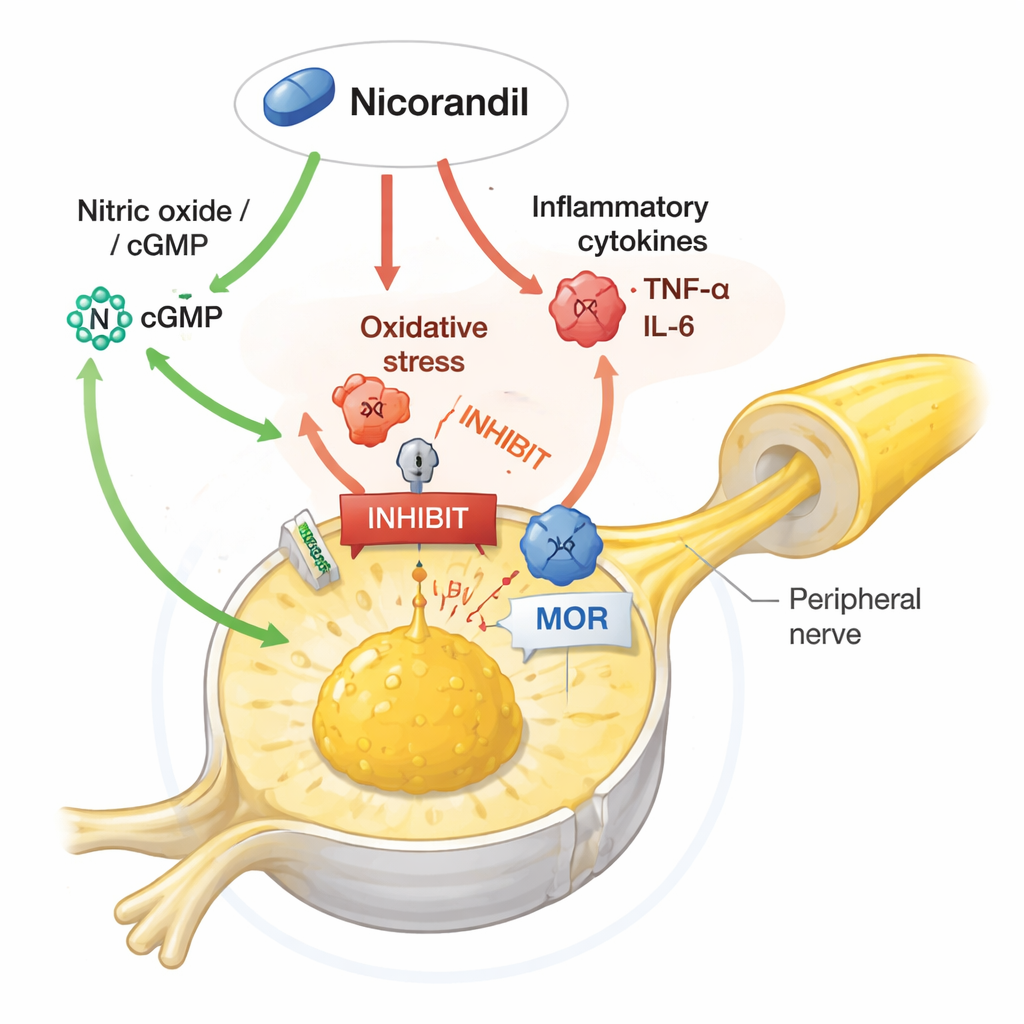
Rozplątywanie sieci sygnalizacyjnej w neuronach bólowych
Badanie poszło dalej, badając, które szlaki molekularne są niezbędne dla korzystnych efektów nikorandyla. Gdy badacze podawali leki, które zwiększały poziom tlenku azotu lub podnosiły cykliczny GMP (cząsteczkę przekaźnikową związaną z tlenkiem azotu), częściowo osłabiało to zdolność nikorandyla do redukcji bólu i normalizacji kluczowych białek. Nikorandyl zapobiegał typowemu wzrostowi ERK1/2 — członka rodziny kinaz MAP, który wzmacnia sygnały bólowe — i ograniczał poziomy TRPV1, kanału zwiększającego wrażliwość nerwów na ciepło i chemiczne drażniące substancje. Wzmacnianie sygnalizacji tlenku azotu lub cyklicznego GMP odwracało te ochronne zmiany, podczas gdy blokowanie enzymów wytwarzających tlenek azotu czasami wzmacniało działanie przeciwbólowe nikorandyla. Zaskakująco, blokada kanałów potasowych, które nikorandyl słynie z otwierania, nie znosiła jego efektów przeciwbólowych, co sugeruje, że w tym kontekście jego moc przeciwbólową wspierają bardziej modulacja tlenku azotu, stresu oksydacyjnego, zapalenia i sygnalizacji opioidowej niż klasyczne działanie naczyniowe.
Co to może oznaczać dla osób z bólem
W sumie wyniki przedstawiają nikorandyl jako wielocelowy modulator bólu: uspokaja nadaktywne szlaki nerwowe przez zmniejszenie uszkodzeń oksydacyjnych i mediatorów zapalenia, wyciszanie ERK1/2 i TRPV1 w neuronach czuciowych oraz interakcję z tlenkiem azotu i własnym systemem opioidowym organizmu. Chociaż wyniki pochodzą z modeli na szczurach i krótkotrwałego podawania, sugerują, że lek już stosowany klinicznie w chorobach serca mógłby w przyszłości zostać zaadaptowany lub ponownie wykorzystany w leczeniu trudnych przypadków bólu neuropatycznego i zapalnego. Konieczne będą dalsze badania u ludzi, aby ustalić bezpieczne dawki, efekty długoterminowe oraz czy te same mechanizmy ochronne działają w ludzkich nerwach.
Cytowanie: Badr, R.M., Abuiessa, S.A., Elblehi, S.S. et al. Nicorandil ameliorates neuropathic and inflammatory pain via TNF-α, IL6/MAPKERK1/2 and NO/cGMP signaling. Sci Rep 16, 4722 (2026). https://doi.org/10.1038/s41598-026-35272-4
Słowa kluczowe: ból neuropatyczny, nikorandyl, zapalenie, stres oksydacyjny, sygnalizacja tlenku azotu