Clear Sky Science · pl
Geny związane z deubikwitynacją definiują podtypy immunologiczne raka jelita grubego i korelują z rokowaniem oraz sygnaturami związanymi z immunoterapią
Dlaczego to badanie ma znaczenie dla ludzi
Rak jelita grubego jest jednym z najczęściej występujących i najbardziej śmiertelnych nowotworów na świecie, jednak u osób z guzem o podobnym wyglądzie pod mikroskopem przebieg choroby i odpowiedź na nowoczesne terapie, takie jak immunoterapia, mogą się znacząco różnić. W tym badaniu zadano nowe pytanie: czy można lepiej podzielić raki jelita grubego na jasne grupy, badając, jak komórki nowotworowe radzą sobie z „przetwarzaniem” białek oraz jak to łączy się z odpowiedzią immunologiczną organizmu? Odpowiedź może pomóc lekarzom lepiej przewidywać rokowanie i w przyszłości projektować mądrzejsze kombinacje terapii.
Sprzątanie białek a zachowanie nowotworu
W każdej komórce zużyte lub uszkodzone białka są znakowane i poddawane recyklingowi, aby nie gromadziły się i nie powodowały szkód. Jedna z gałęzi tego systemu, zwana deubikwitynacją, usuwa te znaczniki i pomaga precyzyjnie regulować, które białka są niszczone, a które zachowywane. Autorzy zgromadzili obszerne publiczne zbiory danych dotyczące guzów jelita i tkanek zdrowych oraz przeskanowali tysiące genów, by znaleźć te powiązane zarówno z tym systemem czyszczenia białek, jak i z przeżyciem pacjentów. Zawęzili listę do 17 kluczowych genów silnie związanych z kontrolą podziałów komórkowych, naprawą uszkodzeń DNA i strukturą macierzy otaczającej komórki. Te geny stały się podstawą nowego sposobu grupowania raków jelita grubego.
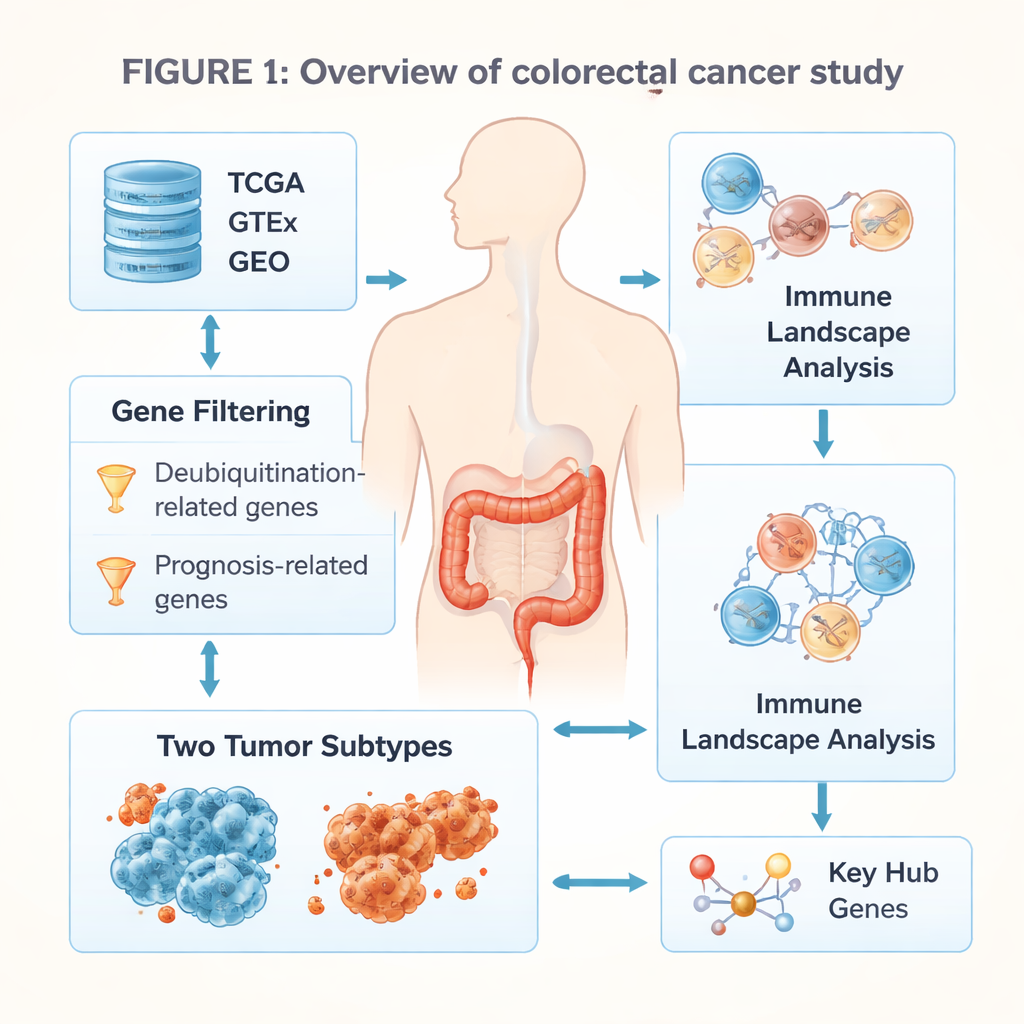
Pojawiają się dwa główne typy guza
Na podstawie wzorców aktywności tych 17 genów badacze podzielili guzy na dwa główne podtypy. Osoby w jednej grupie miały tendencję do dłuższego przeżycia i występowania choroby we wcześniejszym stadium. Druga grupa miała gorsze rokowanie. Gdy zespół spojrzał szerzej na to, które geny były włączone lub wyłączone w każdym podtypie, okazało się, że grupa o złym rokowaniu wykazywała silne sygnały szybkiego wzrostu komórek, odpowiedzi na stres związany z uszkodzeniem DNA i intensywnej przebudowy rusztowania tkankowego otaczającego guz. W przeciwieństwie do tego, grupa o lepszym rokowaniu charakteryzowała się mniejszą agresywną przebudową i bardziej zrównoważonym wzorcem wzrostu i naprawy komórek.
Sąsiedztwo guza i odpowiedź immunologiczna
Nowotwór nie rośnie w izolacji; funkcjonuje w sąsiedztwie komórek odpornościowych, komórek stromalnych i tkanki przypominającej bliznę. W badaniu użyto narzędzi obliczeniowych do oszacowania, które komórki odpornościowe występują w każdym guzie. Dwa podtypy wykazały wyraźnie różne krajobrazy immunologiczne. Podtyp o złym rokowaniu był wzbogacony w gęsty kolagen i włóknistą tkankę, tworząc barierę fizyczną i chemiczną, która może utrudniać dostęp komórkom T walczącym z rakiem. Nosił też sygnały supresji immunologicznej i wyższe wyniki w miarach przewidujących oporność na immunoterapię. Podtyp o lepszym rokowaniu miał słabsze nagromadzenie macierzy, korzystniejsze mieszanki komórek odpornościowych, takich jak cytotoksyczne limfocyty T i limfocyty pomocnicze, oraz wyniki sugerujące większą potencjalną wrażliwość na terapie oparte na układzie odpornościowym.
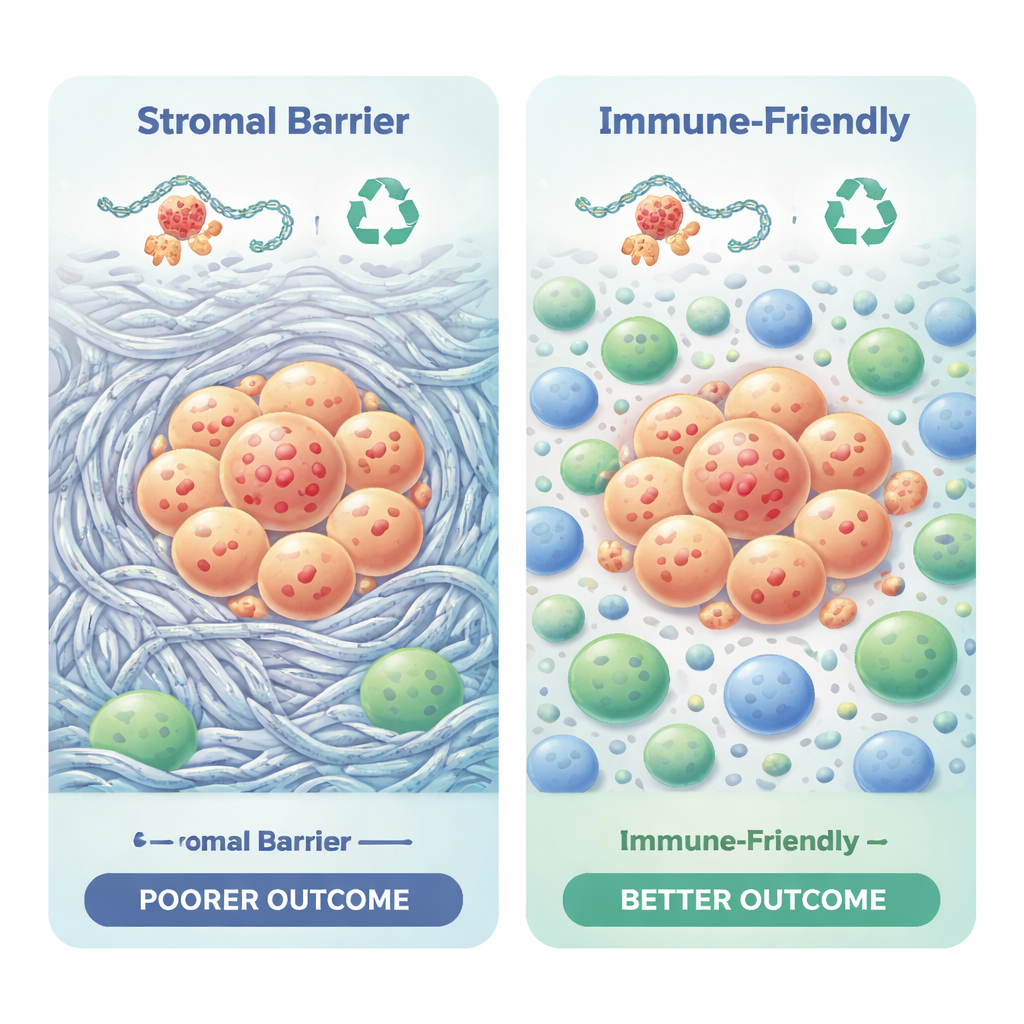
Kluczowe geny strukturalne jako sygnalizatory ostrzegawcze
Aby przejść od szerokich wzorców do praktycznych markerów, autorzy zbudowali sieci białkowych interakcji i poszukiwali centralnych genów „węzłowych”. Zidentyfikowali dziewięć genów głównie zaangażowanych w budowę i przebudowę otaczającego guza rusztowania, w tym kilka kolagenów oraz cząsteczek takich jak fibryonektyna i periostyna. Wysoka aktywność niektórych z tych genów, szczególnie BGN, FN1 i POSTN, konsekwentnie sygnalizowała gorsze przeżycie w dwóch niezależnych grupach pacjentów. Te geny węzłowe znajdują się na skrzyżowaniu sztywności mechanicznej, sygnalizacji chemicznej i rekrutacji komórek odpornościowych, co czyni je atrakcyjnymi kandydatami do przyszłych testów, które mogłyby pomóc przewidywać ryzyko lub ukierunkowywać wybór terapii.
Co to oznacza na przyszłość
To opracowanie nie zmienia jeszcze sposobu leczenia pacjentów, ponieważ opiera się na analizie komputerowej istniejących danych, a nie na nowych badaniach klinicznych. Mimo to daje klarowne, ogólne przesłanie: sposób, w jaki guz jelita grubego zarządza recyklingiem białek i przekształca swoje lokalne otoczenie, zdaje się wpływać na to, czy układ odpornościowy może do niego dotrzeć i go zaatakować. Guzy z silnie zaburzoną kontrolą białek i grubą, włóknistą powłoką mają tendencję do odpychania komórek odpornościowych i wiążą się z gorszymi wynikami, podczas gdy guzy z mniejszym bliznowaceniem i bardziej otwartym dostępem dla komórek odpornościowych radzą sobie lepiej. W przyszłości łączenie leków celujących w naprawę DNA lub macierz włóknistą z immunoterapią może okazać się szczególnie korzystne dla grupy wysokiego ryzyka zdefiniowanej w tym badaniu.
Cytowanie: Xu, Y., Mo, Z., Jiang, Q. et al. Deubiquitination-related genes define immune subtypes of colorectal cancer and are associated with prognosis and immunotherapy-related signatures. Sci Rep 16, 4862 (2026). https://doi.org/10.1038/s41598-026-35271-5
Słowa kluczowe: rak jelita grubego, mikrośrodowisko nowotworu, podtypy immunologiczne, degradacja białek, immunoterapia