Clear Sky Science · pl
Zakłócenie homeostazy cynku obniża poziomy acetylacji histonów w komórkach normalnych i nowotworowych
Kiedy pomocny metal staje się szkodliwy
Cynk jest najbardziej znany jako składnik multiwitamin wspierający nasz układ odpornościowy i gojenie ran. Jednak wewnątrz komórek cynk musi być utrzymywany w bardzo wąskim, „w sam raz” zakresie. Badanie to pokazuje, że gdy poziomy cynku w komórkach stają się zbyt wysokie, mogą one cicho wyłączać ważne geny poprzez dokręcenie pakowania DNA, a nawet skłaniać komórki do procesu samooczyszczania zwanego autofagią. Ponieważ suplementy cynku, składniki przeciwłupieżowe i eksperymentalne leki przeciw nowotworom mogą zmieniać poziomy cynku, zrozumienie tego ukrytego systemu kontroli ma znaczenie dla codziennego zdrowia i przyszłych terapii.
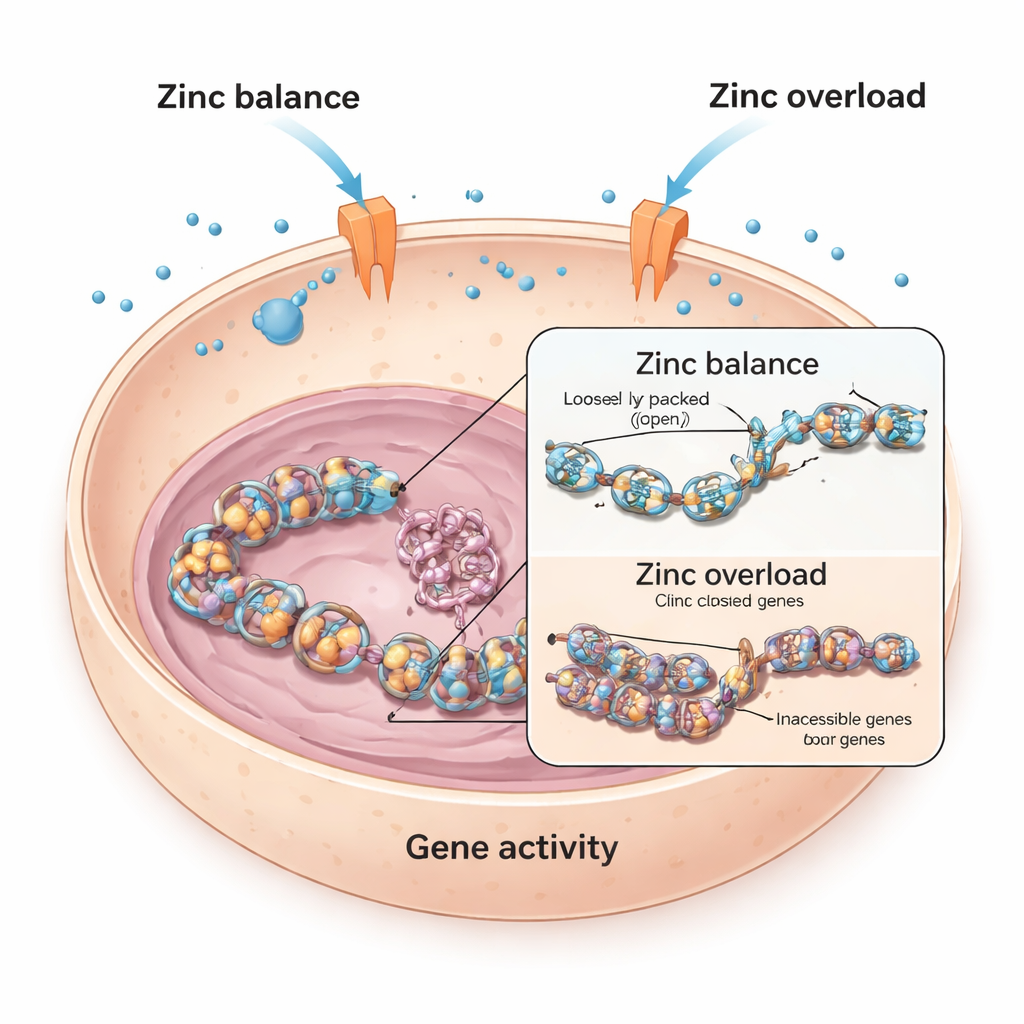
Równoważenie cynku wewnątrz żywych komórek
Każda komórka polega na cynku, który pomaga tysiącom białek wykonywać ich zadania. Aby uniknąć zarówno niedoboru, jak i przeciążenia, komórki używają specjalnych „bramek” w błonach — transporterów cynku — do przemieszczania cynku na zewnątrz i do wewnątrz. Badacze zaczęli od komórek mięśnia sercowego myszy i ludzi, pytając, co się dzieje, gdy te komórki są wystawione na dodatkowy cynk. Stwierdzili, że w mysich komórkach serca wysokie poziomy cynku silnie obniżały aktywność kluczowego genu związanego z sercem, nazwanego Bmp4, który pomaga kierować rozwojem i funkcją serca. Natomiast ludzkie komórki sercowe były znacznie mniej dotknięte, co sugeruje, że różne komórki bronią się przed nadmiarem cynku w różny sposób.
Jak cynk uszczelnia pakowanie DNA
Aby odkryć, jak cynk wycisza geny takie jak Bmp4, zespół przyjrzał się histonom — białkom działającym jak szpule, wokół których owinięte jest DNA. Gdy do histonów dodawane są małe chemiczne znaczniki zwane grupami acetylowymi, DNA staje się luźniejsze i łatwiej dostępne; gdy te znaczniki są usuwane, DNA pakuje się ciaśniej i geny trudniej jest włączać. Badanie wykazało, że nadmiar cynku w mysich komórkach serca prowadził do spadku acetylacji histonów w konkretnym miejscu (znanym jako H3K9), co ściśle współgrało z obniżeniem aktywności Bmp4. Leki blokujące enzymy deacetylujące histony mogły cofnąć efekt cynku i przywrócić poziom Bmp4, co sugeruje, że cynk przechyla równowagę w tym systemie chemicznego znakowania.
Zbyt dużo cynku wewnątrz, nie tylko na zewnątrz
Kluczowym krokiem okazał się cynk w cytoplazmie komórki, a nie tylko w otaczającym płynie. Korzystając z fluorescencyjnego czujnika, który świeci w obecności wolnego cynku, badacze zaobserwowali gwałtowny wzrost cynku wewnątrz mysich komórek serca po leczeniu. Kiedy zastosowali molekułę transportującą cynk, aby wymusić jego bezpośrednie wejście do komórek, zaobserwowali ten sam spadek acetylacji histonów i aktywności genów, nawet przy znacznie niższym cynku w medium zewnętrznym. W komórkach sercowych ludzkich, w przeciwieństwie do tego, transportery w błonie komórkowej szybko się dostosowały: niektóre importery cynku wyciszyły się, a eksportery przyspieszyły, zapobiegając dużemu wzrostowi wewnętrznego cynku i chroniąc acetylację histonów. Mysie komórki serca wykazywały bardziej „niezgrane” odpowiedzi transporterów, pozwalając większej ilości cynku napłynąć i zaburzyć kontrolę genów.
Od kontroli genów do samooczyszczania w komórkach normalnych i nowotworowych
Badacze pytali następnie, czy to napędzane cynkiem uszczelnianie pakowania DNA jest unikalne dla komórek serca. Testowali kilka normalnych ludzkich typów komórek oraz linie komórkowe nowotworów żołądka, macicy i jajnika. Gdy cynk dopuścili do nagromadzenia się wewnątrz za pomocą nośnika, niemal wszystkie te komórki wykazały wyraźny spadek acetylacji histonów. W niektórych komórkach nowotworowych, takich jak komórki raka żołądka, działo się to przy szczególnie niskich dawkach cynku, co sugeruje, że niektóre nowotwory są niezwykle wrażliwe na zaburzenia równowagi cynku. Zespół powiązał także obniżoną acetylację z autofagią — procesem, w którym komórki recyklingują zużyte elementy. Umiarkowane zwiększenie wewnętrznego cynku nasilało autofagię, ale bardzo wysokie jego stężenia ostatecznie ją osłabiały, co sugeruje wąskie okno, w którym cynk mógłby służyć do precyzyjnego modulowania tej ścieżki samooczyszczania.
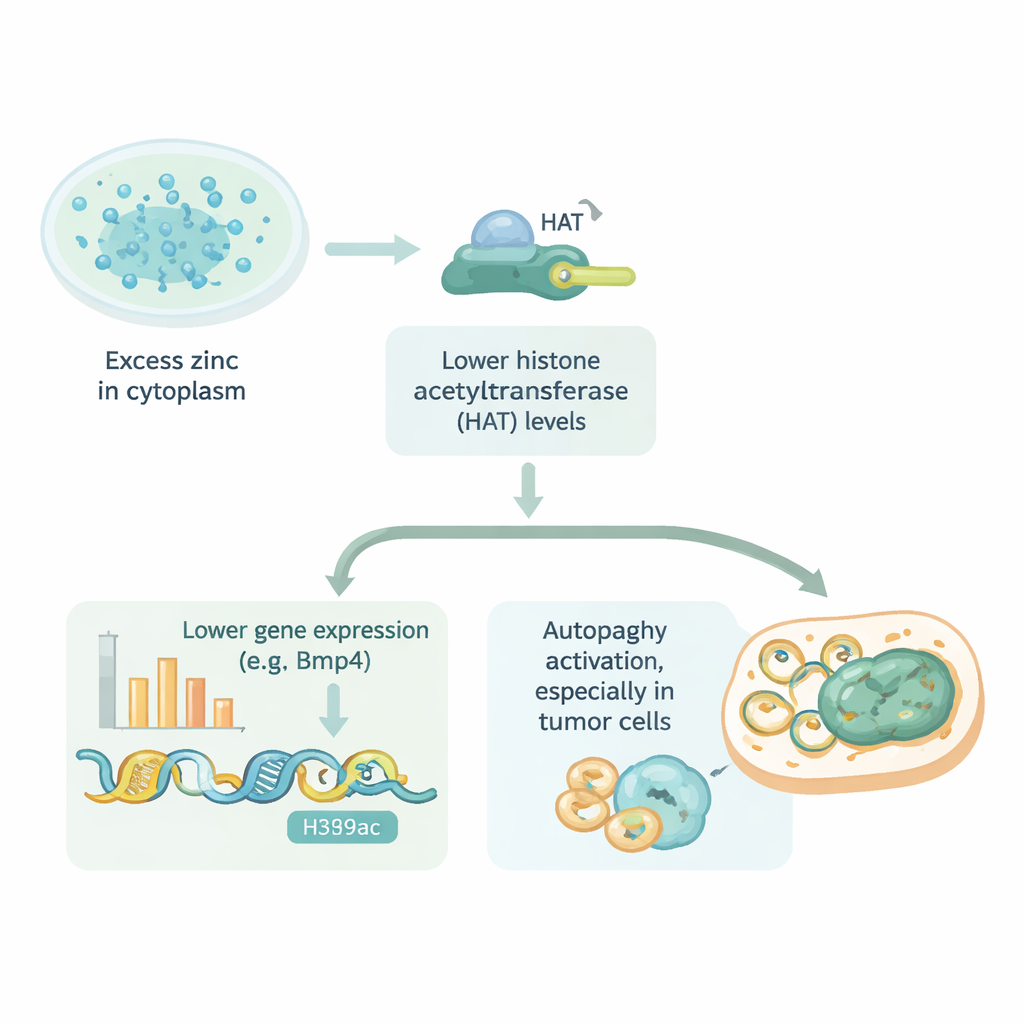
Co to oznacza dla zdrowia i leczenia
Mówiąc krótko, praca ta ujawnia, że nadmiar cynku wewnątrz komórek może wyciszać geny poprzez utrudnianie dostępu do DNA, a ta sama ścieżka może wpływać na aktywność procesów samooczyszczania komórek. Efekt nie ogranicza się do komórek serca; pojawia się w różnych komórkach normalnych i nowotworowych, choć niektóre lepiej bronią się przed przeciążeniem cynkiem niż inne. Te obserwacje sugerują, że maleńkie „bramki” transportujące cynk w błonach komórkowych mogą być obiecującymi celami leków — albo by chronić zdrowe tkanki przed uszkodzeniem związanym z cynkiem, albo by popychać wrażliwe komórki nowotworowe w kierunku śmierci. Choć wyniki pochodzą z eksperymentów na hodowlach komórkowych, dostarczają nowej perspektywy na to, jak powszechny składnik odżywczy może kształtować aktywność genów i chorobę, gdy jego delikatna równowaga zostanie zaburzona.
Cytowanie: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Słowa kluczowe: homeostaza cynku, regulacja genów, acetylacja histonów, autofagia, komórki nowotworowe