Clear Sky Science · pl
Przeprogramowanie metaboliczne zwiększa odporność na stres oksydacyjny w różnicujących się kardiomiocytach
Dlaczego walka komórek serca z tlenem ma znaczenie
Każde uderzenie serca zależy od wyspecjalizowanych komórek mięśniowych zwanych kardiomiocytami. W miarę rozwoju organizmu komórki te przechodzą dramatyczną zmianę życiową: z niskotlenowego, zasilanego głównie glukozą środowiska płodowego trafiają po urodzeniu do świata bogatego w tlen. Tlen jest niezbędny, ale jednocześnie generuje szkodliwe produkty uboczne, które mogą uszkadzać DNA i zabijać komórki. W tym badaniu analizowano, jak dojrzewające komórki serca przebudowują swój metabolizm, aby lepiej radzić sobie z większą ilością tlenu, produkować więcej energii i jednocześnie chronić się przed uszkodzeniami oksydacyjnymi — wnioski, które mogą mieć znaczenie dla przyszłych terapii chorób serca i regeneracji.
Z prostych budowniczych w energetycznych atletów
Niedojrzałe komórki serca, nazywane kardiomioblastami, to małe, dzielące się komórki, które w dużej mierze polegają na rozkładzie glukozy jako źródle energii. W miarę różnicowania w dojrzałe kardiomiocyty przestają się dzielić i stają się większe, często łącząc się w polinuklearne, wydłużone komórki lepiej przystosowane do silnych skurczów. Dzięki mikroskopii wysokiej rozdzielczości badacze obserwowali tę przemianę przez dziesięć dni w modelu komórkowym in vitro. Markery proliferacji komórek spadły, podczas gdy komórki wydłużały się i reorganizowały w włókniste, przypominające serce struktury, co potwierdziło wejście w bardziej dorosły, kurczliwy stan. 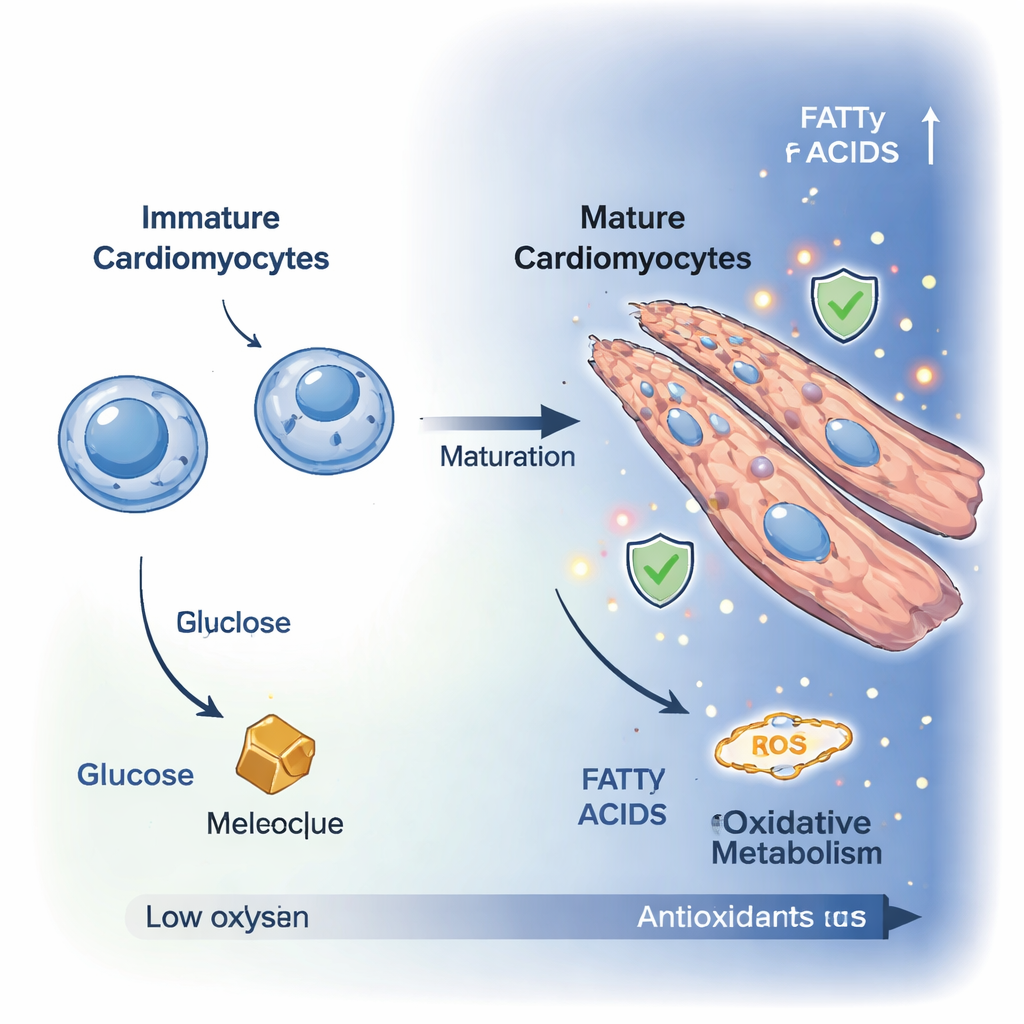
Zmiana źródeł paliwa i przełączanie nowych dróg energetycznych
Aby zrozumieć, co dzieje się „pod maską”, zespół zmierzył setki małych cząsteczek wewnątrz komórek i zastosował zaawansowane obrazowanie naturalnej fluorescencji komórek, aby śledzić wykorzystanie energii w czasie rzeczywistym. Te techniki wykazały wyraźne przesunięcie ze stanu glikolitycznego, w którym komórki głównie spalają glukozę, do stanu oksydacyjnego zdominowanego przez respirację mitochondrialną. Poziomy glukozy i fruktozy spadły, podczas gdy wzrosły pośrednie związki cyklu kwasu trójkarboksylowego (TCA) — takie jak kwas cytrynowy, jabłczan i oksoglutaran. Analiza szlaków metabolicznych ujawniła zwiększoną aktywność dróg dostarczających paliwo do mitochondriów, w tym pompy jabłczan–asparaginian i rozkładu aminokwasów, co wskazuje, że dojrzałe kardiomiocyty rozszerzają spektrum paliw i efektywniej kierują energię do swoich „elektrowni”.
Życie przy większej ilości tlenu — i większym stresie
Bardziej wydajne spalanie paliwa w mitochondriach ma swoją cenę: wyższą produkcję reaktywnych form tlenu (ROS), chemicznie agresywnych cząsteczek, które mogą uszkadzać lipidy, białka i DNA. Badacze stwierdzili, że wraz z dojrzewaniem kardiomiocytów ich mitochondria stawały się większe i bardziej wydłużone, a markery stresu oksydacyjnego wzrastały. Obrazowanie fluorescencyjne ujawniło więcej ziarnistości przypominających lipofuscynę — cechę utlenionych lipidów — a sondy jądrowe wykazały wyższe poziomy ROS w komórkach zróżnicowanych. Metabolomika wskazała na zmiany w metabolizmie glutationu, centralnego systemu antyoksydacyjnego, który wykorzystuje glutation — zbudowany z aminokwasów takich jak glutaminian i glicyna — do neutralizacji ROS. Wyniki te sugerują, że w miarę jak komórki serca zwiększają metabolizm oksydacyjny, jednocześnie regulują swoje szlaki antyoksydacyjne, aby utrzymać szkody w ryzach. 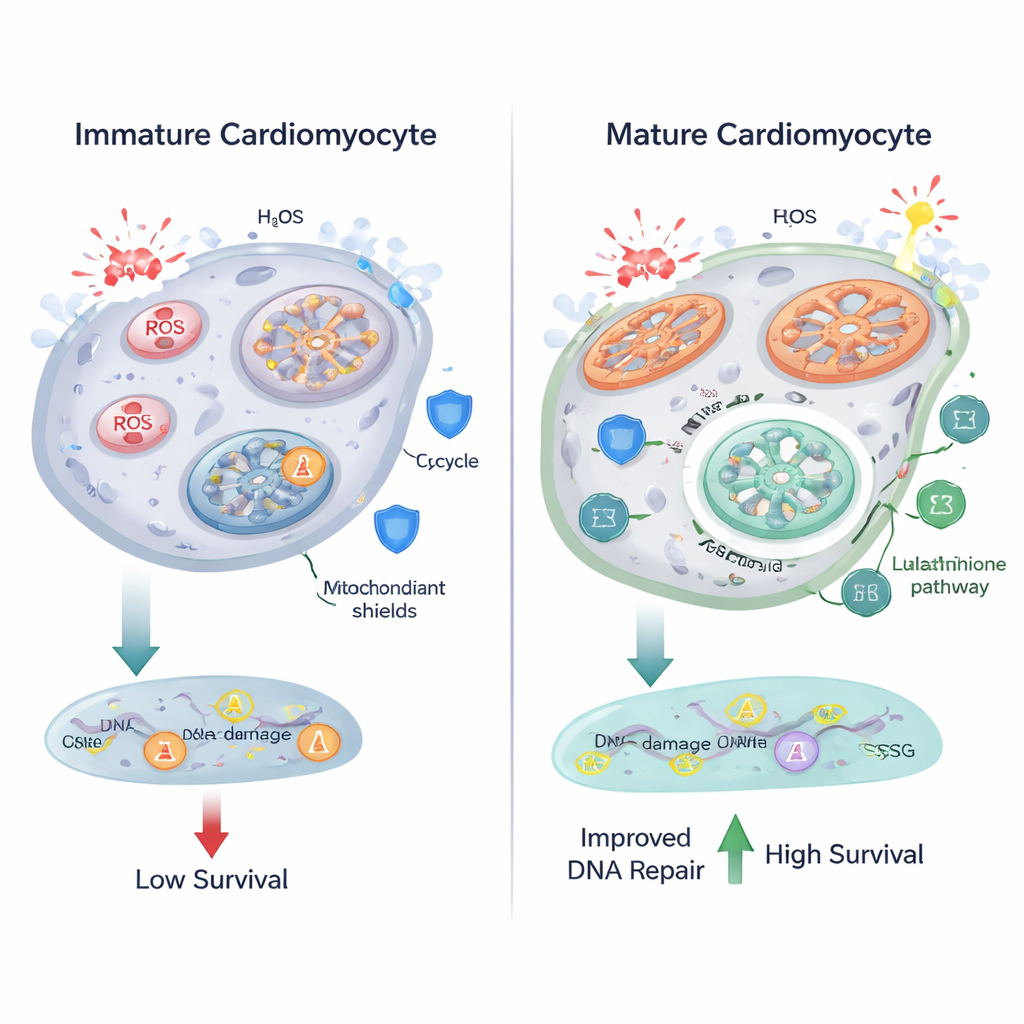
Szkody powstrzymane, obrony wzmocnione
Co zaskakujące, mimo wyższych poziomów ROS, zróżnicowane kardiomiocyty nie wykazywały większej liczby przerw w DNA niż ich niedojrzałe odpowiedniki przy pomiarze ognisk γ-H2AX, czułego markera uszkodzeń DNA. Gdy zespół wystawił komórki na działanie nadtlenku wodoru, silnego utleniacza, zarówno niedojrzałe, jak i dojrzałe komórki gromadziły ROS i uszkodzenia DNA — lecz komórki dojrzałe radziły sobie lepiej. Wykazywały proporcjonalnie mniej uszkodzeń DNA w stosunku do wyższych poziomów ROS, były mniej skłonne do aktywacji sygnałów związanych ze śmiercią komórkową, takich jak PUMA, i prezentowały wyraźnie wyższe wskaźniki przeżycia. Wyniki te wskazują, że dojrzewające kardiomiocyty nie tylko dostosowują swój metabolizm, ale też wzmacniają mechanizmy naprawy DNA i aparaty przetrwania, co pozwala im wytrzymać surowsze warunki oksydacyjne.
Co to oznacza dla ochrony serca
Mówiąc prościej: badanie pokazuje, że w miarę dojrzewania komórki serca uczą się pracować „goręcej” bez spalania się. Przechodzą ze stylu życia opartego na cukrach i niskim dostępie tlenu do trybu intensywnie tlenowego, napędzanego przez mitochondria, jednocześnie budując lepsze tarcze i zespoły naprawcze, by radzić sobie ze stresem oksydacyjnym. Zrozumienie tej precyzyjnie wyregulowanej równowagi między produkcją energii a samoochroną może pomóc naukowcom opracować strategie zwiększające odporność uszkodzonej tkanki serca lub kierować komórki macierzyste ku bezpieczniejszym, trwalszym kardiomiocytom do terapii regeneracyjnych.
Cytowanie: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Słowa kluczowe: różnicowanie kardiomiocytów, stres oksydacyjny, mitochondria, metabolizm komórkowy, choroby serca