Clear Sky Science · pl
Prognozowanie choroby Alzheimera za pomocą głębokiego uczenia i XAI opartego na interpretowalnym doborze cech z danych ekspresji genów we krwi
Dlaczego te badania mają znaczenie
Choroba Alzheimera stopniowo odbiera ludziom pamięć i niezależność, a jednocześnie najdokładniejsze dziś dostępne testy często wymagają skanów mózgu lub nakłuć lędźwiowych, które są kosztowne, inwazyjne i trudne do powtarzania. Badanie to analizuje mniej obciążającą alternatywę: wykorzystanie prostego pobrania krwi i zaawansowanej analizy komputerowej do wykrywania wzorców aktywności genów wskazujących na Alzheimera, co może otworzyć drogę do wcześniejszej i bardziej dostępnej diagnostyki.
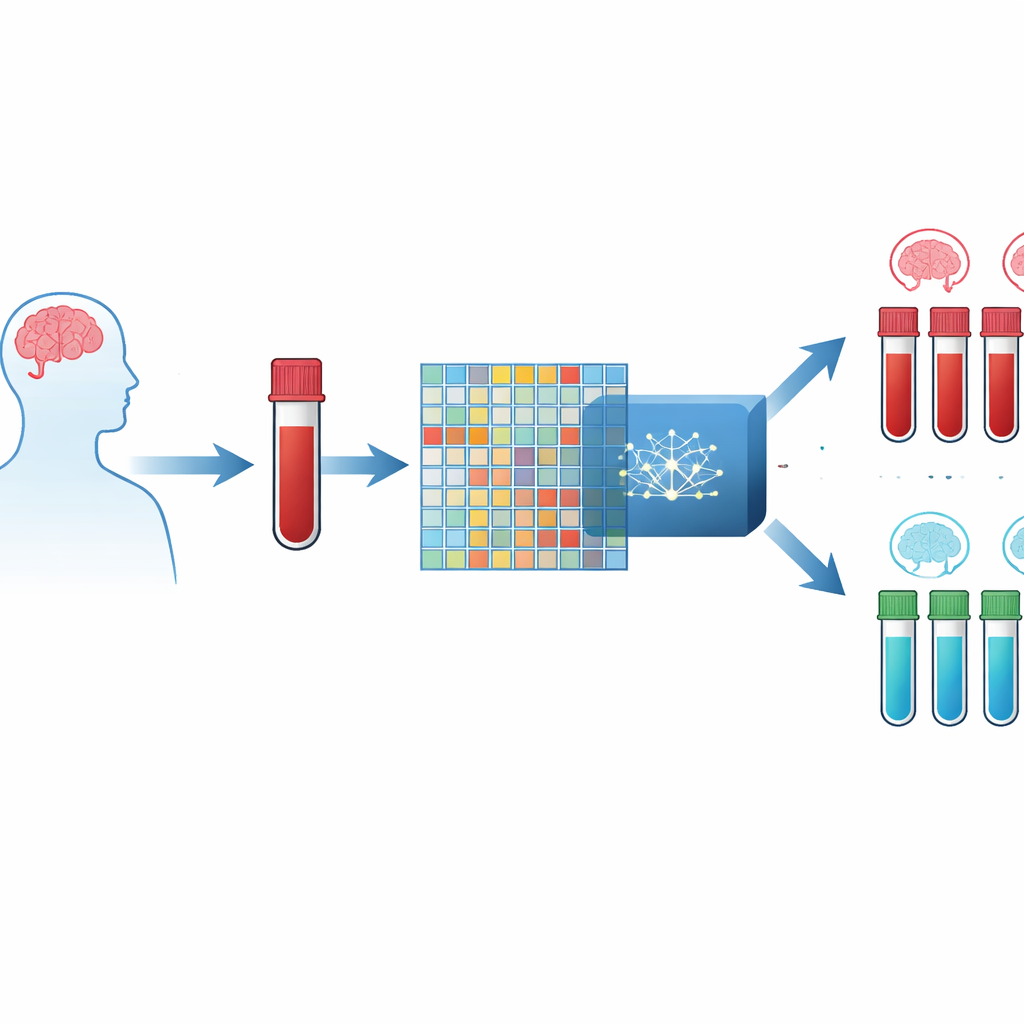
Badanie krwi zamiast skanu mózgu
Autorzy koncentrują się na drobnych zmianach w tym, jak geny są włączane lub wyłączane w komórkach krwi. Nowoczesne chipy laboratoryjne potrafią mierzyć aktywność tysięcy genów jednocześnie, generując ogromną tabelę liczb dla każdej osoby. Problem polega na tym, że pomiarów genów jest znacznie więcej niż pacjentów, co łatwo może wprowadzić modele komputerowe w błąd. Aby temu zaradzić, badacze połączyli trzy duże publiczne zbiory danych próbek krwi od osób z chorobą Alzheimera i od zdrowych ochotników, tworząc zintegrowane źródło z ponad dwunastoma tysiącami wspólnych genów zmierzonych u setek osób.
Nauka komputerów wybierania kluczowych sygnałów ostrzegawczych
Zamiast kazać algorytmowi analizować wszystkie dwanaście tysięcy genów, zespół najpierw nauczył go wybierać znacznie mniejszy zbiór szczególnie informatywnych genów. Porównali kilka sposobów dokonania tego doboru, w tym proste testy statystyczne, metody usuwające mniej użyteczne geny krok po kroku oraz podejścia wbudowujące selekcję bezpośrednio w model. Narzędzia do „wyboru cech” zawęziły listę do kilkuset lub nieco ponad tysiąca genów, które najlepiej odróżniały pacjentów od zdrowych kontrolnych. Zredukowane zbiory genów pomagały zapobiegać zapamiętywaniu szumu przez modele i poprawiały ich wydajność na nieznanych danych.
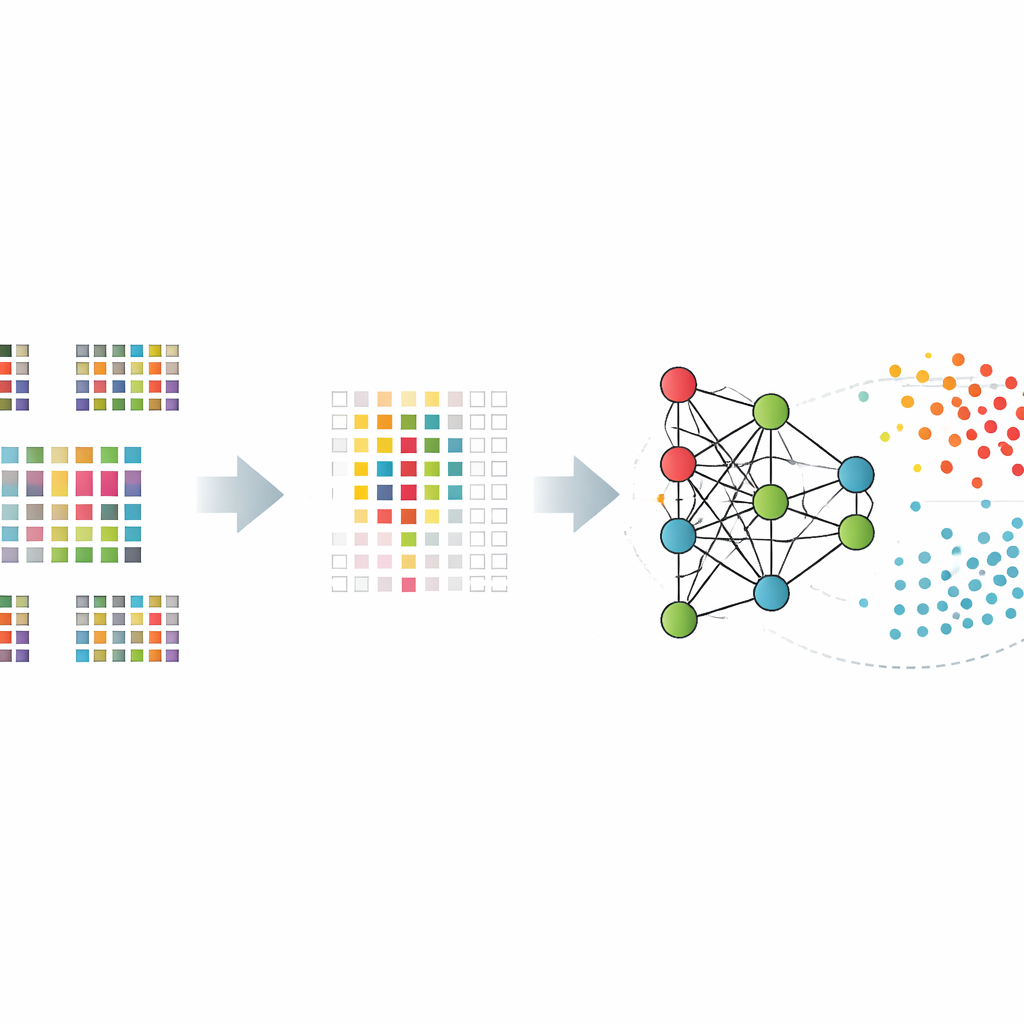
Rozumienie czarnej skrzynki
Aby uniknąć ślepego zaufania do prognozy „czarnej skrzynki”, badacze zastosowali techniki wyjaśnialnej sztucznej inteligencji, by zrozumieć, które geny miały największe znaczenie i jak wpływały na każdą decyzję. Metoda zwana SHAP, zapożyczona z teorii gier, ocenia wkład każdego genu w końcowy wynik dla danej osoby. Stosując ją do swoich najlepiej działających modeli, autorzy wyróżnili podstawową grupę genów, których wzorce aktywności konsekwentnie przechylały klasyfikację w stronę choroby Alzheimera lub stanu zdrowia. Wiele z tych genów już wcześniej powiązano ze zdrowiem mózgu lub funkcjami układu odpornościowego, co dodaje biologicznej wiarygodności wewnętrznym mechanizmom modelu.
Zwiększanie mocy dzięki syntetycznym pacjentom
Nawet po połączeniu zbiorów danych liczba rzeczywistych próbek krwi pozostała umiarkowana. Aby wzmocnić swoje modele, autorzy wytrenowali specjalny rodzaj sieci neuronowej, znany jako generative adversarial network, do tworzenia realistycznych syntetycznych profili ekspresji genów przypominających te z prawdziwych pacjentów. Te sztuczne próbki dodawano tylko do danych treningowych, nigdy do danych testowych, tak aby testy wydajności pozostały rzetelne. Dzięki tak rozszerzonemu zbiorowi treningowemu i starannie dobranym genom, głęboka sieć neuronowa była w stanie rozpoznać przypadki Alzheimera z około 91% ogólną skutecznością i 95% precyzją, co oznacza, że bardzo niewiele zdrowych osób zostało błędnie oznaczonych jako chore.
Co wyniki oznaczają dla pacjentów
Ta praca sugeruje, że przyszły test krwi na Alzheimera, wspierany przez inteligentne algorytmy, które zarówno wybierają, jak i wyjaśniają kluczowe sygnały genowe, mógłby uzupełniać lub nawet zmniejszać zależność od kosztownych badań obrazowych i procedur inwazyjnych. Choć potrzebna jest dalsza walidacja na niezależnych grupach pacjentów, a różnice między metodami laboratoryjnymi muszą być lepiej kontrolowane, badanie pokazuje, że łączenie wielu zbiorów danych, odsiewanie nieprzydatnych informacji oraz otwieranie „czarnej skrzynki” AI mogą przybliżyć nas do praktycznego, interpretowalnego testu krwi umożliwiającego wcześniejsze i wygodniejsze wykrywanie Alzheimera.
Cytowanie: Hariharan, J., Jothi, R. Alzheimer’s disease prediction using deep learning and XAI based interpretable feature selection from blood gene expression data. Sci Rep 16, 8022 (2026). https://doi.org/10.1038/s41598-026-35260-8
Słowa kluczowe: diagnoza choroby Alzheimera, biomarkery we krwi, ekspresja genów, głębokie uczenie, wyjaśnialna sztuczna inteligencja