Clear Sky Science · pl
Federowana segmentacja guzków płuc przy użyciu hybrydowej architektury transformer–U-Net
Dlaczego wykrywanie drobnych ognisk w płucach ma znaczenie
Rak płuca jest najtragiczniejszym w skutkach nowotworem na świecie, a jego najwcześniejsze oznaki — drobne zmiany zwane guzami na tomogramach — łatwo przeoczyć. Radiolodzy muszą przeglądać tysiące szczegółowych obrazów, a wymiana danych pacjentów między szpitalami w celu trenowania inteligentniejszych systemów często napotyka na surowe przepisy dotyczące prywatności. W tym badaniu przedstawiono sposób, w jaki szpitale mogą współpracować, by nauczyć system sztucznej inteligencji (AI) precyzyjnie wykrywać guzki płuc, nie wymieniając nigdy surowych skanów pacjentów.
Wymiana wiedzy bez przekazywania skanów
Nowoczesne tomografy komputerowe rejestrują szczegóły płuc z dokładnością do ułamków milimetra, ale ta precyzja generuje lawinę obrazów, których żadna osoba nie przejrzy samodzielnie. Narzędzia wspomagające komputerowo mogą pomóc, lecz potrzebują dużych, zróżnicowanych zbiorów danych, żeby nie przegapić nietypowych guzków. Przepisy takie jak HIPAA czy RODO uniemożliwiają szpitalom zwykłe zebranie danych pacjentów w jednym miejscu. Autorzy stosują strategię zwaną uczeniem federowanym, aby rozwiązać ten dylemat. Każdy szpital lokalnie trenuje kopię tego samego modelu na swoich tomogramach i przesyła jedynie wyuczone parametry modelu — nie obrazy — do centralnego serwera. Serwer uśrednia te parametry, tworząc ulepszony „globalny” model, i odsyła go z powrotem, dzięki czemu wszystkie placówki czerpią korzyści z doświadczeń innych, a dane pacjentów pozostają w miejscu ich powstania. 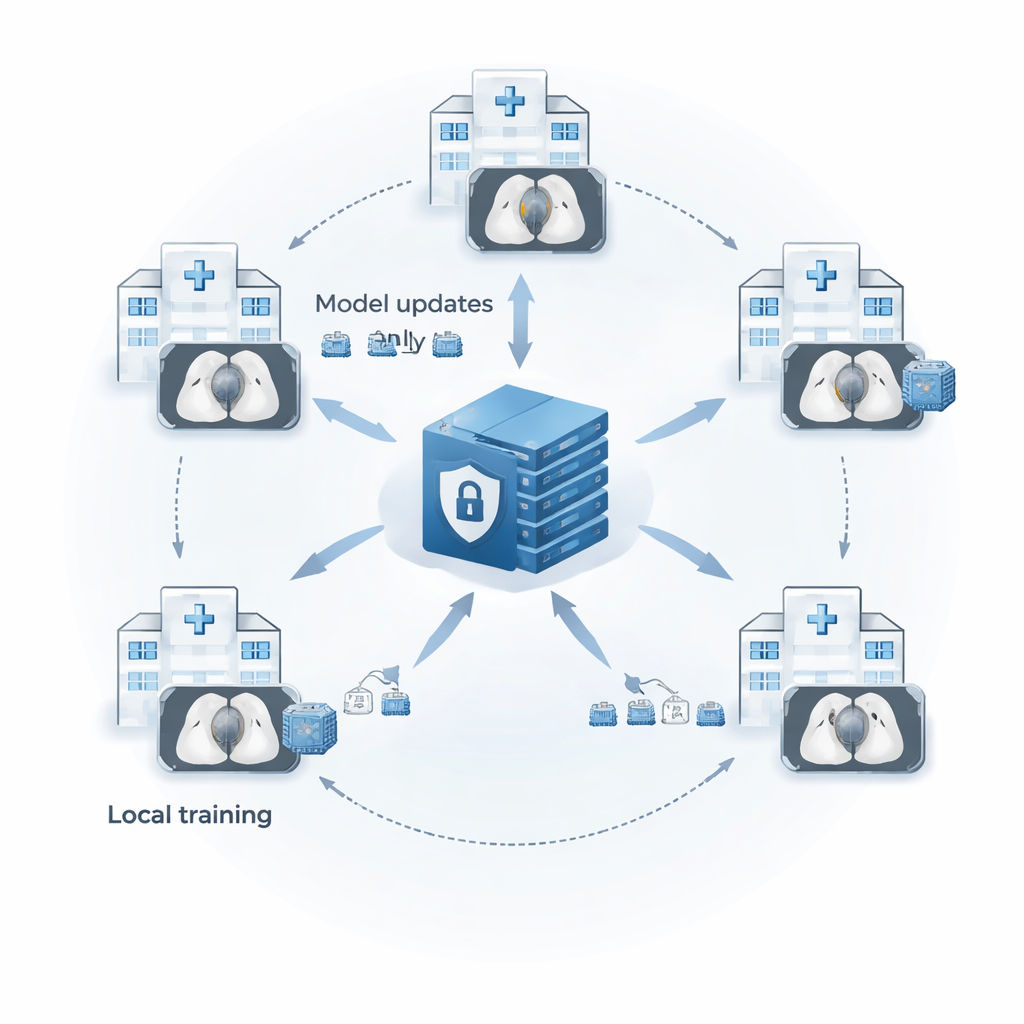
Oczyszczanie obrazów przed nauką AI
Badanie koncentruje się na „zwartych” guzach płuc o średnicy 15–25 milimetrów, które mają znaczenie kliniczne, lecz zajmują tylko kilka pikseli w pojedynczym przekroju CT, co ułatwia ich przeoczenie przez algorytmy. Zanim rozpocznie się proces uczenia, każdy przekrój CT przechodzi dwustopniowe oczyszczanie. Najpierw metoda zwiększania kontrastu nazwana CLAHE uwydatnia słabo widoczne guzki bez nadmiernego wzmacniania szumu, dzięki czemu subtelne zmiany są lepiej widoczne. Następnie obrazy są skalowane tak, aby wartości pikseli mieściły się w przedziale od 0 do 1, co daje modelowi spójną skalę jasności niezależnie od aparatu czy placówki. Ta ustandaryzowana wstępna obróbka pomaga AI skupić się na drobnych, niskokontrastowych guzach zamiast dawać się zmylić różnicami między skanerami.
Połączenie dwóch sposobów patrzenia: szczegół bliski i szerszy kontekst
W sercu systemu znajduje się sieć hybrydowa łącząca dwie potężne idei współczesnej AI: U-Net, który doskonale nadaje się do zaznaczania obiektów na obrazach, oraz Transformera, pierwotnie opracowanego do języka, a teraz powszechnie stosowanego w wizji komputerowej. Część w kształcie litery U najpierw kompresuje obraz przez warstwy drobnych filtrów wyspecjalizowanych w lokalnej teksturze — krawędziach, plamkach i cienkich granicach — a następnie rekonstruuje maskę w pełnym rozmiarze, oznaczając piksele należące do guzka. Połączenia resztkowe i skip connection przenoszą drobne szczegóły przez sieć, aby nie zostały utracone. W środku tej litery U znajduje się „korek” w postaci Transformera, który traktuje łatki obrazu jak tokeny w zdaniu i stosuje mechanizm self‑attention do powiązania odległych regionów. Dzięki temu model widzi zarówno maleńki guzek, jak i jego szersze otoczenie anatomiczne — co jest kluczowe, gdy guzki zlewają się z naczyniami lub strukturami klatki piersiowej. 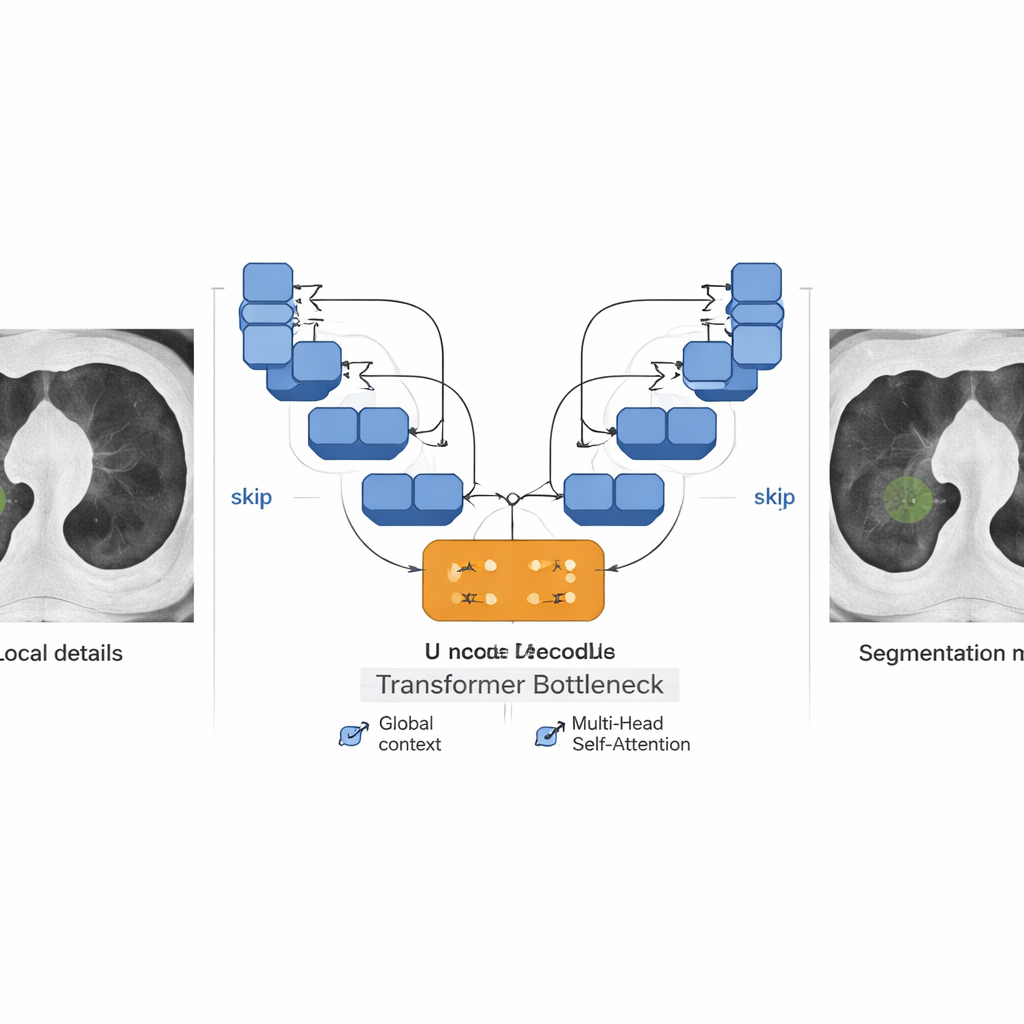
Radzenie sobie z rzadkimi celami i nierównymi danymi
Autorzy rozwiązują także istotny problem w obrazowaniu medycznym: niezrównoważenie klas. W tomografii płuc niemal każdy piksel to tło; piksele guzka są rzadkie. Standardowe treningi mają tendencję do faworyzowania modeli, które po prostu oznaczają wszystko jako tło. Aby temu zapobiec, zespół łączy dwie funkcje strat — stratę Dice, która bezpośrednio nagradza nakładanie się przewidywanych i rzeczywistych guzów, oraz stratę Focal, która kładzie dodatkowy nacisk na piksele trudne do sklasyfikowania. To połączenie Dice–Focal zachęca model do skupienia się na małych, trudnych guzach i wyraźnych granicach. W ich federowanym ustawieniu z pięcioma symulowanymi „klientami” szpitalnymi trenowanymi na publicznym zbiorze LUNA16 system osiągnął wartości Dice aż do 0,93 dla zwartych guzków oraz wykazał niskie wskaźniki zarówno pominiętych guzów, jak i fałszywych alarmów. Wydajność pozostała wysoka w większości klientów pomimo różnic w jakości obrazu i wyglądzie guzków, chociaż guzki o rozmytej lub mieszanej gęstości wciąż stanowiły wyzwanie.
Co to oznacza dla przyszłych badań przesiewowych płuc
Mówiąc krótko, praca pokazuje, że szpitale mogą wspólnie trenować wysokiej jakości AI do wykrywania guzków, nie przesyłając nigdy skanów pacjentów przez sieć. Dzięki połączeniu starannej obróbki obrazów, modelu widzącego zarówno detale, jak i kontekst, oraz strategii treningowej dostosowanej do rzadkich celów, ramy te niezawodnie wyznaczają obwiednie zwartych guzków płuc w realistycznym, wieloszpitalnym środowisku. Choć potrzeba dalszych badań, by poradzić sobie z bardzo słabo widocznymi lub częściowo zwartymi guzami, badanie wskazuje kierunek dla narzędzi przesiewowych raka płuca, które są jednocześnie dokładne i chronią prywatność — przynosząc korzyści płynące z AI opartej na dużych zbiorach danych pacjentom, bez naruszania poufności ich obrazów medycznych.
Cytowanie: Turjya, S.M., Fawakherji, M. Federated lung nodule segmentation using a hybrid transformer–U-Net architecture. Sci Rep 16, 5228 (2026). https://doi.org/10.1038/s41598-026-35243-9
Słowa kluczowe: badania przesiewowe raka płuca, segmentacja obrazów medycznych, uczenie federowane, guzki płuc w tomografii komputerowej, Sztuczna inteligencja z zachowaniem prywatności